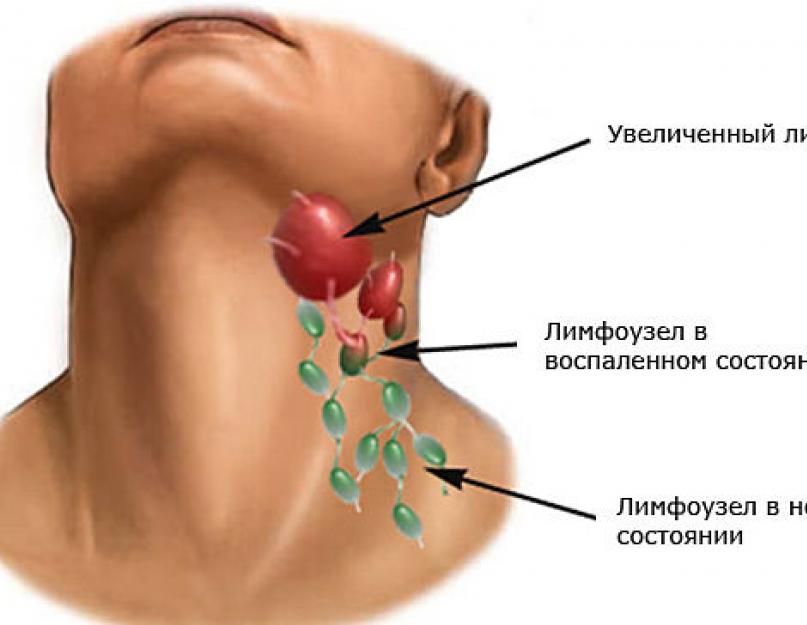
Perifeerse ja vistseraalse suurenemine lümfisõlmed on kõige sagedasem patoloogiline seisund, millega arst kokku puutub üldpraktika. Lümfadenopaatia etioloogia võib olla tingitud erinevatest teguritest: nakkustekitaja, autoimmuunpatoloogia või kasvaja iseloom. Patoloogilise protsessi varases staadiumis on väga oluline eristada reaktiivset lümfadenopaatiat kasvajast. Lümfoomide ja lümfogranulomatoosi puhul on lümfadenopaatia oluline kliiniline ilming.
Põhimõisted ja terminid
Lümfadenopaatia, normaalsete, reaktiivsete ja kasvajaliste lümfisõlmede morfoloogia, lümfadenopaatia etioloogia, lümfadenopaatia sündroomiga nakkushaigused, immunopatoloogilised haigused, immunokompetentse süsteemi kasvajad, metastaatilised kasvajad, ladestushaigused, endokrinopaatiad, diferentsiaaldiagnostika lümfadenopaatia, piirkondliku või lokaalse lümfadenopaatia diagnostiline otsingualgoritm, lümfogranulomatoosi kliinilised ja diagnostilised tunnused, mitte-Hodgkini lümfoomide kliinilised ja diagnostilised tunnused.
Valdkonna erialaste kompetentside kujundamisele suunatud teadmised, oskused ja vilumused meditsiiniline tegevus
Lümfadenopaatia peamised tunnused;
Lokaalse, piirkondliku ja generaliseerunud lümfadenopaatiaga esinevate haiguste klassifikatsioon;
Lümfadenopaatiaga hematopoeetiliste ja mittehematopoeetiliste süsteemide haiguste kliinilised ilmingud, õigeaegse diagnoosimise meetodid, diferentsiaaldiagnostika;
Diagnostiline otsingualgoritm lokaalse ja piirkondliku lümfadenopaatia jaoks;
Lümfogranulomatoos: peamised kliinilised ja diagnostilised tunnused;
Mitte-Hodgkini lümfoomid: peamised kliinilised ja diagnostilised tunnused;
Peamised ravimeetodid lümfogranulomatoosi ja mitte-Hodgkini lümfoomide ravis.
Lümfadenopaatiaga patsientide anamneesi kogumine, kaebuste täpsustamine, lümfoomide, metastaatiliste, põletikuliste, nakkusprotsesside, sidekoehaiguste, AIDSi peamiste sümptomite ja sündroomide määramine;
Viia läbi lümfadenopaatiaga, pahaloomuliste, põletikuliste, reaktiivsete lümfisõlmede nähtudega patsientide füüsiline läbivaatus;
Põhjendada mitte-Hodgkini pahaloomulise lümfoomi diagnoosi kliiniliste, laboratoorsete ja instrumentaalsed meetodid uuringud;
Põhjendage lümfogranulomatoosi (Hodgkini tõbi) diagnoosimist kliiniliste, laboratoorsete ja instrumentaalsete uurimismeetodite tulemuste põhjal, viige läbi diferentsiaaldiagnostika ägeda leukeemia, kroonilise lümfotsütaarse leukeemia, mitte-Hodgkini lümfoomide korral;
Valmistage ette haiguslugu ja vastuvõtuleht.
Lümfogranulomatoosi (Hodgkini tõve) diagnoosimise algoritm
Definitsioon, patogenees ja eelsoodumustegurid. PH on primaarne kasvajahaigus, mida iseloomustab lümfoidkoe hüperplaasia koos lümfogranuloomide moodustumisega. Iseloomulikud on kaks vanusepiiki: 15-30 aastat - meestel ja naistel võrdselt sageli; vanemad kui 50 aastat - suure esinemissagedusega meestel.
Etioloogia ei ole täielikult kindlaks tehtud. PH esinemissageduse märgatav tõus teatud piirkonnas, teatud aastaajal noores vanuserühmas näitab, et etioloogiline roll võib kuuluda viirustele, näiteks Epstein-Barri viirusele, ja keskkonnateguritele. Eelsoodumusteks võivad olla pärilik eelsoodumus (perekondlikud lümfogranulomatoos ja muud lümfoomid, äge lümfoblastne ja krooniline lümfotsütaarne leukeemia), immuunpuudulikkuse seisundid (omandatud ja kaasasündinud), autoimmuunhaigused.
Kasvaja substraadiks on hiiglaslikud kahe- või kolmetuumalised Berezovski-Reed-Sternbergi rakud ja suured ühetuumalised Hodgkini rakud. Esimesed on diagnostilised - PH diagnoos pannakse paika alles siis, kui need avastatakse. Nende rakkude bioloogiline olemus ei ole täielikult selge, kuigi on teada, et enamikul juhtudel sisaldavad need immunoglobuliinide (IgV) varieeruva piirkonna geenide klonaalseid ümberkorraldusi koos somaatilise hüpermutatsiooni jälgedega, mis vastab
Lümfisõlme sekundaarse folliikuli terminali keskpunkti B-lümfotsüüt. Samal ajal ekspresseerivad Berezovski-Reed-Sternbergi rakud oma pinnal makrofaagide ja folliikulite dendriitrakkude antigeene - CD68 ja S100. Haiguse ainulaadsus seisneb selles, et kasvajarakud ise moodustavad pisikese osa kasvaja massist, mida esindavad peamiselt mittekasvaja polüklonaalsed T-abistajarakud (CD4 rakud), plasmarakud, koe histiotsüüdid ja eosinofiilid. Seda omadust seletatakse Berezovski-Reed-Sternbergi rakkude aktiivse sekretoorse aktiivsusega, mis eritavad arvukalt tsütokiine ja atraktante (tabel 18). Esineb unitsentriliselt, tavaliselt kaela lümfisõlmedes, supraklavikulaarsetes piirkondades, mediastiinumis, kasvaja metastaseerub lümfogeensete ja hematogeensete radade kaudu.
Klassifikatsioon. Lümfogranulomatoos eristab protsessi ranget levikut ühest lümfisõlmede rühmast (tähistatud sümboliga "N") teise. Kõige sagedamini on kahjustatud emakakaela lümfisõlmed. Mitmed, erineva suurusega (mõnikord ulatuvad 10 cm läbimõõduni), ümarad, tihedad, sageli valutud lümfisõlmed moodustavad konglomeraate, mis muudavad oluliselt kaela konfiguratsiooni. Mediastiinumi kahjustus on sageli mahukas - 10 cm või rohkem. Mediastiinumi varju laienemisega rohkem kui 2/3 läbimõõdust rind seda näidatakse haiguse diagnoosimisel massiivse kahjustusena ("mahukas haigus"). Prognoosiliselt on see väga oluline – raske kulg.
Vastavalt PH rahvusvahelisele kliinilisele klassifikatsioonile on:
I etapp: üksiku üksiku lümfisõlme, piirkonna või struktuuri haaratus;
II etapp: kahe või enama lümfipiirkonna haaratus diafragma ühel küljel;
III etapp: lümfisõlmede või piirkondade haaratus mõlemal pool diafragmat;
IV etapp: ekstranodaalsete piirkondade kaasamine, välja arvatud E kategoorias kirjeldatud juhtumid.
Maksa ja luuüdi kahjustusi peetakse alati haiguse IV staadiumiks. Samal ajal on mõistlik eristada maksa ja luuüdi difuusseid, väikese fokaalseid kahjustusi üksikutest. Maksa üksikuid kahjustusi iseloomustab ultraheli pilt fokaalsetest varjudest, maks on suurenenud, palpatsioonil valulik. Üksikute luukahjustuste korral täheldatakse ossalgiat, võib esineda patoloogilisi luumurde. See on prognostiliselt ebasoodne kliiniline olukord.
Põrna lüüasaamine ei ole haruldane, eriti haiguse ägenemiste korral, ja seda tähistab sümbol "S". Põrn on suurenenud, laparoskoopia koos biopsiaga paljastab selles tüüpilised lümfogranuloomid.
Lokaliseeritud ekstranodaalne kahjustus on tähistatud tähega "E". See võib olla interstitsiaalne kopsupõletik koos sümptomitega hingamispuudulikkus(õhupuudus, tsüanoos), lümfogranuloomid kopsudes ja rinnakelmes, eksudatiivne pleuriit (tugev valusündroom, patsiendi keha sundasend, rindkere asümmeetrilised liigutused hingamise ajal).
Sümbolid "A" ja "B" tähistavad vastavalt ühe või mitme loetletud olemasolu või puudumist kliinilised sümptomid: öine tugev higistamine; kehatemperatuuri tõus üle 38 ° C vähemalt 3 päeva järjest ilma nähtavate nakkus- ja põletikulised haigused; kaalulangus üle 10% viimase 6 kuu jooksul.
Samuti peaksite pöörama tähelepanu protsessi bioloogilise aktiivsuse väikestele märkidele - ESR-i suurenemineüle 30 mm/h, tasemed
P2-mikroglobuliin, fibrinogeen ja LDH.
Diagnoos tehakse ainult diagnostiliste Berezovski-Reed-Sternbergi rakkude tuvastamise põhjal.
Tabel 18
Rakkude poolt toodetud tsütokiinide mõju
Berezovski – Reed – Sternberg,
PH kliinilise pildi tunnused
PH variandid histopatoloogilise klassifikatsiooni järgi: lümfotsüütide ülekaal (5%), segarakuline variant (15–30%), lümfotsüütide depletsioon (alla 1%), nodulaarse skleroosiga variant (60–80%), nodulaarne lümfoidne ülekaal ( 4–30%), 5%).
laboratoorsed märgid. AT üldine analüüs Tavaliselt täheldatakse vereaneemiat, neutrofiilset leukotsütoosi, lümfopeeniat, trombotsütoosi, suurenenud ESR-i. Biokeemiline analüüs veri: väga oluline märk on LDH, P2-mikroglobuliini taseme tõus koos maksakahjustusega, võib täheldada transaminaaside taseme tõusu, düsproteineemiat ja albumiini taseme langust. Oluline märk on haptoglobiini taseme tõus. Lümfogranulomatoosi bioloogilise aktiivsuse tunnused on: seerumi haptoglobiini taseme tõus üle 1,5 g/l; tseruloplasmiini sisaldus on üle 185 U/l; fibrinogeeni kontsentratsioon üle 0,4 g/l; erütrotsüütide settimise kiirus üle 30 mm/h; LDH sisaldus on üle 300 U / l.
Kõigil juhtudel tuleb teha luuüdi punktsioon ja kahepoolne trepanobiopsia. Nende elundite kahjustuste tuvastamiseks tehakse rindkere röntgenuuring. Vajalik on ka MRI / CT ja rindkere, kõhu ja vaagna ultraheli (sisemiste lümfisõlmede, elundite seisundi hindamine). Invasiivsed diagnostikameetodid: diagnostiline laparotoomia või laparoskoopia koos maksa ja põrna biopsiaga, mediastinoskoopia või mediastinotoomia koos mediastiinumi kasvaja biopsiaga. Võib teha torakoskoopia ja torakotoomia.
Ravi ja prognoos. Enamikul juhtudel tehakse seda ambulatoorselt, kuid ainult spetsialiseeritud asutuses ning see hõlmab PCT-d ja kiiritusravi. PCT olemuse ja selle mahu määrab haiguse staadium ja halva prognoosi tegurite olemasolu või puudumine. Ebasoodsaid prognostilisi tegureid on palju vanem vanus, mees, massiivsed kahjustused (> 10 cm), diafragma all olevate lümfisõlmede kahjustus, ESR üle 30 mm/h, leukotsütoos koos lümfopeeniaga, aneemia.
Praegu on halva prognoosi määramiseks vastu võetud Hasenclever-Deehli kriteeriumid: albumiin< 4 г/л, гемоглобин 105 г/л, мужской пол, стадия IV, возраст >45 aastat vana, leukotsütoos > 16 tuhat, lümfopeenia< 0,6 тыс., или <8 %.
Raviks IIA–IIIA staadiumis kasutatakse ABVD nr 6 kuuri + kiiritusravi. ABVD: 1. ja 14. päeval manustatakse intravenoosselt adriamütsiini (doksorubitsiini) 25 mg/m 2, bleomütsiini 10 mg/m 2, vinblastiini 6 mg/m 2, dakarbasiini 375 mg/m 2. Bleomütsiinravi alguses on võimalik palavik, iiveldus, oksendamine, hilisematel perioodidel - nahakahjustused, küünefalangide hüperesteesia; kauge kõrvalmõju on kopsufibroos (ravi ajal ja 34 nädalat pärast selle lõppu tehakse rindkere röntgenuuringud, et jälgida kasvaja suuruse dünaamikat ja retsidiivi puudumist).
IIB–IVB staadiumis tehakse 6–8 ABVD kuuri, millele järgneb kiiritusravi vastavalt subradikaalsele (kõigi lümfikollektorite kiiritamine mõlemal pool diafragmat, välja arvatud kubeme-niudepiirkonnad) või radikaalprogrammi (+ kubeme -niudepiirkonnad). Mediastiinumi ultraheli tehakse pärast iga keemiaravi kuuri, rindkere radiograafiat - pärast 2., 4., 6. kursust. Pärast 4. PCT kuuri viiakse läbi "restaging" (kontrolluuring) - patsiendi korduv täielik uuring, et selgitada jääkkasvaja mahtu ja hinnata ravi efektiivsust. Kui on kindlaks tehtud 3 või enam prognostilist tunnust, määratakse ravi vastavalt BEACOPP programmile, sealhulgas: tsüklofosfamiid 650 mg/m 2 1 päev i.v., doksorubitsiin 25 mg/m 2 1 päev i.v., etoposiid 100 mg/m 2 1-3 päeva i.v. / in, natulaan - 100 mg / m 2 1-7 päeva sees, prednisoloon 40 mg / m 2 1-14 päeva sees, vinkristiin 1,4 mg / m 2, kuid mitte rohkem kui 2 mg / 8. päeval, bleomütsiin 10 mg/m 2 IV 8. päeval, uue kuuri algus 22. päeval. Kursused tuleks läbi viia haiglas, kuna neil on märkimisväärne müelotoksilisus. Haiguse prognostiliselt halva kulgemise korral viiakse ravi läbi täiustatud BEACOPP protokolli järgi: tsüklofosfamiid 1250 mg/m 2 1 päev i.v., doksorubitsiin 35 mg/m 2 1 päev i.v., etoposiid 200 mg/m 2 1-3 päeva i.v., natulaan - 100 mg / m 2 1-7 päeva sees, prednisoloon 40 mg / m 2 1. ja 14. päeval, vinkristiin 2 mg / 8. päeval, bleomütsiin 10 mg / m 2 / 8. päeval. Ravikuur on müelotoksiline ja nõuab granulotsüütide või granulotsüütide-makrofaagide kolooniaid stimuleeriva faktori (granotsüüdid, neupogeenid, leukomaks) määramist. Kui tuvastatakse progresseerumine, kasvaja suureneb ravi ajal või puudub dünaamika, viiakse patsient üle intensiivsemale ravile belustiini, etoposiidi, melfalaani, tsütarabiini, plaatina preparaatide, deksametasooni suurte annuste kasutamisega. Pärast polükemoteraapiat tehakse enne kiiritusravi kontrolluuring.
Haiguse refraktaarsete vormide ja varajaste ägenemiste (ühe aasta jooksul pärast kiiritusravi lõppu) alternatiivne ravi on suurtes annustes PCT koos vere tüvirakkude mobiliseerimise ja nende järgneva autotransplantatsiooniga ehk allogeense luuüdi siirdamisega. Hiliste ägenemiste (pärast 1-aastast täielikku remissiooni) ravi viiakse läbi vastavalt skeemile, mille alusel saadi varem täielik remissioon. Monokemoteraapia (harva kasutatav) on palliatiivne ravi nõrgestatud eakatele patsientidele ja patsientidele, kelle puhul PCT võimalused on ammendunud. Kasutage kõiki Hodgkini tõve raviskeemis sisalduvaid vähivastaseid ravimeid (nt vinkristiin, vinblastiin, kloorbutiin, gemtsitabiin).
Keskmine viieaastane elulemus on 60-80%. I või II staadiumiga patsientidel ületab viieaastane retsidiivivaba elulemus 90%. IIIA staadiumiga patsientidel on viieaastane elulemus täieliku remissiooniga ligikaudu 70%. Keemiaravi läbiviimine IIIA, IIIB või IV staadiumiga patsientidel annab remissiooni 80–95% juhtudest, üle 70% patsientidest elab üle 5 aasta.
Pahaloomulised haigused lümfisüsteem või lümfoomid: Hodgkini ja mitte-Hodgkini tõbi avaldub lümfisõlmede suurenemises.
Mitte-Hodgkini lümfoomid ühendavad onkoloogiliste haiguste rühma, mis erinevad nende rakkude struktuurist. Mõjutatud lümfoidkoe proovide järgi saab eristada mitut mitte-Hodgkini lümfoomi. Haigus moodustub lümfisõlmedes ja lümfikoega elundites. Näiteks harknääre (harknääre), põrn, mandlid, peensoole lümfiplaadid.
pahaloomulised rakud
Lümfoom tekib igas vanuses, kuid sagedamini eakatel. Mitte-Hodgkini tõbi, esineb kõige sagedamini pärast 5. eluaastat. Nad kalduvad lahkuma esmase arengu kohast ja hõivama teisi organeid ja kudesid, nagu kesknärvisüsteem, maks ja luuüdi.
Lastel ja noorukitel nimetatakse kõrgetasemelisi kasvajaid "kõrge pahaloomulise kasvajaga NHL-iks", kuna need põhjustavad elundites uusi raskeid haigusi ja võivad lõppeda surmaga. Madala raskusastmega aeglaselt kasvav mitte-Hodgkini lümfoom on täiskasvanutel sagedasem.
Mitte-Hodgkini lümfoomide põhjused
Lümfoomide põhjuseid uurivad arstid siiani. On teada, et mitte-Hodgkini lümfoom saab alguse lümfotsüütide mutatsiooni (pahaloomulise muutuse) hetkest. Samal ajal muutub raku geneetika, kuid selle muutumise põhjus pole välja selgitatud. On teada, et mitte kõik selliste muutustega lapsed ei haigestu.
Arvatakse, et mitte-Hodgkini lümfoomi tekke põhjuseks lastel on mitme riskiteguri kombinatsioon korraga:
- immuunsüsteemi kaasasündinud haigus (Wiskott-Aldrichi või Louis Bari sündroom);
- omandatud immuunpuudulikkus (näiteks HIV-nakkus);
- oma immuunsuse pärssimine elundisiirdamise ajal;
- viirushaigus;
- kiirgus;
- teatud kemikaalid ja ravimid.
Mitte-Hodgkini lümfoomi sümptomid ja nähud
Agressiivse kulgemise ja kasvukiirusest tingitud kõrge pahaloomulise kasvaja mitte-Hodgkini lümfoomi sümptomid väljenduvad märgatava kasvaja või lümfisõlmede suurenemises. Nad ei valuta, vaid paisuvad peas, piirkonnas või. Võimalik, et haigus saab alguse kõhukelmest või rinnus, kus sõlmesid pole võimalik näha ega tunda. Siit levib see mittelümfoidsetesse organitesse: aju, luuüdi, põrna või maksa membraanidesse.
Mitte-Hodgkini lümfoom avaldub:
- kõrge temperatuur;
- kaalukaotus;
- suurenenud higistamine öösel;
- nõrkus ja väsimus;
- kõrge temperatuur;
- söögiisu puudumine;
- valus tunne.
Näitab teatud tüüpi mitte-Hodgkini lümfoomi sümptomeid.
Patsient võib kannatada:
- Kõhuvalu, seedehäired (kõhulahtisus või kõhukinnisus), oksendamine ja isutus. Sümptomid ilmnevad siis, kui lümfisõlmed või elundid on kahjustatud kõhuõõnde(põrn või maks).
- Krooniline köha, õhupuudus koos lümfisõlmede kahjustusega rinnaku õõnes, harknääre ja/või kopsud, hingamisteed.
- Valu liigestes koos luude kahjustusega.
- Peavalud, ähmane nägemine, oksendamine tühja kõhuga, kraniaalnärvide halvatus koos kesknärvisüsteemi kahjustusega.
- Sagedased infektsioonid koos tervete valgete vereliblede taseme langusega (koos aneemiaga).
- Määrake vereliistakute vähesusest tingitud nahaverejooksud (petehhiad).
Tähelepanu! Mitte-Hodgkini lümfoomi sümptomite tugevnemine toimub kahe kuni kolme nädala jooksul või kauem. Iga patsient avaldub erinevalt. Kui täheldatakse ühte või 2-3 sümptomit, võivad need olla nakkuslikud ja lümfoomiga mitteseotud haigused. Diagnoosi selgitamiseks peate võtma ühendust spetsialistiga.
Lümfoomi staadiumid
Lümfoblastilise lümfoomi klassifikatsioon on välja pakutud (St. Jude'i klassifikatsioon).
See sisaldab järgmisi kategooriaid:
- I etapp - ühe kahjustusega: ühe anatoomilise piirkonna ekstranodaalne või sõlmeline. Mediastiinum ja kõhuõõs on välistatud.
- II staadium - ühe ekstranodaalse kahjustusega ja piirkondlike LN-de kaasamisega, seedetrakti primaarne kahjustus (ileotsikaalne piirkond ± mesenteriaalsed LN-d).
- III staadium - sõlmede või lümfoidsete struktuuride kahjustustega mõlemal pool diafragmat ja primaarsed mediastiinumi (sh harknääre) või pleura fookused (III-1). Stage III-2, olenemata muudest kahjustustest, viitab mis tahes ulatuslikele primaarsetele kõhuõõnesisestele mitteopereeritavatele kahjustustele, kõigile primaarsetele paraspinaalsetele või epiduraalsetele kasvajatele.
- IV etapp - kõigi kesknärvisüsteemi ja luuüdi esmaste kahjustustega.
Mycosis fungoides'i jaoks on välja pakutud eraldi klassifikatsioon.
See pakub:
- I etapp, mis näitab muutusi ainult nahas;
- II - staadium koos nahakahjustuste ja reaktiivsete suurenenud lümfisõlmedega;
- III staadium koos LN-dega, millel on suurenenud maht ja kinnitatud kahjustused;
- IV etapp vistseraalsete kahjustustega.
Mitte-Hodgkini lümfoomide vormid
NHL-i vorm sõltub vähirakkude tüübist mikroskoobi all ja molekulaarsetest geneetilistest omadustest.
WHO rahvusvaheline klassifikatsioon eristab kolme suurt NHL-i rühma:
- B-rakulised ja T-rakulised lümfoblastilised lümfoomid (T-LBL, pB-LBL), mis kasvavad B-lümfotsüütide ja T-lümfotsüütide (lümfoblastide) ebaküpsetest prekursorrakkudest. Rühm on 30-35%.
- Küpsed B-rakulised NHL ja küpsed B-ALL (B-ALL), mis kasvavad küpsetest B-lümfotsüütidest. Need NHL-id on üks levinumaid vähivorme - peaaegu 50%.
- Anaplastilised suurrakulised lümfoomid (ALCL), mis moodustavad 10–15% kogu NHL-ist.
Igal NHL-i peamisel vormil on alamliigid, kuid ka muud NHL-i vormid on vähem levinud.
Mitte-Hodgkini lümfoomide klassifikatsioon (WHO, 2008)
Mitte-Hodgkins sisaldab:
B-raku lümfoomid:
- B-raku eellaslümfoomid;
- B-lümfoblastne lümfoom/leukeemia;
- Lümfoomid küpsetest B-rakkudest;
- Krooniline lümfotsüütleukeemia / väikerakk-lümfotsüütiline lümfoom;
- B-rakuline prolümfotsüütleukeemia;
- Lümfoom põrna marginaalse tsooni rakkudest;
- karvrakuline leukeemia;
- Lümfoplasmatsüütiline lümfoom / Waldenströmi makroglobulineemia;
- Raske ahela haigused;
- Plasmarakkude müeloom;
- Luude üksildane plasmatsütoom;
- ekstraosseoosne plasmatsütoom;
- Ekstranodaalne lümfoom limaskestaga seotud lümfoidkudede marginaalse tsooni rakkudest (MALT-lümfoom);
- Sõlme marginaalse tsooni raku lümfoom;
- Follikulaarne mitte-Hodgkini lümfoom;
- Primaarne naha tsentrofollikulaarne lümfoom;
- Lümfoom mantli tsooni rakkudest;
- , mittespetsiifiline;
- B-suurrakuline mitte-Hodgkini lümfoom suure hulga T-rakkude / histiotsüütidega;
- Lümfomatoosne granulomatoos;
- Mitte-Hodgkini lümfoom on difuusne suur B-rakuline lümfoom, mis on seotud kroonilise põletikuga;
- Primaarne naha B-suurrakuline lümfoom;
- Intravaskulaarne B-rakuline lümfoom
- ALK-positiivne suur B-rakuline lümfoom;
- plasmablastiline lümfoom
- Suur B-rakuline lümfoom, mis tuleneb HHV8-ga seotud multitsentrilisest Castlemani haigusest
- EBV positiivne suur B-rakuline lümfoom eakatel
- Primaarne mediastiinumi lümfoom (tüümuse) B-suurrakk;
- Primaarne eksudatiivne lümfoom
- B-rakuline lümfoom, mille morfoloogia on difuusse suure B-rakulise lümfoomi ja klassikalise lümfoomi vahepealne;
- Hodgkini B-rakk, mille morfoloogia on vahepealne Burkitti lümfoomi ja difuusse suure B-rakulise lümfoomi vahel.
T-rakulised ja NK-rakulised lümfoomid:
- Lümfoomid eellas-T-rakkudest;
- T-lümfoblastiline lümfoom/leukeemia;
- Lümfoomid küpsetest T- ja NK-rakkudest;
- rõugete lümfoom;
- Täiskasvanu mitte-Hodgkini T-rakuline lümfoom;
- Ekstranodaalne NK/T-rakuline lümfoom, nasaalne tüüp;
- enteropaatiaga seotud T-rakuline Hodgkini lümfoom;
- Hepatospleeniline T-rakuline lümfoom;
- Subkutaanne pannikulaadne T-rakuline lümfoom;
- seente mükoos / Cesari sündroom;
- Primaarne naha anaplastiline suurrakuline lümfoom;
- Primaarne naha gamma-delta T-rakuline lümfoom;
- Primaarne naha CD4-positiivne väikese ja keskmise suurusega T-rakuline lümfoom;
- Primaarne naha agressiivne epidermotroopne CD8 positiivne tsütotoksiline T-rakuline lümfoom;
- Perifeerne T-rakuline lümfoom, mittespetsiifiline;
- Angioimmunoblastiline T-rakuline lümfoom;
- Anaplastiline suurrakuline lümfoom ALK-positiivne;
- Anaplastiline suurrakuline lümfoom ALK-negatiivne.
Haiguse diagnoosimine ja ravi
Seda tehakse onkoloogilistele haigustele ja verehaigustele spetsialiseerunud kliinikutes. Õiget tüüpi mitte-Hodgkini lümfoomi määramiseks peate tegema palju uuringuid, sealhulgas vereanalüüse, ultraheli, röntgenikiirgust ja varaseima lümfisõlme ekstsisioonibiopsiat. See eemaldatakse täielikult. Eemaldamisel ei tohi seda mehaaniliselt kahjustada. Kui protsessis osalevad teised lümfisõlmede rühmad, ei ole histoloogiliseks uuringuks soovitatav eemaldada kubeme lümfisõlmi.
Kasvajakoe uurimine
Kui esialgsete testide põhjal kahtlustatakse mitte-Hodgkini lümfoomi, sõltub diagnoos ja ravi edaspidi kõikehõlmava lisadiagnoosi tulemustest:
- Operatiivsel viisil võetakse elundi kahjustatud kude või eemaldatakse lümfisõlmed.
- Kui vedelik koguneb õõnsustesse, näiteks kõhuõõnde, uuritakse vedelikku. See võetakse punktsiooniga.
- Luuüdi uurimiseks tehakse luuüdi punktsioon.
Tsütoloogiliste, immunoloogiliste ja geneetiliste analüüside, immunofenotüübi määramise tulemuste kohaselt on patoloogia kinnitust või kinnitamata jätmist, määratakse selle vorm. Immunofenotüpiseerimine viiakse läbi voolutsütomeetria või immunohistokeemiliste meetoditega.
Kui lümfoomi terviklik diagnoos kinnitab NHL-i, määravad spetsialistid raviskeemi koostamiseks kindlaks selle levimuse kogu kehas. Selleks uuritakse ultraheli- ja röntgenipilte, MRI-d ja CT-skaneeringuid. Lisainfot saab PET – positronemissioontomograafiast. Kasvajarakkude olemasolu kesknärvisüsteemis on teada tserebrospinaalvedeliku (CSF) proovist, kasutades lumbaalpunktsiooni. Samal eesmärgil tehakse lastele luuüdi punktsioon.
Uuringud enne ravi
Laste ja täiskasvanute südamefunktsiooni testitakse EKG - elektrokardiogrammi ja EchoCG - ehhokardiogrammi abil. Uurige, kas NHL on mõjutanud mõne organi tööd, ainevahetust või infektsioonide olemasolu.
Esialgsed testitulemused on väga olulised, kui NHL-ravis on muudatusi. Lümfoomi ravi ei ole täielik ilma vereülekandeta. Seetõttu määratakse koheselt patsiendi veregrupp.
Ravirežiimide koostamine
Pärast diagnoosi kinnitamist koostavad arstid iga patsiendi jaoks individuaalse raviskeemi, võttes arvesse teatud prognostilisi ja riskitegureid, mis mõjutavad patsiendi ellujäämise prognoosi.
Olulised prognostilised tegurid ja kriteeriumid, mis mõjutavad ravi kulgu, on järgmised:
- spetsiifiline NHL-i vorm, olenevalt sellest, milline raviprotokoll koostatakse;
- haiguse leviku ulatus kogu kehas, staadium. Sellest sõltub ravi intensiivsus ja kestus.
Mitte-Hodgkini lümfoomi kirurgiline ravi
NHL-i operatsiooni ei tehta sageli, ainult kasvaja osa eemaldamise korral ja koeproovide eemaldamiseks diagnoosi selgitamiseks. Kui on isoleeritud organi kahjustus, näiteks mao või maksa, kasutatakse operatsiooni. Kuid sagedamini eelistatakse kiirgust.
Mitte-Hodgkini lümfoomide ravi riskirühmade kaupa
Mitte-Hodgkini lümfoomide ravi on keeruline.
Mitte-Hodgkini lümfoomide ravijuhiste väljatöötamiseks hinnatakse korduvalt iga individuaalset kliinilist olukorda ning lisatakse kogunenud kogemused loid ja agressiivse NHL-i ravis. Sellest on saanud teraapia lähenemisviiside aluseks. Lümfoomi ravimisel tuleb arvesse võtta keha mürgitust (A või B), ekstranodaalseid kahjustusi (E) ja põrna kahjustusi (S), kasvajakollete mahtu. Olulised erinevused agressiivse keemia- ja kiiritusravi (RT) tulemuste prognoosis III ja IV etapis võrreldes Hodgkini lümfoomi täheldatud tulemustega.
Ravi määramiseks hakati kasvaja III etappi jagama:
- III - 1 - võttes arvesse kahjustusi mõlemal pool diafragmat, mis on piiratud põrna, hilari, tsöliaakia ja portaallümfisõlmede kaasamisega;
- III - 2 - võttes arvesse paraortaalset, niude- või mesenteriaalset LU-d.
Kas lümfoomi vastu on ravi? On teada, et üle 60-aastastel patsientidel kulgeb proliferatiivne haigus esimeses staadiumis suhteliselt hästi ning neljandas staadiumis on neil kõrge laktaatdehüdrogenaasi (LDH) tase veres ja halb elulemuse prognoos. Põhimõtte valimiseks ja ravi agressiivsuse suurendamiseks hakati arvestama kasvaja masside suurima mahuga: perifeersed, sõlmede kahjustused - läbimõõduga 10 cm või rohkem ja laienenud mediastaalsete lümfisõlmede läbimõõdu suhe põiki. rindkere mõõtmed on üle 0,33. Erijuhtudel peetakse suurimat kasvaja suurust 5 cm läbimõõduga ebasoodsaks prognostiliseks märgiks, mis mõjutab sõlmekahjustuste ravi valikut.
Ravi valiku põhimõtet mõjutavad veel 5 ebasoodsat riskitegurit, mida ühendab rahvusvaheline prognostiline indeks - IPI (International Prognostic Index; IPI):
- vanus 60 aastat või rohkem;
- LDH taseme tõus veres (rohkem kui 2 korda normaalsest);
- üldine staatus >1 (2–4) ECOG skaalal;
- III ja IV etapp;
- ekstranodaalsete kahjustuste arv >1.
- 1. rühm - madal tase (0-1 märgi olemasolu);
- rühm 2 - madal keskmine tase (2 märgi olemasolu);
- rühm 3 - kõrge keskmine tase (3 märgi olemasolu);
- 4. rühm - kõrge tase (4-5 märgi olemasolu).
Alla 60-aastaste agressiivse NHL-iga patsientide puhul kasutatakse teistsugust MPI mudelit ja 3 ebasoodsa teguri jaoks on määratletud veel 4 riskikategooriat:
- III ja IV etapp;
- kõrgenenud seerumi LDH kontsentratsioon;
- üldine staatus ECOG skaalal >1 (2–4).
- 1. kategooria – madal risk (0) tegurite puudumisel;
- 2. kategooria – madal keskmine risk ühe riskiteguriga;
- 3. kategooria – kõrge keskmine risk kahe teguriga;
- 4. kategooria - kõrge riskiga kolme teguriga.
Ellujäämine 5 aasta jooksul vastavalt kategooriatele on - 83%, 69%, 46% ja 32%.
Selgitades, mis see on ja kuidas seda ravitakse, usuvad onkoloogid, et MPI riskinäitajad mõjutavad ravi valikut mitte ainult agressiivse NHL-i puhul üldiselt, vaid ka mis tahes NHL-i vormide ja igas kliinilises olukorras.
Indolentse NHL-i algne ravialgoritm on see, et see on mõeldud B-rakuliste lümfoomide jaoks. Sagedamini I ja II astme follikulaarsete kasvajate korral. Kuid 20-30% juhtudest muudetakse need hajusateks suurteks B-rakkudeks. Ja see nõuab teistsugust ravi, mis vastab agressiivsete vormide, sealhulgas III astme follikulaarse NHL-i peamisele ravile.
Mitte-Hodgkini lümfoomide peamine ravimeetod on tsütotoksiliste ravimite kombinatsioonide kasutamine. Ravi viiakse sageli läbi lühikeste kursustena, nendevahelised intervallid on 2-3 nädalat. Kasvaja tundlikkuse määramiseks iga konkreetse keemiaravi tüübi suhtes viiakse läbi vähemalt 2 ravitsüklit. Kui efekti pole, ravitakse lümfoomi teise keemiaravi režiimiga.
Muutke keemiaravi režiimi, kui pärast lümfisõlmede suuruse olulist vähenemist suureneb nende tsüklite vaheline intervall. See näitab kasvaja resistentsust kasutatud tsütostaatikumide kombinatsiooni suhtes.
Kui standardse keemiaravi kauaoodatud efekti ei ilmne, viiakse läbi suurtes annustes keemiaravi ja siirdatakse vereloome tüvirakud. Suurannuselise keemia puhul on ette nähtud suured tsütostaatikumide annused, mis tapavad ka kõige vastupidavamad ja püsivamad lümfoomirakud. See ravi võib aga hävitada vereloomet luuüdis. Seetõttu viiakse tüvirakud vereloomesüsteemi, et taastada hävitatud luuüdi, s.o. allogeensete tüvirakkude siirdamine.
Oluline on teada! Allogeense siirdamise korral võetakse tüvirakud või luuüdi teiselt inimeselt (ühilduvalt doonorilt). See on vähem toksiline ja seda tehakse sagedamini. Autoloogse siirdamise korral võetakse patsiendilt tüvirakud enne suure annusega keemiaravi.
Tsütostaatikume manustatakse vereülekande (infusiooni) teel või süstitakse intravenoosselt. Süsteemse keemiaravi tulemusena jaotub ravim veresoonte kaudu kogu kehas ja võitleb lümfoomirakkudega. Kui kahtlustatakse kesknärvisüsteemi kahjustust või sellele viitavad analüüside tulemused, siis lisaks süsteemsele keemiale süstitakse ravim otse ajuvedelikku, s.o. tehakse intratekaalne keemia.
Ajuvedelikku leidub seljaaju ja aju ümbritsevas ruumis. Aju kaitsev hematoentsefaalbarjäär ei lase tsütostaatikumidel läbi veresoonte ajukudedesse pääseda. Seetõttu on intratekaalne keemia patsientide jaoks oluline.
Ravi efektiivsuse suurendamiseks kasutatakse neid täiendavalt. NHL on süsteemne haigus, mis võib mõjutada kogu keha. Nii et ravi ühega kirurgiline sekkumine võimatu. Operatsiooni kasutatakse ainult diagnostilistel eesmärkidel. Kui leitakse väike kasvaja, eemaldatakse see viivitamatult ja määratakse vähem intensiivne keemiaravi. Täielikult keelduda tsütostaatikumidest ainult kasvajarakkude olemasolul nahal.
bioloogiline ravi
Bioloogia: seerumid, vaktsiinid, valgud asendavad kehas toodetud looduslikke aineid. Vere tüvirakkude tootmist ja kasvu stimuleerivate valgupreparaatide hulka kuuluvad näiteks Filgrastrim. Neid kasutatakse pärast keemiaravi vereloome taastamiseks ja infektsioonide riski vähendamiseks.
Tsütokiine, nagu interferoon-alfa, kasutatakse naha T-rakulise lümfoomi ja karvrakulise leukeemia raviks. Spetsiaalsed valged rakud – monoklonaalsed antikehad seonduvad antigeenidega, mis paiknevad kasvajaraku pinnal. Selle tõttu rakk sureb. Terapeutilised antikehad seonduvad nii veres lahustunud antigeenidega ega ole seotud rakkudega.
Need antigeenid soodustavad kasvaja kasvu. Seejärel kasutatakse teraapias – monoklonaalset antikeha. Bioloogiline ravi suurendab standardse keemiaravi mõju ja pikendab remissiooni. Monoklonaalset ravi nimetatakse immuunteraapiaks. Selle erinevad tüübid aktiveerivad immuunsüsteemi nii palju, et see ise hakkab vähirakke hävitama.
Kasvajavaktsiinid on võimelised esile kutsuma aktiivse immuunvastuse kasvajarakkudele spetsiifiliste valkude vastu. Aktiivselt uuritakse uut CC T-rakkude liiki, mis on laetud kimäärsete antigeeni retseptoritega, mis toimivad antud sihtmärgi vastu.
Radioimmunoteraapia töötab radioaktiivse ainega (radioisotoobiga) seotud monoklonaalsete terapeutiliste antikehadega. Kui monoklonaalsed antikehad seostuvad kasvajarakkudega, surevad nad radioisotoobi mõjul.
Informatiivne video
Toitumine mitte-Hodgkini lümfoomide jaoks
Mitte-Hodgkini lümfoomi toitumine peaks olema järgmine:
- energiakulu osas piisav, et vältida kaalu kuhjumist;
- võimalikult mitmekesine: köögiviljade ja puuviljadega, looma-, linnuliha, kala ja sellest valmistatud toodetega, mereandide ja ürtidega.
- minimaalselt kasutatakse hapukurki ja fermenteeritud toite, lauasoola (mere- või lauasoola), suitsuliha.
Toit peaks olema maitsev, sagedane ja väikestes annustes. Igale patsiendile tuleb läheneda individuaalselt, et mitte välistada hüpernatreemiat (naatriumsoolade liig). See hoiab kehas vedelikku ja moodustab turse. Samal ajal tuleks välja jätta sool ja suitsuliha, et mitte suurendada soola K sisaldust veres.naatrium. Tuleb meeles pidada, et pärast kõhulahtisuse ja oksendamise keemiaravi on naatriumisoolad kehale väga vajalikud.
Alternatiivne ravi
Sisaldab: seente tinktuure, tõmmiseid ja dekokte ning ravimtaimed. Tõhusad koirohu, kukeseene, siiberi, džungari akoniidi, musta tibu leotised.
Seenel on ravivad onkoloogilised omadused: kasetšaga, reishi, korditseps, meitake ja shiitake, brasiilia agaric. Nad takistavad metastaase, normaliseerivad hormonaalset taset, vähendavad keemiaravi kõrvalmõjusid: juuste väljalangemist, valu ja iiveldust.
Kasvaja toksiinide eemaldamiseks segatakse purustatud chaga (kaseseen) mägironija mao tükeldatud juurtega (igaüks 3 supilusikatäit) ja valatakse viinaga (tugev kuupaiste) - 0,5 liitrit. Laske tõmmata 3 nädalat pimedas ja võtke 30-40 tilka 3-6 korda päevas.
Toimeaine Leytinan, reishi seene aminohapped ja polüsahhariidid koos shiitake seene ainetega aktiveerib spetsiifilist immuunsust ja taastab verevalemi.
Kasetõrva (100 g) tuleb 9 korda vees pesta, seejärel hõõruda ammoniaagipulbri (10 g) ja jahuga, kaltsineerida pannil. Vormi tainast 0,5 cm läbimõõduga pallid. Pärast jahuga piserdamist saate seda hoida pappkarbis. Esimesed kolm päeva võtke 1 pall 4 korda 60 minutit enne sööki. Pese maha ravimtaimede keetmisega - 100 ml.
Keetmine: segage hakitud apteegi agrimoni ürti jahubanaaniga (lehed), saialille (õied) - igaüks 50 grammi. Keeda (10 min) 600 ml vees 3 spl. l. kogumine. Lase veidi jahtuda, siis joo sidruni ja meega.
Mitte-Hodgkini lümfoomi ellujäämise prognoos
Paljud patsiendid ja nende sugulased on huvitatud küsimusest, kui kaua elavad ühe või teise tüüpi mitte-Hodgkini lümfoomiga patsiendid? Prognoos sõltub haiguse alamliigist, selle leviku staadiumist ja astmest kogu kehas. Selle haiguse klassifikatsioon sisaldab 50 lümfoomi nimetust.
Vastavalt uuringutele näitab tabel mitte-Hodgkini lümfoomide eeldatavat eluiga pärast 5-aastast ravi.
| 5-AASTNE ELLUJUMINE ERINEVAT TÜÜPI MITTEHODGKINI Lümfoomide (PÄRIS) ELULEJUMINE SÕLTUVALT KAHJULIKEST TEGURISTEST | |||
| NHL VALIK | % PATSIENTIDE KOKKU | 5-AASTA ELULEJA (% PATSIENTIDEst) | |
| 0-1 TEGURID | (SAMAAJALISELT) 4 TEGURIT |
||
| Follikulaarne | 75 | 83 | 12 |
| marginaalne tsoon | 70 | 90 | 52 |
| mantli tsoon | 29 | 58 | 12 |
| Hajus suur B-rakk | 45 | 72 | 22 |
| Perifeerne T-rakk | 26 | 64 | 15 |
| Anaplastiline suur rakk | 77 | 80 | 77 |
Mitte-Hodgkini lümfoomide kliinikut iseloomustavad lümfadenopaatia, ühe või teise organi kahjustuse sümptomid ja palaviku-mürgistuse sündroom. Diagnoos põhineb kliinilistel ja radioloogilistel andmetel ning hemogrammi, lümfisõlmede ja luuüdi biopsia tulemustel. Kasvajavastane ravi hõlmab polükemoteraapia ja kiiritusravi kursusi.
Mitte-Hodgkini lümfoomid
Mitte-Hodgkini lümfoomid (lümfosarkoomid) - erinevad morfoloogiast, kliinilised tunnused ja pahaloomuliste lümfoproliferatiivsete kasvajate kulg, mis erinevad oma omaduste poolest Hodgkini lümfoomist (lümfogranulomatoos). Sõltuvalt primaarse fookuse esinemiskohast jagatakse hemoblastoosid leukeemiateks (luuüdi kasvajakahjustused) ja lümfoomideks (primaarse medullaarse lokaliseerimisega lümfoidkoe kasvajad). Lümfoomi iseloomulike morfoloogiliste tunnuste põhjal jagunevad need omakorda Hodgkini ja mitte-Hodgkini omadeks; viimaste hulka hematoloogias kuuluvad B- ja T-rakulised lümfoomid.
Mitte-Hodgkini lümfoome esineb kõigis vanuserühmades, kuid enam kui pooled lümfosarkoomi juhtudest diagnoositakse üle 60-aastastel inimestel. Keskmine esinemissagedus meeste seas on 2-7 juhtu, naistel - 1-5 juhtu elanikkonna kohta. ajal Viimastel aastatel on tendents mitte-Hodgkini lümfoomide esinemissageduse järkjärgulisele suurenemisele.
Mitte-Hodgkini lümfoomide põhjused
Lümfosarkoomide etioloogia on teadmata ja seetõttu on õigem rääkida riskiteguritest, mis suurendavad mitte-Hodgkini lümfoomi tekke tõenäosust. Selliste ebasoodsate tingimuste hulka kuuluvad viiruslikud kahjustused (HIV, Epstein-Barri viirus, C-hepatiit). Helicobacter pylori infektsioon, mis on seotud peptiline haavand mao, võib põhjustada sama lokaliseerimise lümfoomi arengut.
Mitte-Hodgkini lümfoomide tekkerisk suureneb kaasasündinud ja omandatud immuunpuudulikkuse, rasvumise, vanemas eas, pärast elundisiirdamist. Lümfosarkoomide ja varasema kokkupuute vahel keemiliste kantserogeenidega (benseen, insektitsiidid, herbitsiidid), kiirituse ja vähiravi keemiaraviga on põhjuslik seos. Lümfoom kilpnääre areneb tavaliselt autoimmuunse türeoidiidi taustal.
Mitte-Hodgkini lümfoomide klassifikatsioon
Lümfosarkoome, mis arenevad peamiselt lümfisõlmedes, nimetatakse sõlmedeks, teistes organites (suulae- ja neelumandlid, süljenäärmed, magu, põrn, sooled, aju, kopsud, nahk, kilpnääre jne) – ekstranodaalne. Kasvajakoe struktuuri järgi jagunevad mitte-Hodgkini lümfoomid follikulaarseteks (nodulaarseteks) ja difuusseteks.
Progressioonikiiruse järgi liigitatakse mitte-Hodgkini lümfoomid loiduks (aeglase ja suhteliselt soodsa kulgemisega), agressiivseteks ja üliagressiivseteks (kiire arengu ja üldistamisega). Ravimata jätmise korral elavad loidsete lümfoomidega patsiendid keskmiselt 7-10 aastat, agressiivsete - mitmest kuust kuni 1,5-2 aastani.
Kaasaegses klassifikatsioonis on üle 30 mitmesugused mitte-Hodgkini lümfoomid. Enamik kasvajaid (85%) pärinevad B-lümfotsüütidest (B-raku lümfoomid), ülejäänud T-lümfotsüütidest (T-raku lümfoomid). Nendes rühmades on erinevad mitte-Hodgkini lümfoomide alatüübid.
B-rakuliste lümfoomide rühma kuuluvad:
- difuusne suur B-rakuline lümfoom on kõige levinum mitte-Hodgkini lümfoomi histoloogiline tüüp (31%). Seda iseloomustab agressiivne kasv, hoolimata sellest, peaaegu pooltel juhtudel saab seda täielikult ravida.
- follikulaarne lümfoom - selle esinemissagedus on 22% mitte-Hodgkini lümfoomide arvust. Kursus on loid, kuid võimalik on muutumine agressiivseks hajutatud lümfoomiks. 5-aastase elulemuse prognoos on 60-70%.
- väikerakk-lümfotsüütiline lümfoom ja krooniline lümfotsüütleukeemia on sarnased mitte-Hodgkini lümfoomide tüübid, mis moodustavad 7% nende arvust. Kursus on aeglane, kuid halvasti ravitav. Prognoos on varieeruv: mõnel juhul areneb lümfosarkoom välja 10 aasta jooksul, mõnel juhul muutub see teatud staadiumis kiiresti kasvavaks lümfoomiks.
- lümfoom mantlirakkudest - mitte-Hodgkini lümfoomide struktuuris on 6%. Ainult 20% patsientidest ületab viieaastase elulemuse piiri.
- Marginaalse tsooni rakkudest pärinevad B-rakulised lümfoomid jagunevad ekstranodaalseteks (võivad areneda maos, kilpnäärmes, süljes, piimanäärmetes), sõlmelisteks (areneb lümfisõlmedes), põrnaks (lokaliseerumisega põrnas). Erineb aeglase kohaliku kasvu poolest; varases staadiumis annavad ravile hästi järele.
- B-rakuline mediastiinumi lümfoom – esineb harva (2% juhtudest), kuid erinevalt teist tüüpi mitte-Hodgkini lümfoomist mõjutab see peamiselt noori naisi. Seoses kiire kasv põhjustab mediastiinumi organite kokkusurumist; paraneb 50% juhtudest.
- Waldenströmi makroglobulineemia (lümfoplasmotsüütiline lümfoom) diagnoositakse 1% mitte-Hodgkini lümfoomiga patsientidest. Seda iseloomustab IgM hüperproduktsioon kasvajarakkude poolt, mis põhjustab vere viskoossuse suurenemist, veresoonte tromboosi ja kapillaaride rebenemist. Sellel võib olla nii suhteliselt healoomuline (elulemus kuni 20 aastat) kui ka mööduv areng (patsiendi surmaga 1-2 aasta jooksul).
- Karvrakuline leukeemia on väga haruldane mitte-Hodgkini lümfoomi tüüp, mis esineb vanematel inimestel. Kasvaja kulg on aeglane, ei vaja alati ravi.
- Burkitti lümfoom – see moodustab umbes 2% mitte-Hodgkini lümfoomidest. 90% juhtudest mõjutab kasvaja alla 30-aastaseid noori mehi. Burkitti lümfoomi kasv on agressiivne; intensiivne keemiaravi võimaldab saavutada poolte patsientide paranemise.
- kesknärvisüsteemi lümfoom – kesknärvisüsteemi esmane kahjustus võib mõjutada pea või selgroog. Seostub sagedamini HIV-nakkusega. Viie aasta elulemus on 30%.
T-rakulise päritoluga mitte-Hodgkini lümfoomid on esindatud:
- T-lümfoblastiline lümfoom või eellasleukeemia - esineb sagedusega 2%. Need erinevad üksteisest luuüdi blastrakkude arvu poolest: 25% - nagu leukeemia. Diagnoositud peamiselt noortel inimestel keskmine vanus haige - 25 aastat. Halvim prognoos on T-lümfoblastne leukeemia, mille paranemise määr ei ületa 20%.
- perifeersed T-rakulised lümfoomid, sealhulgas naha lümfoom (Cesari sündroom, mycosis fungoides), angioimmunoblastne lümfoom, ekstranodaalne looduslik tapja-lümfoom, enteropaatiaga lümfoom, subkutaanne pannikuliit-sarnane lümfoom, anaplastiline suurrakuline lümfoom. Enamiku T-rakuliste mitte-Hodgkini lümfoomide kulg on kiire ja tulemus on halb.
Mitte-Hodgkini lümfoomide sümptomid
Mitte-Hodgkini lümfoomide kliiniliste ilmingute variandid varieeruvad suuresti sõltuvalt primaarse fookuse lokaliseerimisest, kasvajaprotsessi levimusest, kasvaja histoloogilisest tüübist jne. Kõik lümfosarkoomide ilmingud jagunevad kolmeks sündroomiks: lümfadenopaatia, palavik ja mürgistus. , ekstranodaalsed kahjustused.
Enamikul juhtudel on mitte-Hodgkini lümfoomi esimene märk perifeersete lümfisõlmede suurenemine. Algul jäävad nad elastseks ja liikuvaks, hiljem sulanduvad suurteks konglomeraatideks. Samal ajal võivad mõjutada ühe või mitme piirkonna lümfisõlmed. Fistuloossete käikude moodustumisel on vaja välistada aktinomükoos ja tuberkuloos. Mediastiinsete lümfisõlmede kahjustusega areneb söögitoru ja hingetoru kokkusurumine, SVC kokkusurumise sündroom. Suurenenud intraabdominaalsed ja retroperitoneaalsed lümfisõlmed võivad põhjustada soolesulgust, lümfostaasi keha alumises pooles, obstruktiivset kollatõbe ja kusejuha kokkusurumist.
Sellised mitte-Hodgkini lümfoomide mittespetsiifilised sümptomid, nagu palavik ilma ilmsete põhjusteta, öine higistamine, kehakaalu langus, asteenia, viitavad enamikul juhtudel haiguse üldistatud olemusele. Ekstranodaalsete kahjustuste hulgas domineerivad Pirogov-Waldeyeri ringi, seedetrakti ja aju mitte-Hodgkini lümfoomid; harvemini on kahjustatud piimanääre, luud, kopsuparenhüüm ja muud organid.
Nasofarüngeaalne lümfoom on endoskoopilisel uurimisel kahvaturoosa kasvaja, millel on mugulakujulised kontuurid. Sageli tärkavad ülalõua- ja ninakõrvalurged, orbiit, põhjustades nasaalse hingamise raskusi, rinofooniat, kuulmislangust, eksoftalmust.
Primaarsel munandi mitte-Hodgkini lümfoomil võib olla sile või konarlik pind, elastne või kivine kõvadus. Mõnel juhul tekib munandikoti turse, naha haavandid kasvaja kohal, kubeme-niude lümfisõlmede suurenemine. Munandite lümfoomidel on eelsoodumus varaseks levikuks koos teise munandi, kesknärvisüsteemi jne kahjustusega.
Rindade lümfoom palpatsioonil on määratletud kui selge kasvaja sõlm või difuusne rinna tihendus; nibu tagasitõmbumine on ebaloomulik. Kui kõht on kahjustatud, sarnaneb kliiniline pilt maovähiga, millega kaasneb valu, iiveldus, isutus ja kaalulangus. Kõhu mitte-Hodgkini lümfoomid võivad avalduda osalise või täieliku soolesulgusena, peritoniidina, malabsorptsiooni sündroomina, kõhuvalu, astsiidina.
Naha lümfoom avaldub sügeluse, sõlmede ja punakaslilla kõvendusena. Kesknärvisüsteemi esmane kahjustus on tüüpilisem AIDS-iga patsientidele - selle lokaliseerimise lümfoomi kulgemisega kaasnevad fokaalsed või meningeaalsed sümptomid.
Mitte-Hodgkini lümfoomide diagnoosimine
Mitte-Hodgkini lümfoomide diagnoosimise küsimused on onkohematoloogide pädevuses. Lümfosarkoomi kliinilised kriteeriumid on ühe või mitme lümfisõlmede rühma suurenemine, mürgistus, ekstranodaalsed kahjustused.
Kavandatud diagnoosi kinnitamiseks on vaja uurida kasvaja rakulist substraati. Sel eesmärgil tehakse diagnostilisi operatsioone: lümfisõlmede punktsioon või ekstsisioonbiopsia, laparoskoopia, torakoskoopia, luuüdi punktsioon koos järgnevate immunohistokeemiliste, tsütoloogiliste, tsütogeneetiliste ja muude diagnostilise materjali uuringutega. Lisaks diagnoosimisele on see oluline ravitaktika valikul ja mitte-Hodgkini lümfoomide prognoosi määramisel.
On vaja eristada mitte-Hodgkini lümfoome lümfogranulomatoosiga, metastaatilise vähiga, tulareemiaga esineva lümfadeniidiga, brutselloosiga, tuberkuloosiga, toksoplasmoosiga, süüfilisega, nakkuslik mononukleoos, gripp, SLE jne.
Mitte-Hodgkini lümfoomide ravi
Mitte-Hodgkini lümfoomide ravivõimalused hõlmavad kirurgiat, kiiritusravi ja keemiaravi; nende valiku määrab kasvaja morfoloogiline tüüp, levimus, lokaliseerimine, patsiendi ohutus ja vanus.
Kirurgilist sekkumist kasutatakse tavaliselt organi, tavaliselt seedetrakti, isoleeritud kahjustuse korral. Kiiritusravi kui mitte-Hodgkini lümfoomide monoteraapiat kasutatakse ainult lokaliseeritud vormide ja madala astme kasvajate korral. Lisaks saab kiiritust kasutada ka palliatiivse meetodina, kui keemiaravi ei ole võimalik.
Kõige sagedamini algab mitte-Hodgkini lümfoomide ravi polükemoteraapia kuuriga. See meetod võib olla sõltumatu või kombineeritud kiiritusraviga. Kombineeritud kemoradioteraapia võimaldab saavutada pikemaid remissioone. Ravitsüklitesse on võimalik lisada hormoonravi. Ravi jätkub kuni täieliku remissiooni saavutamiseni, pärast mida on vaja veel 2-3 tugevdavat kuuri.
Alternatiivsed meetodid hõlmavad immunoteraapiat interferooniga, monoklonaalseid antikehi, autoloogse või allogeense luuüdi ja perifeersete tüvirakkude siirdamist.
Mitte-Hodgkini lümfoomide prognoos on erinev, sõltuvalt peamiselt kasvaja histoloogilisest tüübist ja avastamise staadiumist. Lokaalselt arenenud vormide puhul on pikaajaline elulemus keskmiselt 50-60%, üldistatud vormide puhul vaid 10-15%.
Mitte-Hodgkini lümfoomid - ravi Moskvas
Haiguste kataloog
Verehaigused
Viimased uudised
- © 2018 "Ilu ja meditsiin"
on ainult informatiivsel eesmärgil
ja see ei asenda kvalifitseeritud arstiabi.
Newmed
ravi Iisraelis
Miks patsiendid SRÜ riikidest
kas valida NewMed Center?
"NewMed Center Israel" - eelised
- suhtleme vene keeles
- nõustame tasuta
- valime välja parima kitsa profiiliga spetsialisti
- broneeri piletid
- broneerida majutus
- koostada kutse
- teostame ülekande
- töötame ilma ettemaksuta
- maksame kliinikute kassasse kliinikute hindadega
- korraldame ekskursioone
Hodgkini lümfoomi ja mitte-Hodgkini lümfoomi ravi Iisraelis
Lümfoomi sõeluuringuprogramm Iisraelis. Diagnostiliste protseduuride hinnad
* - diagnostika hinnad võivad Iisraeli tervishoiuministeeriumi pideva regulatsiooni tõttu veidi erineda
Hodgkini lümfoomi ravi Iisraelis
Seda haigust nimetatakse ka lümfogranulomatoosiks. See haigus on pahaloomuline ja mõjutab meie keha lümfisüsteemi. Haigus võib kulgeda erineva agressiivsusega, esineb üsna sageli ja nõuab kohustuslikku ravi. Kui me räägime üldiselt lümfisüsteemi vähist, siis võib selle jagada kahte lümfoomi rühma - Hodgkini ja mitte-Hodgkini. Esimesel juhul võib haigus avalduda igas vanuses inimestel ja meestel on see iseloomulik sagedamini.
Hodgkini lümfoomi ravi Iisraelis algab esmase uuringuga, mis aitab tuvastada mediastiinumi ja kaela lümfisõlmede suurenemist. Praeguses etapis tervise halvenemise kohta kaebusi ei ole. Ilmsete kahjustusnähtude korral on haiguse staadiumi täpne määramine võimalik ainult täiendava uurimisega. Mitte-Hodgkini lümfoom (NHL) on tavalisem kui Hodgkini tõbi. Seda tüüpi lümfoomi iseloomustab protsessi kiire levik kogu kehas ja paljudel patsientidel väljendub see ühe või mitme lümfisõlmede rühma suurenemises. See haigus võib sageli jäljendada muid haigusi. Sellist jäljendamist seostatakse NHL-i asukohaga. Mõnel patsiendil on luu- ja nahakahjustused haiguse algfaasis, kolmandikul patsientidest võib tekkida aneemia.
Meie keha on mitmesuguste kudede kogum, mis koosneb väikestest rakkudest. Igal vähil on kahjustav omadus, just sellel rakutasandil. Meie rakud on oma olemuselt erinevad välimus ja selle spetsiifilisuse (täidetavate funktsioonide) tõttu. Kuid üks protsess, mis neil kõigil on, on peaaegu identne – see on nende paljunemine. Rakkude normaalne jagunemine on reguleeritud ja kontrollitud protsess, kuid kui see protsess on häiritud, muutub jagunemine kaootiliseks. Selle tulemuseks on uute rakkude moodustumine ilma vajaduseta.
Lümfisõlmedes, mis on osa inimese lümfisüsteemist, kogunevad pahaloomulised lümfirakud. Nad võivad tungida läbi lümfivoolu, levida üle kogu keha, sattuda teistesse lümfisõlmedesse või sattuda veresoontesse. Perifeerne veri on võimeline toimetama lümfoomirakke meie keha erinevatesse organitesse, kuid enamikul juhtudel on mõjutatud piiratud rühm lokaalseid lümfisõlmesid. Vähirakkude struktuur erineb tervetest rakkudest, sellest järeldub, et diagnoosi saab määrata ainult kahjustatud lümfisõlme bioloogilist materjali analüüsides. Seda analüüsi nimetatakse biopsiaks.
Hodgkini lümfoomi ravi Iisraelis on viimastel aastatel märgatavalt edenenud. See on juba kvalitatiivselt uus tase täiustatud meetoditega, mille tõhusus on oluliselt suurenenud. Tuleb märkida, et me räägime juhtumitest, mille puhul pahaloomulised rakudületada piirkondlike lümfisõlmede piire ja levida teistesse meie keha organitesse. Samuti suureneb Iisraelis Hodgkini lümfoomi ravile tulnud patsientide arv, kellel õnnestus sellest haigusest täielikult vabaneda, samuti nende patsientide arv, kellel on stabiilne remissioon (haiguse taandumine mitmeks aastaks).
lümfisüsteem
Organismi lümfisüsteemil on oluline roll selle kaitsmisel erinevate infektsioonide eest. Inimese lümfisüsteem sisaldab lümfopoeesi organeid, mis on ühendatud õhukeste veresoonte võrguga. Nende elundite hulka kuuluvad põrn, harknääre ja luuüdi. Lümfisõlmed paiknevad erinevates kehaosades ja on hästi palpeeritavad (kael, kubemes, kaenlaalus). Kuid nende jaotus kogu kehas on ebaühtlane. Näiteks kaenlaaluses on nende arv 20–50 sõlme ja mujal on neid väga vähe.
Kindlasti on igaüks meist kogenud nohuga kurguvalu. Seega saate sel juhul iseseisvalt kontrollida lümfisõlmede suurenemist. Nende suurenemine on märk meie immuunsüsteemi aktiivsest tööst, mis võitleb infektsioonidega. Lümfisõlmede töö tagab lümfi – lümfotsüüte sisaldava värvitu vedeliku – läbiminek. Need rakud on teatud tüüpi leukotsüüdid (valged verelibled). Seega on nad meie keha kaitsmisel oluline näitaja mitmesugused infektsioonid ja haigused. Lümfotsüüte toodab luuüdi ja need on ebaküpsed rakud (tüvirakud). Need rakud jagunevad kahte rühma:
Esimene rühm rakke küpseb luuüdis, aga ka meie lümfisüsteemi perifeersetes organites ning teine rühm harknääres (nn harknääre). See asub rinnaku tagaosas ja on sisesekretsiooninääre.
Hodgkini ja mitte-Hodgkini lümfoomi erinevus
Biopsia alusel toimub diferentsiaaldiagnostika, mis taandab diagnoosi ühele võimalusele. Hodgkini lümfoomi iseloomustab asjaolu, et Reed-Sternbergi rakud (spetsiifilised patoloogilised rakud) sisalduvad lümfisõlmede kudedes. Nende puudumine räägib teist tüüpi lümfoomidest, mis kuuluvad teise rühma - mitte-Hodgkini lümfoomi. Spetsiifiliste rakkude olemasolu peetakse Hodgkini lümfoomi peamiseks kliiniliseks tunnuseks ja see on väga oluline, kuna mõlema lümfoomi ravis on põhimõtteline erinevus.
Haiguse diagnoosimine ja ravi
Viimastel aastatel on mitte-Hodgkini lümfoomi ja Hodgkini tõve ravi Iisraelis saavutanud kõrgeid tulemusi, mis võimaldas tõsta selle ravi uuele tasemele. Nüüd saab seda haigust täielikult ravida ja kordumine on minimeeritud. Iisraeli kliinikute sõnul ei ole mitte-Hodgkini lümfoomi diagnoos lause. Kaasaegsed meetodid ravimeetodid ja uued ravimid ei aita mitte ainult säilitada ja pikendada patsientide eluiga, vaid parandavad selle kvaliteeti ja seda üsna märgatavalt. Ja kuidas saada usaldusväärset teavet mitte-Hodgkini lümfoomi ja Hodgkini tõve ravile jõudmise kohta Iisraeli, eriti ilma kliinikut külastamata? Täida lehel olev taotlusvorm ja saad vastused kõikidele oma küsimustele.
B- ja T-rakulised lümfoomid
Need kaks lümfoomide rühma klassifitseeritakse mitte-Hodgkini lümfoomideks. Meie immuunsüsteemis on peamised rakud B- ja T-lümfotsüüdid. Sellest võime juba järeldada, et kõigil mitte-Hodgkini lümfoomidel on üks ühine joon – nad kõik arenevad ja "kasvavad" meie immuunsüsteemi rakkudest ning mõjutavad negatiivselt lümfopoeesi organeid. Need rakud on võimelised intensiivselt liikuma ning võivad diagnoosimise ja ravi ajal juba levida kogu kehasse. Enamik mitte-Hodgkini lümfoome diagnoositakse hilisemates staadiumides, kuid Iisraeli onkoloogide sõnul on see normaalne. See haigus on teiste kasvajatega võrreldes hästi ravitav. Meie onkoloogiakliinikutel on juba palju näiteid mitte-Hodgkini lümfoomi ravist Iisraelis, kui lümfoom kadus täielikult, jätmata märki kordumise kohta.
Mitte-Hodgkini lümfoomi ravi Iisraelis
Mitte-Hodgkini lümfoomid erinevad mitte ainult haiguse vormide mitmekesisusest, vaid ka nende arengu ajast ja käigu iseloomust. On tuntud vorme, mis ei nõua meditsiini sekkumist pikkadeks aastateks, kuid on ka neid, millel on agressiivse kulgemise vorm. Kui mitte-Hodgkini lümfoome iseloomustatakse üldiselt, võib need jagada kolme klassi:
Üsna sageli muudab selle haiguse keeruliseks asjaolu, et veres ja luuüdis on kahjustusi. Seda lümfoomi vormi nimetatakse leukeemiaks. See hakkab moodustuma luuüdis ja seda nimetatakse vedelaks kasvajaks. Kuid aju ja verd võivad mõjutada ka mittevedelkoe lümfoomid, mis arenevad siseorganites ja lümfisõlmedes. Kui teil on lümfoom, sõltub edukas ravi järgmistest teguritest:
- Lavalt;
- Vaate pealt;
- Voolu iseärasustest;
- Alates suurusest;
- Tervislikust seisundist jne.
Iisraeli onkoloogid viivad haiguse esmast ravi läbi kahes suunas - keemiaravi ja kiiritusravi. Esimesel juhul teostavad Iisraeli onkoloogilised kliinikud lisaks keemiaravile ka ravi monoklonaalsete antikehadega. Need on uue klassi ravimid, mille väljatöötamine võimaldas meil astuda selle haiguse vastase võitluse uude, progressiivsemasse etappi.
Siinkohal tasub mainida sellist ravimit nagu rituksimab, mis annab suure tõenäosuse täielikuks paranemiseks isegi mitte-Hodgkini lümfoomi agressiivse vormi korral. Kiiritusravist rääkides viiakse selline protseduur läbi Iisraelis spetsiaalsetes kompleksides, mis on varustatud uusimatega uuenduslik tehnoloogia. Kui tegemist on progresseeruva haigusega või selle kordumisega, võib lisada mõlemad ravimeetodid bioloogiline teraapia või luuüdi siirdamine.
Lümfoomi ravi - maksumuse saate teada ja programmi saate täites lehel avalduse.
Hodgkini lümfoom ja mitte-Hodgkini lümfoom GNM-is
On ainult üks ühine joon: mõlemad lümfoomitüübid tähistavad taastumisfaasi pärast olemasolevat bioloogilist šokki (BDS). enese devalveerimise konflikt. Vastasel juhul on neil täiesti erinev sisu konfliktide põhjustest, sealhulgas erinevad releed ajus, mis käivitavad vastava Bioloogilised eriprogrammid(SBP).
Traditsioonilises meditsiinis nimetatakse neid "lümfisõlmede vähiks". Sümptomaatilisel patsiendil tehakse diagnoos alati taastumisfaasis (vastava SBP PCL-i faasis) või kaebusteta patsientidel mõnikord puhtjuhuslikult pärast paranemist.
nn Hodgkini tõbi kuulub keskmise idukihi (mesodermi) kudedesse ja sisse Saksa uus meditsiin tekib PCL-i faasis raku mitoosi tõttu, mis põhjustab lümfisõlmede turset, st siis, kui konflikt on juba lahendatud. Seda tüüpi lümfoomi puhul on alati olemas eelnev konflikt suhteliselt kerge eneseamortisatsioon.
Või arvab patsient, et ta ei saa eksamit sooritada. "Ma ei saa hakkama, ma pole seda ainet täielikult õppinud." Siin mõjutab kubemepiirkond, kus konflikti aktiivses faasis (SA-faas) toimub osteolüüs, kuid mida tavaliselt ei tunnetata. Alles siis, kui eksam on veel võimalik sooritada (konfliktide lahendamine – konfliktolüüs), saab inimene kubeme lümfisõlmede paranemise – ja alles sel hetkel pöörab ta füüsiliste aistingute tõttu sellele tähelepanu ning tal diagnoositakse Hodgkini tõbi.
Mõjutatud on skeleti samale tsoonile vastavad lümfisõlmed, iga lümfisõlm kuulub vastava külje luusse. Eneseamortisatsioon on veidi väiksem kui luu enda mõjul. SA faasi ajal - nekroos ("õõnsused"). Lümfisõlmed reageerivad samamoodi nagu luud. Mikroskoobi all näeb selline nekrootiline lümfisõlm välja nagu "Šveitsi juust".
Pärast konflikti lahendamist (PCL-faas) - nekrootilise koe taastamine kahjustatud lümfisõlme tursega (positiivne taastumise märk!); lümfisoonte nekrootiliste piirkondade taastamine, lümfisoonte laienemine, lümfi väljavoolu takistamine ("sündroomiga" suureneb turse).
nn Hodgkini tõbi= Suurenenud lümfisõlmed on raku mitoosi tagajärg. See rakkude proliferatsioon erineb "healoomulisest" lümfisõlmest kuivendatud abstsessi piirkonnas, mis on ülepinge tõttu kasvanud, antud juhul raku mitoos puudu. Kell "sündroom"- suurenenud turse. Bioloogiline tähendus on lümfisoonte tugevdamine ja lümfisõlm, mis muutub senisest suuremaks (bioloogilisest aspektist on suur lümfisõlm parem kui väike).
nn mitte-Hodgkini lümfoom on SBP taastav osa, mida juhitakse välimisest germinaalsest kihist (ektoderm, relee ajukoores) ja on märk taastumisfaasist pärast "rinde hirmu/rünnaku konflikti", "vähihirmu" konflikti või "impotentsuse" konfliktid ("peab midagi kiiresti tegema"). midagi olulist") - ja sõltub lateraalsusest (vasak- või paremakäelisus), hormonaalsest seisundist, ajukoore tähtkujudest jne. - on sageli selle tagajärg, et inimene satub ühte kõige kohutavamasse nõiaringi.
Hirm "frontaalrünnak"- see on hirm millegi ees, mis "tuleb meile vastu" ja mida me ei saa vältida. On ka tagasitee - "taganemise võimatus, põgenemistee blokeerimine", lisa "hirm kaelas" ja ajukoore fronto-kuklakonstellatsioon (nn skisofreenia tähtkuju).
Frontaalne hirm on inimestel ja loomadel väga reaalne, see on hirm reaalse ohu ees, mis tuleneb inimeste või loomade ründamisest jne. Vaid inimesel võib see hirm olla ka kujuteldav, mis toob kaasa hirmu millegi ees, mis ei tundu meile looduses mitte vähem ohtlik kui reaalne oht metsloomale: näiteks ütleb arst patsiendile: „Meil on kahtlus, et teil on vähk" või "teil on vähk". Kuna enamikule inimestele (ja enamikule arstidele) esitletakse vähki endiselt kui midagi vältimatut ja "lõpuni viivat", defineeritakse ka kui "saatuslikku sündmust", tähendab see tajutav oht sattumist "frontaalse hirmu" või "rinderünnaku" konflikti. " , kuigi tegelikkuses samas vähis ohtu praktiliselt pole, kui inimene teab selle tekkepõhjusi ja teab, mida teha. Patsiendid ja arstid, kellel on teadmisi Saksa uuest meditsiinist, isegi vähidiagnoosiga, ei kannata sellist "vähihirmu".
„Finaalse ohu” või „vähihirmuga” oleme evolutsiooniliselt viidud arhailisse aega, mil meie esivanemad elasid vees. Nende kalataoliste olendite suurim katastroof oli see, et nende lõpused olid millegi võõraga ummistunud või paiskusid nad veest välja (näiteks suure lainega) ja nende lõpused jäid kokku nii, et nad ei saanud hingata. Just see ürgne hirm, et oleme "õhust väljas", annab meile selle "frontaalse ärevuse" ja konfliktid, mis on sisult sarnased "vähihirmuga". Nagu üks patsient ütles: "Mul on tunne, et mu kurk on kinni." Juhul, kui inimene saab sellise “vähidiagnoosikonflikti”, ilmutab ta koheselt konfliktitegevuse märke, nimelt: jäised (külmad) käed, isutus, unetus, segasus mõtlemises - hirmust piiratud patsient ei suuda. selgeks mõelda jne. Las väike, kuid lokaalne pitsitustunne või pigistustunne on tunda ka kaelal.
Konflikti aktiivses faasis tekivad lõpusevahe iidsete (arhailiste) neelujuhade (soonte) haavandid. (fissura branchialis) nende laiendamiseks, et parandada vee (hapniku) voolu ja hingamist. Need iidsed, tänapäevani säilinud neelukanalid on vooderdatud lameepiteeliga ja haavandudes annavad kaelas mõõdukat valu.
Pärast konflikti lahendamist (PCL-faas) tekib neelukanalite sisemuses haavandilise piirkonna ümber turse. Selle tulemusena tekivad kanalitesse seroosse vedelikuga täidetud tsüstid. Mediastiinumis võivad need tsüstid kasvada diafragmasse. Varem diagnoositi need tsüstid, mida tavameditsiin tunneb ära alles taastumisfaasis, kui "tsentrotsüütiline-tsentroblastiline mitte-Hodgkini lümfoom (lümfosarkoom)".
Need tsüstid võivad tunduda ja tunduda nagu "pallid" naha all mõlemal pool kaela ja kõrvade taga, alla kaela alla õlani ja edasi supraklavikulaarsesse lohku ja kaugemale. Sees võivad need ulatuda diafragma ja sisaldada ka paksu vedelikku.
Mediastiinumi tsüstid kasvavad märkamatult ja kui konflikt ei lahene täielikult, vaid sageli "lülitub" aktiivsest faasist taastumisfaasi ja vastupidi (CA-faas / PCL-faas), siis tsüstid tugevnevad ja kasvavad rohkem, moodustades sees sidekoe (armkude), mida tavameditsiinis diagnoositakse siis kui "väikerakk-kopsuvähk".
"Metastaaside paanika" tagajärjel kannatavad nad taas "vähihirmu" konflikti all ja selle tõttu taastumisfaas peatub, inimene langeb uuesti konflikti aktiivsesse faasi, mille suurus väheneb. tsüstid (haavandiprotsessi kordumine). Või vähipaanika korral tehakse inimesele keemia- ja/või kiiritusravi, mis samuti paneb keha stressiseisundisse (bioloogiline – seda tajutakse rünnakuna kehale), mis samuti annab vähenenud tsüstide suurus, mida tajutakse kui "kemoteraapia edu", see "teraapia" aga peatab alles eelmise taastumise faasi pärast eelmise konflikti lahendamist. Mõlemal juhul patsient kohe satub nõiaringi. Konflikti kordumisel jäetakse taas ravi ära, väheneb lõpusekaare tsüstide suurus, haavandid lõpusekaare kanalites laienevad veelgi ning suureneb ka "konflikti mass".
Konfliktide massi suurenemine tähendab, et kui patsient uuesti rahustada, on korduva paranemise märgina uuesti esile kerkivad vedelikutsüstid varasemast katkenud paranemise ja uuest paanikast tuleneva konflikti massi tõttu veelgi suuremad. . Loomulikult süveneb paratamatult ka epileptoidne kriis, kui see oleks olnud esimesel korral, kui esialgne "vähihirmu" konflikt oleks ilma edasise tagasilanguseta lõpuni lahendatud.
Kui inimene teab põhimõtteid Saksa uus meditsiin, siis isegi üsna suurte tsüstide olemasolul ei satu ta "vähihirmu konfliktist" paanikasse ja taastumisfaas möödub täielikult, mis tahes tugevusega epileptoidse kriisiga (inimest hoiatatakse selle eest ja ta teab võimalikest sümptomitest). selles taastumise etapis). Sageli, eriti kui kaelas (või mediastiinumis) paiknevad üsna suured tsüstid, võib inimesel tekkida tunne, et hingetoru kokkusurumise tõttu saab ta mehaaniliselt vähem õhku. Reaalset lämbumisohtu aga pole, sest tsüst ei suuda hingetoru täielikult sulgeda.
Epileptoidse kriisi hetkel võib aga subjektiivselt tunnetatav arhailine loomade hirm lämbumise ees olla väga tugev ja võib hirmunud inimese taas paanikasse ajada. Kuid õnneks juhtub see ainult äärmuslikel juhtudel, kui tegemist on väga suurte tsüstidega. Tutvustage inimest (patsienti) põhitõdedega Saksa uus meditsiin ja konkreetselt oma juhtumi käigu põhimõtetega suudab ta päästa paanikast õudusest ja see on iga tõelise arsti kõige olulisem ülesanne.
Sellistele patsientidele rahustavate ravimite andmine on mõttetu ja enamasti lihtsalt märk teadmatusest, sest pärast epileptoidset kriisi satub patsient teise vagotoonilise faasi (PCL-B-faas) ja suurenenud sedatsioon võib olla surmav. Keemiline sedatsioon on mürgistuse liik, mis ei saa kunagi olla inimesele rahustav julgustus ega asendada sobivat meditsiinilist tegevust. Alles pärast selle teise vagotoonilise faasi läbimist taastub inimene tõeliselt.
Keemiaravi ja kiiritusravi korral arst traditsiooniline meditsiin algselt omandavad pürrhose võidu, kui lõpusekaare tsüstid vähenevad. Aga see saavutatakse paranemise ärajäämise hinnaga ning seda tehes saab kogu organism kohutavalt ja sageli ka korvamatult kahjustatud. Seda ei saa nimetada "teraapiaks", sest inimese eluiga pikeneb parimal juhul vaid lühikest aega – seda aga luuüdi arvelt. Tegelikult pole see ravim, vaid lihtsalt jama! Juhul, kui keemiaravi pole inimest veel täielikult tapnud, algab paranemisprotsess uuesti ja koos sellega naasevad tsüstid uuesti. See viib patsiendi pidevasse nõiaringi, millest ta tavaliselt välja ei pääse.
Mediastiinumi piirkonnas suurte tsüstidega patsientidele tehakse sageli rindkere operatsioon, mille järel saab inimene tavaliselt uue DHS-i konfliktist "rünnak rinnaõõnde vastu" - uut tüüpi vähk - pleura mesotelioom. See vähk käivitatakse väikeajust, mis kontrollib keskmise idukihi - mesodermi - kudesid ja seetõttu toimub konflikti aktiivses faasis lümfoidse tüüpi rakkude kasv. Kompaktne pleura mesotelioom kasvab olenevalt rünnaku iseloomust kas lamedaks või moodustab üksikud suured kompaktsed kasvajad. Näiteks DHS võib käivituda, kui patsient vaatab rindkere röntgenipilti. Kui ta näeb vasakpoolsel küljel kasvajat, tekib tal mesotelioom ja hiljem pleuraefusioon (pärast konflikti lahendamist taastumisfaasis) samale vasakule küljele, kuigi tegelikkuses on kasvaja (näiteks bronhiaalvähk) lokaliseeriti paremal küljel. Selle SBP bioloogiline eesmärk on see, et keha püüab end rünnaku eest kaitsta, püüdes tugevdada rindkere sisemist vooderdust - pleurat - kasvatades mesotelioomi.
Pleuraefusioon on taastumise märk. Hingamisraskused tekivad ainult massiivse pleuraefusiooni korral, osaliselt efusiooni enda ja osaliselt ajuturse tõttu. Aktiivse "pagulaskonflikti" ("sündroom") korral muutub eksudatsiooniprotsess veelgi teravamaks (nt podagra on osteolüüsi paranemise faas, eriti leukeemia korral). "Sündroomi" puudumisel ei tuvastata tavaliselt enamikku eksudatiivse või transudatiivse iseloomuga pleuraefusioone. See kehtib transudatiivse pleuraefusiooni kohta, mida õigemini nimetatakse "podagraks". Pärast seda leitakse sageli kaltsifikatsioone.
Pleura mesotelioomi märgatakse reeglina alles siis, kui keha rünnaku konflikt on lahenenud. Võtame näiteks operatsioonijärgse patsiendi, kellele arst ütleb: "Sinuga on nüüd kõik korras", "rünnak rinnus" konflikti lahendamine annab paranemise märgiks pleuriidi. Kõigi väikeajust ravitavate kasvajate puhul moodustub taastumisfaasis vedelik. Pleuravähk annab pleuriidi, kõhukelmevähk - astsiit, perikardivähk - perikardiit.
Mida traditsioonilises meditsiinis sageli nimetatakse "metastaasideks" ( mida pole olemas nende traditsioonilises tähenduses) - on tegelikult tervenemisprotsess, kuigi tervenemisfaas vajab veel läbielamist (eriti konflikti pikkade retsidiivide korral =) suur mass konflikti ja "sündroomi" juuresolekul). Nüüd pole raske mõista, miks enamik patsiente sureb mõne nädala või kuu jooksul pärast diagnoosi saamist – nad lihtsalt satuvad (või aetakse) nõiaringi, millest nad ei saa enam iseseisvalt välja. Seega on arvamus, et vähk on "juhuslik, saatuslik, kontrollimatu sündmus", põhimõtteliselt vale.
Siin on traditsioonilise meditsiini materjalid: Lümfoom on lümfikoe hematoloogiliste haiguste rühm, mida iseloomustab lümfisõlmede suurenemine ja/või erinevate siseorganid mille puhul toimub "kasvaja" lümfotsüütide kontrollimatu kuhjumine. Lümfoomide esimesed sümptomid on erinevate rühmade (emakakaela, kaenlaaluse või kubeme) lümfisõlmede suuruse suurenemine.
Lümfoomi iseloomustab primaarse tuumori fookuse olemasolu, mis sarnaneb soliidkasvajatega. Lümfoomid on aga võimelised mitte ainult metastaase (tahkete kasvajatena), vaid ka levima kogu kehas samaaegselt lümfoidleukeemiat meenutava seisundi tekkega.
On olemas Hodgkini lümfoom (lümfogranulomatoos) ja mitte-Hodgkini lümfoom (ingl. Mitte - Hodgkin lümfoom ).
Indolentsed lümfoomid (madala pahaloomulisuse astmega lümfoomid) ei pruugi mõnel juhul ravi vajada, piisab arsti (hematoloogi või onkoloogi) järelevalvest. Kuid esimeste progresseerumise märkide korral - lümfisõlmede suurenemine, kehatemperatuuri tõus, täheldatud kehatemperatuuri tõus, kroonilise nõrkuse ilmnemine, algab patsiendi ravi.
Need. arstid teevad vastupidi – “ravivad” inimest siis, kui ta on praktiliselt paranenud, esialgse konflikti šokist eemaldunud ja keha taastumisfaasis. "Teraapia" ajab inimese tagasi, sageli andmata talle mingit võimalust tervist taastada.
Nagu me praegu teame, on vähk ja kõik muud niinimetatud "haigused" osa looduse tähendusrikastest bioloogilistest eriprogrammidest (SBP) – intelligentsed, loogilised ja hästitoimivad läbi evolutsiooni ning põhinevad viiel loodusseadusel.
- Lisa kommentaar
- 14 kommentaari
Valige keel Praegune versioon v.221.1
See haigus erineb teistest vähivormidest selle poolest, et sellel on täiesti erinev bioloogiline iseloom, täiesti erinevad sümptomid, struktuur ja prognoos.
1971. aastal tegi väljapaistev Saksa kirurg Theodor Billroth ettepaneku nimetada seda kasvajat mitte-Hodgkini lümfoomiks või vähiks.
Haiguse põhjused
Põhjuseid ja tegureid, mis võivad põhjustada mitte-Hodgkini lümfoomi, ei ole kindlaks tehtud. Spekuleeritakse, et selle põhjuseks on viirused, kiirgus või koostoime kemikaalidega.
Haiguse päritolu saab alguse lümfotsüütide mutatsioonist, samas muutuvad raku geneetilised tunnused, kuid miks see juhtub, pole selge.
On soovitusi, et lastel tekib patoloogia järgmistel põhjustel:
- Immuunsüsteemi kaasasündinud patoloogiad.
- Omandatud HIV-nakkus.
- Pärast elundisiirdamist, kui enda oma immuunsüsteem alla surutud.
- Viirushaiguste esinemine.
- Kiiritus.
- Teatud kemikaalide mõju ja mitmesugused ravimid.
Mitte-Hodgkini lümfoomid on vähisurmade põhjuste hulgas kuuendal kohal. Statistika kohaselt kannatavad mehed selle haiguse all sagedamini kui naised.
Võib märkida, et haigus muutub üha tavalisemaks. Inimesed haigestuvad vanemas eas. Kuigi haigestumise oht saadab neljakümne aastaga üle piiri läinud inimesi.
Patsiendi vanus ja haiguse tüüp on omavahel seotud. Lastel ja noorukitel diagnoositakse agressiivne mitte-Hodgkini lümfoom. See võib olla väikerakuline, suurrakuline lümfoom, difuusse või lümfoblastse päritoluga kasvajad. Ja kui me räägime vanematest inimestest, avastavad nad tõenäolisemalt follikulaarset lümfoomi, selle arengu aste võib olla erinev.
Lisaks on vihjeid, et pärast somaatilise elundi siirdamist võib ilmneda patoloogia.
Märgid, mis näitavad haiguse algust
Haigust on kahte tüüpi, see on agressiivne ja loid. Mõnel juhul diagnoositakse haiguse väga agressiivne areng. Seejärel hakkab kasvaja katma suuremat kehapiirkonda.
Kui diagnoositakse kõrge pahaloomulise kasvajaga mitte-Hodgkini lümfoomid, kulgeb haigus liiga agressiivselt. Teised mitte-Hodgkini lümfoomide sordid, mille pahaloomulisuse aste on palju madalam, esinevad pikemas manifestatsioonis, need võivad olla kroonilised. Küll aga oskavad nad end spontaanselt väljendada.
Tuleb märkida, et agressiivsel kujul kulgevat haigust saab täielikult ravida, kroonilist ja pikaajalist haigust ei saa ravida.
Hoolimata asjaolust, et traditsiooniline ravi ikka aitab, on raskuseks see, et see kordub sageli ja see viib juba patsiendi surmani. Mitte-Hodgkini lümfoomi diagnoosiga patsiendid elavad seitsmekümnel protsendil juhtudest kuni seitse aastat. Eeldatav eluiga ei sõltu valitud ravimeetodist.
Mõnel juhul degenereeruvad need vähirakud suuremaks pahaloomulisteks kasvajateks ning see juhtub kiiresti ja ootamatult. Pärast sellist degeneratsiooni muutub see hajusaks B-suurrakuks ja hiljem võib see katta ka luuüdi. Kui see juhtub, vähendab see oluliselt patsiendi taastumisvõimalusi ja oodatav eluiga pärast seda on umbes aasta.
Mitte-Hodgkini lümfoomid erinevad leukeemiast selle poolest, et nad hakkavad arenema lümfisüsteemis ja seejärel mõjutavad luuüdi. Sellist diagnoosi saab panna igale inimesele igas vanuses. Alguses esineb patoloogia perifeersetes ja vistseraalsetes lümfisõlmedes, seedetraktis. Mõnikord võib seda leida põrnas, kopsudes ja muudes elundites.
Need lümfoomid jagunevad asukoha järgi:
- Sõlmed, need, mis paiknevad otse lümfisõlmedes.
- Ekstranodaalne.
- Levib vere ja lümfi kaudu.
Need kasvajad katavad esialgu kogu keha. Seetõttu leitakse nende diagnoosimisel kasvajaid mis tahes kehapiirkonnas.
Kui lümfoom esineb väga agressiivsel kujul, tähendab see, et haigus areneb väga kiiresti, see tähendab, et see areneb. Seega, kui ilmnevad esimesed sümptomid ja patsient läheb kliinikusse, leitakse, et peaaegu kogu keha on haigusega kaetud.
Sümptomid
Kuid teisest küljest võib see haigus areneda erineval viisil, nagu ka mis tahes muu haigus. Kuid kuna see areneb lümfoidkoes, on sellel spetsiifilised sümptomid ja need on:
- Lümfadenopaatiat määrab lümfisõlmede suurenemine.
- Ekstranodaalse kasvaja välimus. Näitab konkreetse organi kahjustust. Näiteks võib see olla mao, kesknärvisüsteemi, naha lümfoom.
- Keha nõrkus.
- Kehatemperatuuri tõus.
- Järsk kaalulangus.
Kõik need sümptomid ilmnevad süsteemse tervise halvenemisega.
Mõnel juhul ilmnevad mitte-Hodgkini lümfoomi sümptomid, mis näitavad, et haigus on mõjutanud mitte ainult lümfisüsteemi, vaid ka kõiki organeid, kudesid ja muid kehasüsteeme.
Haiguse arenguks on selline tendents, 45 protsendil patsientidest kulgeb haigus aeglases, kroonilises vormis ja ülejäänutel on haiguse kulg agressiivne.
Kõige sagedamini diagnoositakse haigust seedetraktis, peas ja kaelas. Kuid bronhides ja kopsudes tuvastatakse peamiselt neoplasmi sekundaarsed ilmingud.
Möödunud sajandi lõpus suurenes kesknärvisüsteemi esmaste kasvajaprotsesside diagnoosimine. Tuleb märkida, et neerudes ja põies on patoloogia haruldane.
Diagnoosi ajal on oluline kindlaks teha selle olemasolu või puudumine onkoloogiline protsess luuüdis.
Haiguse etapid
Lümfoomi klassidesse jagunemine toimub vastavalt selle pahaloomulisuse astmele ja struktuurile.
Pahaloomulise kasvaja astme võib jagada kolme tüüpi:
Kuid haigusel on neli etappi:
- Esimest etappi iseloomustab ühe lümfisõlme ja ühe kasvaja kahjustus, mis ei võimaldanud metastaase naaberorganitesse ja süsteemidesse.
- Teine etapp, see on juba mitme lümfisõlme kahjustus, võib mõjutada ka diafragma ühte külge. Sel juhul võivad kohalikud sümptomid ilmneda või mitte. Kui haiguse vorm selles staadiumis on B-rakk, siis on võimalik neoplasm eemaldada kirurgiliselt. Kuigi mõnel juhul pole eemaldamine siiski võimalik.
- Kolmas etapp, selles etapis on kahjustatud diafragma mõlemad pooled, rind. Samuti võivad metastaasid katta kõhuõõnde. Võib esineda luuüdi kasvajaid.
- Neljas staadium on kõige raskem staadium, kus pole enam vahet, kus esmane patoloogia paikneb. Seda iseloomustab lokaliseerimispiirkond, see on luuüdi, kesknärvisüsteem ja luustiku luud.
Haiguse ravi
Enne ravi alustamist tuleb patsientidele läbi viia täiendavad uuringud.
On vaja kontrollida südame tööd, selleks on ette nähtud elektrokardiogramm ja ehhokardiogramm. Samuti selgitatakse, kuidas haigus mõjutas siseorganeid, ainevahetusprotsesse ja kas organismis on infektsioon.
Peaasi, et peale esmaseid analüüse nende tulemused kuhugi ei kaoks, sest hiljem läheb neid vaja, kui raviprotsessis on muudatusi.
Lisaks tuleb kindlaks teha patsiendi veregrupp, sest ükski ravimeetod ei ole täielik ilma vereülekandeta. Seetõttu on rühma määramiseks ette nähtud vere annetamine.
Mitte-Hodgkini lümfoomi ravi
Ükskõik, milline meetod selleks valitud on, on selle eesmärk patsiendi eluea pikendamine ja selle kvaliteedi parandamine. Siiski tuleb märkida, et selle eesmärgi edukus sõltub kasvaja tüübist ja selle arenguastmest. Kui neoplasmil on selged piirid, saab seda kergesti eemaldada, nii et patsiendi eluiga saab pikendada. Kuigi siis on ikkagi vaja läbida eriravi, et haigus ei korduks.
Juhul, kui patoloogiline protsess on haaranud kogu keha, tuleb kasvajavastast ravi rakendada inimtegevuse eluea säilitamise meetoditega.
Kui haigus viib patsiendi siiski paratamatult surma, rakendatakse kõiki ravimeetodeid, mis ei ole suunatud mitte ainult elu jätkumisele, vaid ka selle kvaliteedile.
Meetodid hõlmavad järgmist:
- Sümptomite kõrvaldamine.
- Vaimne abi.
- Sotsiaalne abi.
- Psühholoogiline tugi.
Peaaegu nelikümmend protsenti agressiivse lümfoomi ravijuhtudest, kui prognoos oli soodne, lõpeb positiivsete tulemustega.
Agressiivsete vormidega patsiendid, kui prognoos on soodne, määratakse tavalisele uimastiravi. Selleks määratakse intravenoosselt doksorubitsiin, onkoviin, tsüklofosfamiid, prednisoloon. Pärast seda määratakse keemiaravi ravimid, et vältida haiguse remissiooni. Lisaks on see üks patsiendi eluea pikendamise meetodeid.
Osalise remissiooniga pahaloomulist lümfoomi ravitakse ravimitega ja kiiritatakse patoloogia lokaliseerimiskohti.
Üks väljakutseid on vanemate inimeste teraapia. sest positiivne tulemus ravi sõltub suuresti patsiendi vanusest.
Näiteks saavutatakse ravis täielik remissioon, kui patsient on alla neljakümne aasta vana, juhtub seda kuuekümne viiel protsendil juhtudest. Kuuekümne aasta pärast langeb see näitaja järsult kolmekümne viie protsendini. Kuid on ka toksilisusest põhjustatud surmade statistika, see ulatub kolmekümne protsendini.
Spetsiaalset tehnikat kasutatakse patsientide raviks, kellel esineb haiguse ägenemisi kogu keha kahjustamise korral.
Selle valik sõltub järgmistest teguritest:
- Teatud tüüpi neoplasm.
- Varem kasutatud ravimeetod.
- Keha reaktsioon ravile.
- Patsiendi vanus.
- Keha üldine seisund.
- Kõigi kehasüsteemide töö.
- Luuüdi seisundid.
Tuleb märkida, et haiguse retsidiivi korral ei tohiks te kasutada ravimeid, mida kasutati patsiendi esmakordsel ravil.
Kuid kui retsidiiv tekkis aasta pärast remissiooni algust, võite kasutada algselt määratud ravi.
Hajus suurrakulise lümfoomi ajal ja selle suured suurused, on suur risk retsidiivide tekkeks. Sel juhul on vaja kasutada suuremate annustega ravimeid. Arstid nimetavad seda ravi "meeleheite teraapiaks". Täielik remissioon saavutatakse vaid kahekümne viiel protsendil juhtudest ja isegi siis pole see pikaajaline. Seejärel määratakse patsiendile keemiaravi, kasutades ravimi suuri annuseid, kuid selleks peab patsient olema kõrge somaatilise seisundiga.
Selline ravi on võimalik esimestel retsidiividel, isegi kui haigus kulgeb agressiivses olekus.
Kui haigus kulgeb aeglaselt, saab valida mis tahes tüüpi ravi. sest standardne ravi selliseid vorme ei eksisteeri. Lõppude lõpuks on sellised kasvajad ravi suhtes tundlikud, nii et taastumist ei toimu. Sel juhul kasutatakse tavapäraseid keemiaravi protseduure. Pärast sellist ravi tekivad lühikesed remissioonid, mis lõppevad kiiresti ägenemistega.
Kiiritust kasutatakse ainult patoloogia arengu algfaasis. Alates teisest etapist kasutatakse lisaks kiiritamisele ka ravimeid.
Kui luuüdis tuvastatakse kasvajakahjustusi, kasutatakse standardseid raviskeeme. Kasutatakse selliseid ravimeid nagu kloorbutiin koos prednisolooniga. Hiljem tehakse kemoterapeutilisi protseduure.
See ravimeetod võib pikendada patsiendi eluiga, kuid see ei saa garanteerida, et retsidiive on palju vähem. Ravimite kasutamist ei peatata enne remissiooni saabumist. Lõplik ravimeetod on kiiritus, kuid seda kasutatakse vastavalt näidustustele.
Pärast ravi määratakse patsiendile interferooni süstid kolm korda päevas pooleteise aasta jooksul. See toetab patsiendi nõrka immuunsüsteemi.
Hiljuti on sellist ravimit nagu rituksimab kasutatud sagedamini, see on patoloogilise protsessi pahaloomulistele rakkudele kahjulik ravim. Seda saab kasutada iseseisva ravivahendina ja kombinatsioonis teiste ravimitega.
Ravi rahvapäraste ravimitega
Mitte-Hodgkini lümfoomi raviks võite kasutada valmistatud infusioone, tinktuure ja keetmisi. ravimtaimed ja seened.
Heaks vahendiks peetakse mõru koirohu, musta tibu, hemlocki infusioone.
Kui arvestada seeni, võite kasutada shiitake, reishi, kasetšaga ja paljud teised. Seened on võimelised tõkestama metastaaside levikut, taastama hormonaalset tasakaalu, vähendama keemiaravi järel tekkivaid kõrvalmõjusid (iiveldus, kiilaspäisus, valud).
Kui võtate reishi ja shiitake seeni, saate taastada verevalemi ja aktiveerida immuunsüsteemi.
Kasvaja toksiinide organismist väljaviimiseks on vaja kaseseen segada ussijuurega (eelnevalt hakitud). Seejärel valage segu viinaga, katke kinni ja pange kahekümne üheks päevaks pimedasse kohta. Tinktuura on valmis, peaksite võtma nelikümmend tilka kuus korda päevas.
Kuidas keetmist valmistada?
Jahvatage ja segage saialilleõisi, jahubanaani lehti, ürdi apokalüpsist. Valage vette ja keetke kümme minutit. Seejärel eemaldage tulelt ja laske toatemperatuuril jahtuda. Joo mee ja sidruniga.
Prognoos
Kõik mittespetsiifilised kopsuhaigused (nln) ennustatakse kasvaja skoori või Mannheimi kõhukelme indeksi (MPI) järgi. Iga negatiivne sümptom ja märk saab ühe punkti, lõpus summeeritakse.
Andmete arvutamisel valib arst sobiva ravimeetodi.
B-rakulised kasvajad saavad positiivse prognoosi ja T-rakulised kasvajad, vastupidi, ainult ebasoodsad. Prognoosi mõjutavad suuresti sellised tegurid nagu patsiendi vanus, neoplasmi tüüp, arengustaadium ja kahjustuse aste.
Soodsateks peetakse järgmisi patoloogiaid: lümfoomid seedetrakti, süljenäärmed. Ebasoodsate hulka kuuluvad: kesknärvisüsteemi, rinna, luukoe, munasarjade lümfoomid.
Toitumine lümfoomi korral
Õige toitumise jaoks on mitu kriteeriumi:
- Mõõdukalt kõrge kalorsusega, nii et patsient ei võtaks ülekaalu ja on üsna mitmekesine. Teisisõnu, toidus peaks olema kõik: köögiviljad, puuviljad, liha, kala, maitsetaimed, mereannid.
- Vähendage konservide, suitsuliha, soola kogust.
Söögid peaksid olema sagedased, kuid osa peaks olema väike. Iga patsiendi lähenemine peaks olema individuaalne.
Inimesed ei saa süüa värsket toitu, nii et kaaviari ja oliive võib nende dieeti veidi lisada. Kuid paralleelselt peab patsient võtma ravim mis aitab eemaldada naatriumi kehast.
Kui on ette nähtud keemiaravi protseduuride kuur, ei tohi seda võtta pärast keemiaravi, eriti kui kõrvalmõju algas oksendamine ja kõhulahtisus, naatrium on organismis vajalik.
Mitte-Hodgkini lümfoomid
Mitte-Hodgkini lümfoomid on lümfisüsteemi pahaloomulised haigused, mida esindavad pahaloomulised B- ja T-rakulised lümfoomid. Mitte-Hodgkini lümfoomi esmane fookus võib esineda lümfisõlmedes või muudes elundites ja seejärel metastaaseeruda lümfogeense või hematogeense tee kaudu. Mitte-Hodgkini lümfoomide kliinikut iseloomustavad lümfadenopaatia, ühe või teise organi kahjustuse sümptomid ja palaviku-mürgistuse sündroom. Diagnoos põhineb kliinilistel ja radioloogilistel andmetel ning hemogrammi, lümfisõlmede ja luuüdi biopsia tulemustel. Kasvajavastane ravi hõlmab polükemoteraapia ja kiiritusravi kursusi.
Mitte-Hodgkini lümfoomid
Mitte-Hodgkini lümfoomid (lümfosarkoomid) on pahaloomulised lümfoproliferatiivsed kasvajad, mis erinevad morfoloogia, kliiniliste tunnuste ja kulgemise poolest ning erinevad oma omaduste poolest Hodgkini lümfoomist (lümfogranulomatoos). Sõltuvalt primaarse fookuse esinemiskohast jagatakse hemoblastoosid leukeemiateks (luuüdi kasvajakahjustused) ja lümfoomideks (primaarse medullaarse lokaliseerimisega lümfoidkoe kasvajad). Lümfoomi iseloomulike morfoloogiliste tunnuste põhjal jagunevad need omakorda Hodgkini ja mitte-Hodgkini omadeks; viimaste hulka hematoloogias kuuluvad B- ja T-rakulised lümfoomid.
Mitte-Hodgkini lümfoome esineb kõigis vanuserühmades, kuid enam kui pooled lümfosarkoomi juhtudest diagnoositakse üle 60-aastastel inimestel. Keskmine esinemissagedus meeste seas on 2-7 juhtu, naistel - 1-5 juhtu elanikkonna kohta. Viimastel aastatel on täheldatud mitte-Hodgkini lümfoomide esinemissageduse järkjärgulist suurenemist.
Mitte-Hodgkini lümfoomide põhjused
Lümfosarkoomide etioloogia on teadmata ja seetõttu on õigem rääkida riskiteguritest, mis suurendavad mitte-Hodgkini lümfoomi tekke tõenäosust. Selliste ebasoodsate tingimuste hulka kuuluvad viiruslikud kahjustused (HIV, Epstein-Barri viirus, C-hepatiit). Maohaavandiga seotud Helicobacter pylori infektsioon võib põhjustada sama lokaliseerimisega lümfoomi arengut.
Mitte-Hodgkini lümfoomide tekkerisk suureneb kaasasündinud ja omandatud immuunpuudulikkuse, rasvumise, vanemas eas, pärast elundisiirdamist. Lümfosarkoomide ja varasema kokkupuute vahel keemiliste kantserogeenidega (benseen, insektitsiidid, herbitsiidid), kiirituse ja vähiravi keemiaraviga on põhjuslik seos. Kilpnäärme lümfoom areneb tavaliselt autoimmuunse türeoidiidi taustal.
Mitte-Hodgkini lümfoomide klassifikatsioon
Lümfosarkoome, mis arenevad peamiselt lümfisõlmedes, nimetatakse sõlmedeks, teistes organites (suulae- ja neelumandlid, süljenäärmed, magu, põrn, sooled, aju, kopsud, nahk, kilpnääre jne) - ekstranodaalseteks. Kasvajakoe struktuuri järgi jagunevad mitte-Hodgkini lümfoomid follikulaarseteks (nodulaarseteks) ja difuusseteks.
Progressioonikiiruse järgi liigitatakse mitte-Hodgkini lümfoomid loiduks (aeglase ja suhteliselt soodsa kulgemisega), agressiivseteks ja üliagressiivseteks (kiire arengu ja üldistamisega). Ravimata jätmise korral elavad loidsete lümfoomidega patsiendid keskmiselt 7-10 aastat, agressiivsete - mitmest kuust kuni 1,5-2 aastani.
Kaasaegne klassifikatsioon sisaldab enam kui 30 erinevat tüüpi mitte-Hodgkini lümfoomi. Enamik kasvajaid (85%) pärinevad B-lümfotsüütidest (B-raku lümfoomid), ülejäänud T-lümfotsüütidest (T-raku lümfoomid). Nendes rühmades on erinevad mitte-Hodgkini lümfoomide alatüübid.
B-rakuliste lümfoomide rühma kuuluvad:
- difuusne suur B-rakuline lümfoom on kõige levinum mitte-Hodgkini lümfoomi histoloogiline tüüp (31%). Seda iseloomustab agressiivne kasv, hoolimata sellest, peaaegu pooltel juhtudel saab seda täielikult ravida.
- follikulaarne lümfoom - selle esinemissagedus on 22% mitte-Hodgkini lümfoomide arvust. Kursus on loid, kuid võimalik on muutumine agressiivseks hajutatud lümfoomiks. 5-aastase elulemuse prognoos on 60-70%.
- väikerakk-lümfotsüütiline lümfoom ja krooniline lümfotsüütleukeemia on sarnased mitte-Hodgkini lümfoomide tüübid, mis moodustavad 7% nende arvust. Kursus on aeglane, kuid halvasti ravitav. Prognoos on varieeruv: mõnel juhul areneb lümfosarkoom välja 10 aasta jooksul, mõnel juhul muutub see teatud staadiumis kiiresti kasvavaks lümfoomiks.
- lümfoom mantlirakkudest - mitte-Hodgkini lümfoomide struktuuris on 6%. Ainult 20% patsientidest ületab viieaastase elulemuse piiri.
- Marginaalse tsooni rakkudest pärinevad B-rakulised lümfoomid jagunevad ekstranodaalseteks (võivad areneda maos, kilpnäärmes, süljes, piimanäärmetes), sõlmelisteks (areneb lümfisõlmedes), põrnaks (lokaliseerumisega põrnas). Erineb aeglase kohaliku kasvu poolest; varases staadiumis annavad ravile hästi järele.
- B-rakuline mediastiinumi lümfoom – esineb harva (2% juhtudest), kuid erinevalt teist tüüpi mitte-Hodgkini lümfoomist mõjutab see peamiselt noori naisi. Seoses kiire kasvuga põhjustab mediastiinumi organite kokkusurumine; paraneb 50% juhtudest.
- Waldenströmi makroglobulineemia (lümfoplasmotsüütiline lümfoom) diagnoositakse 1% mitte-Hodgkini lümfoomiga patsientidest. Seda iseloomustab IgM hüperproduktsioon kasvajarakkude poolt, mis põhjustab vere viskoossuse suurenemist, veresoonte tromboosi ja kapillaaride rebenemist. Sellel võib olla nii suhteliselt healoomuline (elulemus kuni 20 aastat) kui ka mööduv areng (patsiendi surmaga 1-2 aasta jooksul).
- Karvrakuline leukeemia on väga haruldane mitte-Hodgkini lümfoomi tüüp, mis esineb vanematel inimestel. Kasvaja kulg on aeglane, ei vaja alati ravi.
- Burkitti lümfoom – see moodustab umbes 2% mitte-Hodgkini lümfoomidest. 90% juhtudest mõjutab kasvaja alla 30-aastaseid noori mehi. Burkitti lümfoomi kasv on agressiivne; intensiivne keemiaravi võimaldab saavutada poolte patsientide paranemise.
- kesknärvisüsteemi lümfoom – kesknärvisüsteemi esmane kahjustus võib mõjutada pea- või seljaaju. Seostub sagedamini HIV-nakkusega. Viie aasta elulemus on 30%.
T-rakulise päritoluga mitte-Hodgkini lümfoomid on esindatud:
- T-lümfoblastiline lümfoom või eellasleukeemia - esineb sagedusega 2%. Need erinevad üksteisest luuüdi blastrakkude arvu poolest: 25% - nagu leukeemia. Seda diagnoositakse peamiselt noortel inimestel, haigete keskmine vanus on 25 aastat. Halvim prognoos on T-lümfoblastne leukeemia, mille paranemise määr ei ületa 20%.
- perifeersed T-rakulised lümfoomid, sealhulgas naha lümfoom (Cesari sündroom, mycosis fungoides), angioimmunoblastne lümfoom, ekstranodaalne looduslik tapja-lümfoom, enteropaatiaga lümfoom, subkutaanne pannikuliit-sarnane lümfoom, anaplastiline suurrakuline lümfoom. Enamiku T-rakuliste mitte-Hodgkini lümfoomide kulg on kiire ja tulemus on halb.
Mitte-Hodgkini lümfoomide sümptomid
Mitte-Hodgkini lümfoomide kliiniliste ilmingute variandid varieeruvad suuresti sõltuvalt primaarse fookuse lokaliseerimisest, kasvajaprotsessi levimusest, kasvaja histoloogilisest tüübist jne. Kõik lümfosarkoomide ilmingud jagunevad kolmeks sündroomiks: lümfadenopaatia, palavik ja mürgistus. , ekstranodaalsed kahjustused.
Enamikul juhtudel on mitte-Hodgkini lümfoomi esimene märk perifeersete lümfisõlmede suurenemine. Algul jäävad nad elastseks ja liikuvaks, hiljem sulanduvad suurteks konglomeraatideks. Samal ajal võivad mõjutada ühe või mitme piirkonna lümfisõlmed. Fistuloossete käikude moodustumisel on vaja välistada aktinomükoos ja tuberkuloos. Mediastiinsete lümfisõlmede kahjustusega areneb söögitoru ja hingetoru kokkusurumine, SVC kokkusurumise sündroom. Suurenenud intraabdominaalsed ja retroperitoneaalsed lümfisõlmed võivad põhjustada soolesulgust, lümfostaasi keha alumises pooles, obstruktiivset kollatõbe ja kusejuha kokkusurumist.
Sellised mitte-Hodgkini lümfoomide mittespetsiifilised sümptomid, nagu palavik ilma ilmsete põhjusteta, öine higistamine, kehakaalu langus, asteenia, viitavad enamikul juhtudel haiguse üldistatud olemusele. Ekstranodaalsete kahjustuste hulgas domineerivad Pirogov-Waldeyeri ringi, seedetrakti ja aju mitte-Hodgkini lümfoomid; harvemini on kahjustatud piimanääre, luud, kopsuparenhüüm ja muud organid.
Nasofarüngeaalne lümfoom on endoskoopilisel uurimisel kahvaturoosa kasvaja, millel on mugulakujulised kontuurid. Sageli tärkavad ülalõua- ja ninakõrvalurged, orbiit, põhjustades nasaalse hingamise raskusi, rinofooniat, kuulmislangust, eksoftalmust.
Primaarsel munandi mitte-Hodgkini lümfoomil võib olla sile või konarlik pind, elastne või kivine kõvadus. Mõnel juhul tekib munandikoti turse, naha haavandid kasvaja kohal, kubeme-niude lümfisõlmede suurenemine. Munandite lümfoomidel on eelsoodumus varaseks levikuks koos teise munandi, kesknärvisüsteemi jne kahjustusega.
Rindade lümfoom palpatsioonil on määratletud kui selge kasvaja sõlm või difuusne rinna tihendus; nibu tagasitõmbumine on ebaloomulik. Kui kõht on kahjustatud, sarnaneb kliiniline pilt maovähiga, millega kaasneb valu, iiveldus, isutus ja kaalulangus. Kõhu mitte-Hodgkini lümfoomid võivad avalduda osalise või täieliku soolesulgusena, peritoniidina, malabsorptsiooni sündroomina, kõhuvalu, astsiidina.
Naha lümfoom avaldub sügeluse, sõlmede ja punakaslilla kõvendusena. Kesknärvisüsteemi esmane kahjustus on tüüpilisem AIDS-iga patsientidele - selle lokaliseerimise lümfoomi kulgemisega kaasnevad fokaalsed või meningeaalsed sümptomid.
Mitte-Hodgkini lümfoomide diagnoosimine
Mitte-Hodgkini lümfoomide diagnoosimise küsimused on onkohematoloogide pädevuses. Lümfosarkoomi kliinilised kriteeriumid on ühe või mitme lümfisõlmede rühma suurenemine, mürgistus, ekstranodaalsed kahjustused.
Kavandatud diagnoosi kinnitamiseks on vaja uurida kasvaja rakulist substraati. Sel eesmärgil tehakse diagnostilisi operatsioone: lümfisõlmede punktsioon või ekstsisioonbiopsia, laparoskoopia, torakoskoopia, luuüdi punktsioon koos järgnevate immunohistokeemiliste, tsütoloogiliste, tsütogeneetiliste ja muude diagnostilise materjali uuringutega. Lisaks diagnoosimisele on see oluline ravitaktika valikul ja mitte-Hodgkini lümfoomide prognoosi määramisel.
Vajalik on eristada mitte-Hodgkini lümfoome lümfogranulomatoosi, metastaatilise vähi, tulareemiaga esineva lümfadeniidi, brutselloosi, tuberkuloosi, toksoplasmoosi, süüfilise, nakkusliku mononukleoosi, gripi, SLE-ga jne.
Mitte-Hodgkini lümfoomide ravi
Mitte-Hodgkini lümfoomide ravivõimalused hõlmavad kirurgiat, kiiritusravi ja keemiaravi; nende valiku määrab kasvaja morfoloogiline tüüp, levimus, lokaliseerimine, patsiendi ohutus ja vanus.
Kirurgilist sekkumist kasutatakse tavaliselt organi, tavaliselt seedetrakti, isoleeritud kahjustuse korral. Kiiritusravi kui mitte-Hodgkini lümfoomide monoteraapiat kasutatakse ainult lokaliseeritud vormide ja madala astme kasvajate korral. Lisaks saab kiiritust kasutada ka palliatiivse meetodina, kui keemiaravi ei ole võimalik.
Kõige sagedamini algab mitte-Hodgkini lümfoomide ravi polükemoteraapia kuuriga. See meetod võib olla sõltumatu või kombineeritud kiiritusraviga. Kombineeritud kemoradioteraapia võimaldab saavutada pikemaid remissioone. Ravitsüklitesse on võimalik lisada hormoonravi. Ravi jätkub kuni täieliku remissiooni saavutamiseni, pärast mida on vaja veel 2-3 tugevdavat kuuri.
Alternatiivsed meetodid hõlmavad immunoteraapiat interferooniga, monoklonaalseid antikehi, autoloogse või allogeense luuüdi ja perifeersete tüvirakkude siirdamist.
Mitte-Hodgkini lümfoomide prognoos on erinev, sõltuvalt peamiselt kasvaja histoloogilisest tüübist ja avastamise staadiumist. Lokaalselt arenenud vormide puhul on pikaajaline elulemus keskmiselt 50-60%, üldistatud vormide puhul vaid 10-15%.
Mitte-Hodgkini lümfoomid - ravi Moskvas
Haiguste kataloog
Verehaigused
Viimased uudised
- © 2018 "Ilu ja meditsiin"
on ainult informatiivsel eesmärgil
ja see ei asenda kvalifitseeritud arstiabi.
Mitte-Hodgkini lümfoom: sümptomid ja ravi
Mitte-Hodgkini lümfoom - peamised sümptomid:
- Peavalu
- Nõrkus
- Suurenenud lümfisõlmed
- Naha sügelus
- Kõhuvalu
- kõrgendatud temperatuur
- Kaalukaotus
- Hingeldus
- Seljavalu
- higistamine
- Köha
- Väsimus
- Suurenenud higistamine
- letargia
Onkoloogilised haigused on tänapäeval ühed raskeimad ja raskemini ravitavad haigused. Nende hulka kuuluvad mitte-Hodgkini lümfoom. Võimalusi on aga alati ja selge ettekujutus haigusest, selle tüüpidest, põhjustest, diagnoosimismeetoditest, sümptomitest, ravimeetoditest ja tulevikuprognoosist võib neid suurendada.
Mis on haigus
Et mõista, mis on mitte-Hodgkini lümfoom, tuleks mõista lümfoomi mõistet üldiselt. Lümfoom on nimi, mis ühendab onkoloogiliste haiguste rühma. Vähirakud mõjutavad lümfikoe, lümfisõlmed suurenevad oluliselt, võivad kannatada somaatilised elundid. Mitte-Hodgkini lümfoom on mis tahes tüüpi haigus, mis ei ole Hodgkini lümfoom.
Mis võib haigust põhjustada
Mitte-Hodgkini lümfoomi põhjused pole veel täielikult teada. Kaudselt võivad haiguse arengut ja edasist prognoosi mõjutada järgmised tegurid:
- töötada agressiivsete kemikaalidega;
- elamine ebasoodsate keskkonnatingimustega piirkondades;
- raske viirusnakkused, eriti - Epstein-Barri viirus;
- kokkupuude ioniseeriva kiirgusega.
Samuti võib märkida, et mehed põevad mitte-Hodgkini lümfoomi mõnevõrra sagedamini kui naised. Samuti suureneb vanusega haiguse avastamise tõenäosus: statistika järgi on haigete seas enamus üle 40-aastaseid. Haiguse vorm sõltub sageli vanusest: lastel ja noortel esineb sagedamini haiguse väikerakulise vormi ehk Burkitti lümfoomi sümptomeid, follikulaarseid lümfoome täheldatakse tavaliselt eakatel.
Haiguse erinevate vormide klassifikatsioon
Nagu juba mainitud, on mitte-Hodgkini lümfoom nimi, mis ühendab rühma sarnaseid (üsna sarnaseid sümptomeid, ravimeetodeid ja prognoose tulevikuks), kuid siiski erinevaid haigusi. Ja neid haigusi saab jagada järgmiste tunnuste järgi:
Haiguse kulgemise olemus
Selle põhjal jagatakse mitte-Hodgkini lümfoomid kahte tüüpi: agressiivsed ja indolentsed lümfoomid, mis arenevad kiiresti, sõna otseses mõttes "purskuvad". mitmesugused sümptomid ja levis kogu kehas uskumatu kiirusega. Kummalisel kombel ravitakse kõige tõenäolisemalt just agressiivseid lümfoomi. Indolentseid lümfoome iseloomustavad loid, krooniline kulgäkiliste ägenemistega. Just need retsidiivid põhjustavad sageli patsiendi surma. Lisaks kipub indolentset tüüpi lümfoom degenereeruma difuusseks suureks rakuks, mis suurendab oluliselt pahaloomulist kasvajat ja seega halvendab prognoosi.
Kasvaja lokaliseerimine
Kuigi nimi "lümfoom" viitab peamiselt lümfisõlmede lüüasaamisele, võib lümfoomi leida mitte ainult seal. Sõltuvalt lokaliseerimisest eristatakse järgmisi lümfoomi tüüpe:
- Sõlm. Selles variandis paiknevad kasvajad eranditult lümfisõlmedes. Tavaliselt on see umbes varajased staadiumid haigused. Selle vormi prognoos on üsna hea, pikaajalise remissiooni võimalus on suur.
- Ekstranodaalne. Sel juhul levib lümfoom kudedesse ja organitesse – lümfi või vere kaudu. Haiguse kaugelearenenud staadiumides tungivad kasvajad luudesse ja ajju. Üks kõige enam rasked vormid ekstranodaalne lümfoom on Burkitti lümfoom.
- hajus. Sel juhul on lümfoomi tuvastamine kõige raskem, kuna seintel asuvad patogeensed rakud veresooned, sest lümfisõlme joonistus kustutatakse. Rakkude kuju järgi võib difuusne lümfoom olla: polülümfotsüütne (sel juhul täheldatakse suuri ümaraid patogeenseid rakke), lümfoblastne (keerdunud rakud), immunoblastne (keskraku ümber toimub tugev rakkude vohamine - nukleoolid) ja ei ole eristatav.
Haiguse sümptomid
Reeglina on haiguse esimesed etapid peaaegu asümptomaatilised. Siiski on veidi hiljem näha järgmised sümptomid haigused:
- Lümfisõlmede (tavaliselt emakakaela ja aksillaarne) tugev suurenemine.
- Nõrkus, letargia.
- Kõrgendatud temperatuur.
- Üsna kiire kaalulangus.
- Liigne higistamine isegi jaheda või külma ilmaga.
- Peavalu.
Kõik ülaltoodud sümptomid on üsna tavalised, mistõttu on lümfoomi varajases staadiumis üsna raske tuvastada. Kui aga siiski õnnestus lümfisõlme suurenemine leida, tuleb koheselt pöörduda spetsialisti poole, sest lümfisõlmede suurenemine võib tekkida nii külmetusest kui ka sellisest. tõsine haigus nagu lümfoom.
Kuidas diagnoositakse
Lisaks kogutud anamneesile on täpse diagnoosi kindlakstegemiseks vaja läbi viia mitmeid täiendavaid uuringuid. Nende hulgas:
- Histoloogiline uuring (lümfisõlme punktsioon või biopsia). Tänu sellele analüüsile saab lümfis tuvastada patoloogilisi rakke, mis viitavad lümfoomi esinemisele.
- Punktaadil põhinevad tsütoloogilised ja tsütokeemilised analüüsid.
- Immunoloogilised uuringud.
Kui on võimalik välja selgitada, kas inimesel on lümfoom, määratakse muud uuringud, mis aitavad kindlaks teha kõik haiguse parameetrid, sest sellest sõltub edasine ravi.
Haiguse arenguetapid
Haiguse diagnoosimise käigus tehakse kindlaks selle pahaloomulisus ja haiguse staadium. Pahaloomulisus võib olla kõrge, madal või keskmine. Mis puudutab etappe, siis neid on neli.
ma lavastan
Haiguse algses, esimeses staadiumis võib täheldada ainult eraldiseisvat põletikulist lümfisõlme, üldised sümptomid(nõrkus, halb enesetunne, hüpertermia) ei ole täheldatud.
II etapp
Sellise haiguse nagu mitte-Hodgkini lümfoomi teises etapis muutuvad kasvajad mitmekordseks. Järk-järgult hakkavad ilmnema üldised sümptomid. Kui me räägime B-raku vormist, siis selles etapis hakatakse kasvajaid jagama eemaldatavateks ja mitte eemaldatavateks.
III etapp
Selles haiguse arengufaasis levivad kasvajad sageli diafragmasse, kõhuõõnde ja rindkeresse. Mõjutatud on kuded, samuti kõik või peaaegu kõik siseorganid.
IV etapp
Haiguse viimane ja kõige raskem staadium. Kahjuks on sel juhul prognoos väga pettumust valmistav. Haigus mõjutab mitte ainult elundeid, vaid ka luuüdi, satub kesknärvisüsteemi ja luudesse. Kui ravi viibis nii palju, et lümfoom läks sellesse staadiumisse, siis ei saa paranemisest juttugi olla.
Millised on mitte-Hodgkini lümfoomi ravimeetodid?
Ravi meetodid sõltuvad paljuski haiguse olemusest, kasvajate suurusest, staadiumist ja pahaloomulisest kasvajast. Kuid üldiselt saab haigusega võitlemiseks eristada järgmisi viise:
- Keemiaravi. Tema on ravi aluseks. Madala astme lümfoomide varases (esimeses ja teises) staadiumis kasutatakse monokemoteraapiat. Kui staadiumid on rasked või lümfoom käitub äärmiselt agressiivselt, kasutatakse polükemoteraapiat. Mõnikord kombineeritakse keemiaravi kiiritusraviga, kuid kiiritamine puhtal kujul aitab ainult I etapis. Samuti rakendatakse kiiritusravi mõnikord lokaalselt nendes piirkondades, kus kasvaja käitub kõige agressiivsemalt.
- Kasvaja kirurgiline eemaldamine. Loomulikult kasutatakse seda meetodit ainult siis, kui kasvaja staadium ja tüüp seda võimaldavad. Kiiritusravi eduka kasutamisega ja kirurgiline sekkumine prognoos on üsna positiivne: remissioon võib tekkida 5–10 aasta jooksul.
- Programmide BATsOP, TsOP jne kasutamine. Pean ütlema, et need programmid näitavad üsna head jõudlust.
- Palliatiivne ravi, mille eesmärk on leevendada valu ja parandada patsiendi elukvaliteeti nii palju kui võimalik. Seda kasutatakse lõppstaadiumis, kui prognoos on ebasoodne ja haiguse võitmise võimalused on väga väikesed. Lisaks ravimitele võib patsient vajada psühholoogi abi, aga ka lähedaste tuge.
Milline on haiguse tulemuse prognoos
Nagu juba mainitud, on ravi ja ka selle mõju mitte-Hodgkini lümfoomi puhul väga individuaalne küsimus. Kellelgi õnnestub esimesel katsel saavutada täielik taastumine, keegi peab silmitsi seisma ägenemistega, keegi saab eluiga pikendada vaid mitme aasta võrra ja mõnel juhul on meditsiin täiesti jõuetu. Diagnoosi ei tohiks siiski pidada lauseks: õigeaegse diagnoosi korral õige ravi ja mitte liiga problemaatiline haiguse vorm, taastumise võimalused ulatuvad 65-70%. Ja sellest piisab.
Kui arvate, et teil on mitte-Hodgkini lümfoom ja sellele haigusele iseloomulikud sümptomid, siis saavad teid aidata arstid: onkoloog, hematoloog, kirurg.
Soovitame kasutada ka meie veebipõhist haiguste diagnostika teenust, mis valib sisestatud sümptomite põhjal välja tõenäolised haigused.
Histoplasmoos on haigus, mille areng tekib konkreetse seeninfektsiooni tungimise tõttu inimkehasse. Selle patoloogilise protsessiga mõjutavad siseorganid. Patoloogia on ohtlik, kuna see võib areneda erineva vanusega inimestel. Ka meditsiinilises kirjanduses võib leida selliseid haiguse nimetusi - Ohio Valley haigus, Darlingi tõbi, retikuloendotelioos.
Lümfotsütaarne leukeemia on pahaloomuline kahjustus, mis esineb lümfikoes. Seda iseloomustab kasvaja lümfotsüütide kogunemine lümfisõlmedesse, perifeersesse veresse ja luuüdis. Lümfotsütaarse leukeemia äge vorm on hiljuti klassifitseeritud "lapseea" haiguseks, kuna see on kokku puutunud peamiselt kahe kuni nelja aasta vanused patsiendid. Tänapäeval täheldatakse täiskasvanute seas sagedamini lümfotsüütilist leukeemiat, mille sümptomeid iseloomustab nende spetsiifilisus.
Lümfoom ei ole üks konkreetne haigus. See on terve rühm hematoloogilisi vaevusi, mis mõjutavad tõsiselt lümfisüsteemi. Kuna seda tüüpi kuded paiknevad peaaegu kogu inimkehas, võib pahaloomuline patoloogia tekkida mis tahes piirkonnas. Isegi siseorganid võivad olla kahjustatud.
Leukeemia (sün. leukeemia, lümfosarkoom ehk verevähk) on rühm kasvajahaigusi, millel on iseloomulik kontrollimatu kasv ja mitmesugused etioloogiad. Leukeemia, mille sümptomid määratakse selle spetsiifilise vormi alusel, kulgeb normaalsete rakkude järkjärgulise asendamisega leukeemiliste rakkudega, mille vastu tekivad tõsised tüsistused (verejooks, aneemia jne).
zoonootiline infektsioon, mille kahjustuspiirkond on peamiselt südame-veresoonkonna, lihasluukonna, suguelundite ja närvisüsteemid inimest nimetatakse brutselloosiks. Selle haiguse mikroorganismid tuvastati juba 1886. aastal ja haiguse avastajaks on inglise teadlane Bruce Brucellosis.
Treeningu ja karskuse abil saab enamik inimesi ilma ravimiteta hakkama.
Inimeste haiguste sümptomid ja ravi
Materjalide kordustrükk on võimalik ainult administratsiooni loal ja allikale aktiivse lingi märkimisel.
Kogu esitatud teave kuulub raviarsti kohustusliku konsultatsiooni alla!
Küsimused ja ettepanekud:
Mitte-Hodgkini lümfoom on üks levinumaid vähiliike, mis mõjutab sadu inimesi üle maailma. Et mõista, kuidas haigust ära tunda ja seda ravida, peate kõigepealt mõistma, mis see on.
Mitte-Hodgkini lümfoom on koondmõiste, see viitab tervele rühmale onkoloogilistest haigustest, mille puhul pahaloomulised rakud mõjutavad lümfoidkudesid. Teisisõnu hõlmab see kategooria kõiki olemasolevaid lümfoomi liike, välja arvatud Hodgkini lümfoom. Viimase eripäraks on muutunud ja mitmetuumaliste rakkude olemasolu kahjustatud kudedes.
Haiguse tunnused
Mitte-Hodgconi lümfoomide hulka kuulub umbes 80 mitmesugused haigused, mis erinevad agressiivsuse ja lokaliseerimise poolest.
Patsientide hulgas on ligikaudu sama palju mehi ja naisi, kuigi mõne haiguse puhul on endiselt sõltuvus soost. Mis puutub vanusekategooriatesse, siis vanematel inimestel on veidi suurem risk haigestuda onkoloogiasse. Samal ajal diagnoositakse seda haigust sageli lastel.
Kuna mitte-Hodgkini lümfoomid ei ole üks, vaid palju haigusi, mida ühendab üks tunnus, tuleks korraga arvestada mitmete vormide ja sortidega. Sellised tunnused nagu ravikuuri kestus ja intensiivsus, ravi prognoos ja võimalikud tüsistused sõltuvad otseselt haiguse omadustest.
B-raku vorm
Kõige tavalisemaks klassifikatsioonitüübiks võib pidada Maailma Terviseorganisatsiooni poolt vastu võetud klassifikatsiooni. See põhineb täpselt onkoloogia rakulisel koostisel. On 2 laia kategooriat: B-rakulised ja T-rakulised lümfoomid. Igaüht neist tuleks üksikasjalikumalt mainida.
Mis on B-rakuline mitte-Hodgkini lümfoom? See on lümfoidkoe pahaloomuline haigus, mis mõjutab B-lümfotsüüte. Nende põhiülesanne on antikehade tootmine, seetõttu osalevad nad ka immuunhumoraalses vastuses. Lümfoome on mitut tüüpi:
- Sõlme ja põrn. Neid liike iseloomustab aeglane kasv.
- Burkitti lümfoom. Meditsiinistatistika kohaselt kannatavad selle haigusvormiga sagedamini umbes 30-aastased mehed. Arstid ei kiirusta soodsat prognoosi andma: Burkitti mitte-Hodgkini lümfoomiga patsientide elulemus 5 aasta jooksul on vaid 50%.
- Follikulaarne. Enamikul juhtudel areneb see onkoloogiline haigus üsna aeglaselt, kuid see võib muutuda hajusaks vormiks, mida iseloomustab kiire areng.
- Marginaalse tsooni MALT lümfoom. See vorm levib makku ja suureneb aeglaselt. Kogu selle raviga on seda äärmiselt raske ravida.
- Primaarne mediastiinum (või mediastiinum). See haigus mõjutab kõige sagedamini naisi, 5-aastane elulemus pärast ravi on 50%.
- Lümfotsentriline väikerakk. Areng on aeglane, kuid paranemise määr on üsna madal.
- Primaarne kesknärvisüsteemi lümfoom.
- Difuusne mitte-Hodgkini lümfoomi suur rakk. See sort viitab kiiresti progresseeruvatele onkoloogilistele haigustele.
Mitte-Hodgkini T-rakulise lümfoomi sordid
T-rakuline lümfoom on pahaloomuline haigus, mille puhul esineb T-lümfotsüütide kontrollimatu kasv. Nende tootmine toimub harknääres ja nad toetavad naha ja limaskestade rakulist (või barjääri) immuunsust.
- lümfoblastiline vorm. Enamik selle diagnoosiga patsiente on alla 40-aastased noored mehed. Ravi soodsat tulemust ennustatakse ainult siis, kui luuüdi protsessi ei kaasata.
- Suurerakuline mitte-Hodgkini lümfoom anaplastiline. Enamasti esineb see haigus noortel inimestel, kuid õigeaegse diagnoosi korral allub see ravile hästi.
- Ekstranodaalne NHL. See haigusvorm mõjutab T-tapjaid, selle agressiivsus võib olla erinev.
- Cesari sündroom (või nahahaigus). Seda vormi nimetatakse sageli seente mükoosiks ja see moodustub peamiselt vanematel inimestel (50-60 aastat).
- Lümfoom koos enteropaatiaga. On märgatud, et seda tüüpi vähk on tüüpiline gluteenitalumatusega inimestele. Seda iseloomustab äärmiselt agressiivne ja raskesti ravitav.
- Angioimmunoblastiline. Seda tüüpi on raske ravida ja seetõttu ei tee arstid eluks soodsat prognoosi.
- Mitte-Hodgkini lümfoom on pannikuliiti sarnane. Selline onkoloogia areneb nahaaluses rasvas. Selle vormi iseloomulik tunnus on madal tundlikkus keemiaravi suhtes, mis muudab ravi ebaefektiivseks.
Liigid agressiivsuse järgi
Teine võimalus neodgkini lümfoomide klassifitseerimiseks on jagamine protsessi agressiivsuse järgi. See on arstidele väga mugav, kuna võimaldab optimaalselt valida ravikuuri ja vaatlustaktika.
- Agressiivne NHL. See tüüp hõlmab onkoloogilisi haigusi kiire areng, aktiivselt leviv ja mõnel juhul keemiaravi suhtes resistentne. Siin saab ravi prognoosi teha peamiselt onkoloogia staadiumi põhjal, mil mitte-Hodgkini lümfoom avastati. Nende haigusvormide retsidiivid esinevad üsna sageli.
- Laisk. Erinevalt eelmisest vormist kasvab indolentne lümfoom aeglaselt ja annab metastaase. Mõnikord vähihaigused see vorm ei pruugi avalduda aastaid (st mitte põhjustada inimesel seda valu ja muud patoloogia sümptomid). Üldiselt on mitte-Hodgkini lümfoomi õigeaegse ravi korral prognoos siin üsna hea.
- Keskmine. Seda tüüpi haigused algavad aeglaselt, kuid aja jooksul kiirendavad nende tempot, kaldudes rohkem agressiivsete vormide poole.
Arengu põhjused
Siiani ei ole arstid suutnud täpselt tuvastada tegureid, mis provotseerivad mis tahes tüüpi mitte-Hodgkini lümfoomi arengut. Siin tuleks aga arvesse võtta järgmist punkti. Selle päritolu järgi jaguneb haigus järgmisteks osadeks:
- esmane - onkoloogia mõjutab peamiselt lümfoidseid kudesid (iseseisev fookus) ja annab seejärel metastaase teistele organitele;
- sekundaarne - sel juhul toimib see haigus metastaaside kujul, seetõttu võib põhjuseks nimetada pahaloomuliste rakkude olemasolu kehas.

Kui me räägime primaarse lümfoomi põhjustest, on meditsiinis mitmeid tegureid:
- Infektsioonid kehas. C-hepatiidi viirus, HIV-nakkus või inimese herpesviirus (tüüp 8) võivad provotseerida patoloogiliste rakkude ilmumist. Epsteini-Barri viirus põhjustab sageli Burkitti lümfoomi ehk haiguse follikulaarset vormi. Inimestel, kes puutuvad kokku bakteriga Helicobacter pylori (mis põhjustab maohaavandeid), on märkimisväärselt suurem risk haigestuda MALT lümfoomid.
- Mõned geneetilised haigused. Nende hulgas on: ataksia-telangiektaasia sündroom, Chediak-Higashi sündroom, samuti Klinefelteri sündroom.
- Ioniseeritud kiirgus mis tahes annuses.
- Benseenide, insektitsiidide, herbitsiidide ja paljude teiste mutageenide või keemiliste kantserogeenide mõju.
- Autoimmuunse iseloomuga haigused. Tüüpiline näide on reumatoidartriit või süsteemne erütematoosluupus.
- Erinevate immunosupressantide pikaajaline kasutamine.
- Vanusega seotud muutused keha kudedes. Vanusega suureneb mitte-Hodgkini lümfoomi tekkerisk märkimisväärselt. Arsti soovitus selle riski vähendamiseks on regulaarne arstlik läbivaatus. See võimaldab haigust tuvastada varajases staadiumis ja alustage kohe ravi.
- Ülekaaluline.
Samas tuleb märkida, et ühe või mitme teguri olemasolu ülaltoodud loetelust ei tähenda sugugi onkoloogiliste haiguste vältimatut arengut. Need suurendavad ainult selle esinemise ohtu.
Lümfoomide etapid
Kogu onkoloogilise haiguse kulgemise periood jaguneb tavaliselt 4 etapiks (staadiumid) ja lümfoom pole sel juhul erand.
1 etapp. Mitte-Hodgkini lümfoomi selles etapis esindab ühe lümfisõlme kahjustus või ühe sõltumatu fookuse ilmumine. Kohalikke ilminguid pole veel täheldatud.
2. etapp. See etapp hõlmab pahaloomuline kasvaja, mis on levinud kahte või enamasse lümfisõlme ja läks ka lümfisõlmedest kaugemale, kuid on lokaliseeritud ainult diafragma ühel küljel. Seega võib kasvaja levida kas ainult kõhuõõnes või ainult rinnus.
3 etapp. Järgmine arenguetapp on fookuste olemasolu diafragma mõlemal küljel.
4 etapp. Seda lümfoomi arenguetappi peetakse viimaseks. Sel ajal ulatub kahjustus luuüdi, luustiku ja kesknärvisüsteemini. Seda etappi ei peeta asjata patsiendi jaoks viimaseks ja kõige raskemaks. Üks ilmingutest on pidev äge valu mida ei saa enam peatada tavapäraste valuvaigistite abil.

Kliiniline pilt
Mitte-Hodgkini lümfoomi sümptomid on väga mitmekesised ja sõltuvad haiguse vormist ja lokaliseerimisest. Lümfoidkoe pahaloomulise kahjustuse tavaline sümptom on lümfisõlmede suurenemine (sage või lokaalne) ja valu selles piirkonnas. Selle seisundiga kaasnevad teatud organi kahjustuse sümptomid või keha üldise joobeseisundi tunnused.
T-raku vormid avalduvad sageli järgmiselt:
- suurendama;
- esineb põrna suurenemine ja selle töö rikkumine;
- kopsud ja nahk on kahjustatud.
On mitmeid sümptomeid, mis on iseloomulikud mitte-Hodgkini lümfoomidele, kuid puuduvad Hodgkini lümfoomi puhul. Nende hulgas:
- mediastiinumi (rindkere õõnsuse) lümfisõlmede kahjustus, näo turse ja hüperemia (liigne verevool teatud kehaosasse);
- kui tüümuses tekivad pahaloomulised rakud, esineb sageli õhupuudust ja köha;
- provotseerib vaagna- või retroperitoneaalsete lümfisõlmede suurenemine neerupuudulikkus või hüdroonefroos (neerude järkjärguline atroofia).

Samal ajal on võimatu mitte märkida sümptomeid, mis kaasnevad mis tahes onkoloogilise haigusega. Mitte-Hodgkini lümfoomi korral hakkavad need ilmnema haiguse 2. staadiumis ja muutuvad järk-järgult heledamaks:
- tõhususe järsk langus, nõrkuse ja väsimuse ilmnemine;
- söögiisu puudumine;
- kaalukaotus;
- ärrituvuse, apaatia ilmnemine;
- pidev tugev higistamine, peamiselt öösel;
- aneemia tunnused.
Lümfoomide diagnoosimine
Lümfisõlmede suurenemine näitab mitte ainult onkoloogilist haigust, vaid ka infektsiooni esinemist inimkehas. Kui kahtlustatakse nakkuslikku komponenti, määratakse patsiendile ravimtoode mõeldud allika kõrvaldamiseks. Mõne aja pärast korratakse kontrolli. Kui paranemist ei täheldata, rida laboratoorsed uuringud ja instrumentaalsed diagnostilised protseduurid. Mitte-Hodgkini lümfoomi ravi põhimõtted ja meetodid valib arst uuringuandmete põhjal.
- Vereanalüüsid keha seisundi määramiseks ja patoloogia otsimiseks.
- Rindkere röntgen. Selle protseduuri tulemuste kohaselt selgub rindkere lümfisõlmede seisund.
- CT - kompuutertomograafia annab teavet kõigi lümfisõlmede seisundi ja metastaaside võimaliku esinemise kohta teistes elundites.
- MRI. Arstid määravad magnetresonantstomograafia abil seljaaju ja aju hetkeseisundi ning võimaliku pahaloomuliste rakkude olemasolu neis.
- PAT. Selle mõiste alla kuulub diagnostiline protseduur positronemissioontomograafia. Selle käigus süstitakse patsiendi veeni spetsiaalne aine, mis aitab tuvastada kõik sees olevad vähikolded pehmed koed.
- Galliumi skaneerimine. See meetod täiendab tõhusalt PET-i, kuna tuvastab luukoes pahaloomulised rakud.
- Ultraheli annab teavet siseorganite seisundi kohta.
- Biopsia. See diagnoos on kasvajarakkude ekstraheerimine ja nende edasine uurimine laboris. Võib teha biopsia erinevatel viisidel Seetõttu eristatakse sisselõiget, ekstsisiooni, punktsiooni, spinaalpunktsiooni ja luuüdi aspiratsiooni.

Ravi
Igal juhul määratakse ravikuur, võttes arvesse diagnoosi tulemusi. Mõned lümfoomi vormid ei vaja esialgu ravi (sealhulgas aeglase arenguga ja väljendunud sümptomite puudumisega kasvajate tüübid).
Keemiaravi. Mitte-Hodgkini lümfoomi korral on ette nähtud mitu keemiaravi kursust. Terapeutiline toime saavutatakse tugevate vähivastaste ravimite kasutamisega, mis on mõeldud patoloogiliste rakkude kasvu ja paljunemise blokeerimiseks. Kursuste vaheline intervall on umbes 2 või 4 nädalat. Annustamisvorm: intravenoossed lahused või tabletid.

Kiiritusravi. Ravi olemus taandub vähi kasvajale kahjulike ioniseeritud kiirte mõjule inimkehale. Selline mitte-Hodgkini lümfoomi ravi on mõnel juhul peamine, kuid enamasti kombineeritakse seda keemiaraviga.

Kirurgia. Lümfoomide puhul kasutatakse operatsiooni väga harva, selle madala efektiivsuse tõttu. Selle määramine on mõttekas ainult kasvaja piiratud leviku korral.
Immunoteraapia. Mitte-Hodgkini lümfoomi ravi viiakse sageli läbi ravimitega, mis sisaldavad interferooni, monoklonaalseid antikehi ja keemiaravi ravimeid. Selle toime olemus seisneb organismi varustamises nende ainetega, mida inimkeha normaalsetes tingimustes ise toodab. Sellised ravimid vähendavad oluliselt kasvaja suurust, aeglustavad selle kasvu ja suurendavad järsult inimese immuunsust haiguse vastu võitlemisel.
Luuüdi siirdamine. Seda ravimeetodit kasutatakse siis, kui muud tüüpi ravi ei aita. Enne siirdamist läbib patsient suure annuse kiiritus- või keemiaravi. Hilisem siirdamine on vajalik, sest suured kiirgusdoosid või ravimid tapavad mitte ainult vähirakke, vaid ka terveid kudesid. Just luuüdi taastamiseks on ette nähtud siirdamine.
Tähtis! Sellise diagnoosiga enesega ravimine on rangelt keelatud! Mis tahes tüüpi ja laadi lümfoome ei ravita rahvapärased abinõud, selleks on vaja professionaalset lähenemist ja meetmete komplekti kasvaja kõrvaldamiseks.
Prognoos
Nagu näitavad meditsiinistatistika ja meditsiinilised ülevaated, ravitakse mitte-Hodgkini lümfoomi tõhusalt 1. ja 2. arenguetapis. Sel juhul on patsientide elulemus järgmise 5 aasta jooksul umbes 80%. See on haiguse tõsidust arvestades üsna kõrge näitaja. 3. astme onkoloogiaga patsientide ravimisel on elulemus madalam, kuna kasvajal on aega levida fookusest kaugele ja sellega toime tulla on palju raskem. 4. etapis on elulemus madal - ainult 20%.
Arstid rõhutavad eriti, et isegi pidevad arengud ja uuringud selles vallas ei võimalda onkoloogilisi haigusi 100% efektiivsusega ravida. Seetõttu sõltub palju patsiendist endast. Haigussümptomite varajane avastamine ja kliinikusse pöördumine suurendavad oluliselt täieliku paranemise võimalust.