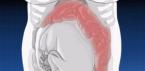
आनुवंशिक विकृति दुर्लभ जन्मजात बीमारियां हैं जिनकी पहले से भविष्यवाणी करना मुश्किल है। वे उस समय भी होते हैं जब भ्रूण का निर्माण होता है। ज्यादातर वे माता-पिता से प्रेषित होते हैं, लेकिन हमेशा ऐसा नहीं होता है। कुछ मामलों में, जीन विकार अपने आप होते हैं। ब्रूटन की बीमारी इन विकृतियों में से एक है। यह प्राथमिक इम्युनोडेफिशिएंसी राज्यों से संबंधित है। यह रोग हाल ही में, 20वीं सदी के मध्य में खोजा गया था। इसलिए, डॉक्टरों द्वारा इसका पूरी तरह से अध्ययन नहीं किया गया है। यह काफी दुर्लभ है, केवल लड़कों में।
ब्रूटन की बीमारी: अध्ययन का इतिहास
यह विकृति एक्स-लिंक्ड क्रोमोसोमल असामान्यताओं को संदर्भित करती है, जो आनुवंशिक स्तर पर प्रसारित होती है। ब्रूटन की बीमारी बिगड़ा हुआ हास्य प्रतिरक्षा द्वारा विशेषता है। मुख्य लक्षण संक्रामक प्रक्रियाओं के लिए संवेदनशीलता है। इस विकृति का पहला उल्लेख 1952 में मिलता है। उस समय, अमेरिकी वैज्ञानिक ब्रूटन ने एक बच्चे के इतिहास का अध्ययन किया, जो 4 साल की उम्र में 10 से अधिक बार बीमार था। के बीच संक्रामक प्रक्रियाएंइस लड़के को सेप्सिस, निमोनिया, मेनिन्जाइटिस, ऊपरी हिस्से की सूजन थी श्वसन तंत्र. बच्चे की जांच करने पर पता चला कि इन बीमारियों के प्रति एंटीबॉडी नहीं थे। दूसरे शब्दों में, संक्रमण के बाद कोई प्रतिरक्षा प्रतिक्रिया नहीं देखी गई। बाद में, 20वीं सदी के अंत में, डॉक्टरों द्वारा ब्रूटन की बीमारी का फिर से अध्ययन किया गया। 1993 में, डॉक्टर एक दोषपूर्ण जीन की पहचान करने में सक्षम थे जो बिगड़ा हुआ प्रतिरक्षा का कारण बनता है।
ब्रूटन रोग के कारण
एग्माग्लोबुलिनमिया (ब्रूटन रोग) अक्सर वंशानुगत होता है। दोष को एक पुनरावर्ती लक्षण माना जाता है, इसलिए विकृति वाले बच्चे के होने की संभावना 25% है। उत्परिवर्ती जीन की वाहक महिलाएं हैं। यह इस तथ्य के कारण है कि दोष एक्स गुणसूत्र पर स्थानीयकृत है। हालांकि, यह बीमारी केवल पुरुषों में ही फैलती है। एग्माग्लोबुलिनमिया का मुख्य कारण एक दोषपूर्ण प्रोटीन है जो जीन एन्कोडिंग टाइरोसिन किनसे का हिस्सा है। इसके अलावा, ब्रूटन की बीमारी अज्ञातहेतुक हो सकती है। इसका मतलब है कि इसके प्रकट होने का कारण स्पष्ट नहीं है। बच्चे के आनुवंशिक कोड को प्रभावित करने वाले जोखिम कारकों में शामिल हैं:
रोग रोगजनन?
रोग के विकास का तंत्र एक दोषपूर्ण प्रोटीन से जुड़ा है। आम तौर पर, टाइरोसिन किनसे को एन्कोडिंग के लिए जिम्मेदार जीन बी-लिम्फोसाइटों के निर्माण में शामिल होता है। वे प्रतिरक्षा कोशिकाएं हैं जो शरीर की हास्य रक्षा के लिए जिम्मेदार हैं। टाइरोसिन किनसे की विफलता के कारण, बी-लिम्फोसाइट्स पूरी तरह से परिपक्व नहीं होते हैं। नतीजतन, वे इम्युनोग्लोबुलिन - एंटीबॉडी का उत्पादन करने में सक्षम नहीं हैं। ब्रूटन रोग का रोगजनन हास्य संरक्षण का पूर्ण अवरोध है। नतीजतन, जब संक्रामक एजेंट शरीर में प्रवेश करते हैं, तो उनके प्रति एंटीबॉडी का उत्पादन नहीं होता है। इस बीमारी की एक विशेषता यह है कि बी-लिम्फोसाइटों की अनुपस्थिति के बावजूद, प्रतिरक्षा प्रणाली वायरस से लड़ने में सक्षम है। हास्य संरक्षण के उल्लंघन की प्रकृति दोष की गंभीरता पर निर्भर करती है।
ब्रूटन रोग: विकृति विज्ञान के लक्षण
पैथोलॉजी सबसे पहले खुद को शैशवावस्था में महसूस करती है। सबसे अधिक बार, रोग जीवन के 3-4 वें महीने से पहले ही प्रकट हो जाता है। यह इस तथ्य के कारण है कि इस उम्र में बच्चे का शरीर मातृ एंटीबॉडी की रक्षा करना बंद कर देता है। पैथोलॉजी के पहले लक्षण टीकाकरण के बाद एक दर्दनाक प्रतिक्रिया हो सकते हैं, त्वचा के चकत्ते, ऊपरी और निचले श्वसन पथ के संक्रमण। बहरहाल स्तन पिलानेवालीबच्चे की रक्षा करता है भड़काऊ प्रक्रियाएंक्योंकि मां के दूध में इम्युनोग्लोबुलिन होता है। ब्रूटन की बीमारी लगभग 4 साल की उम्र तक प्रकट होती है। इस समय, बच्चा अन्य बच्चों के साथ संपर्क करना शुरू कर देता है, भाग लेता है बाल विहार. संक्रामक घावों में, मेनिंगो-, स्ट्रेप्टो- और स्टेफिलोकोकल माइक्रोफ्लोरा प्रमुख हैं। नतीजतन, बच्चों को शुद्ध सूजन के अधीन किया जा सकता है। सबसे आम बीमारियों में निमोनिया, साइनसाइटिस, ओटिटिस मीडिया, साइनसिसिस, मेनिन्जाइटिस, नेत्रश्लेष्मलाशोथ शामिल हैं। असामयिक उपचार के साथ, ये सभी प्रक्रियाएं सेप्सिस में बदल सकती हैं। साथ ही, ब्रूटन रोग की अभिव्यक्ति त्वचा संबंधी विकृति हो सकती है। कम प्रतिरक्षा प्रतिक्रिया के कारण, घाव और खरोंच के स्थान पर सूक्ष्मजीव तेजी से गुणा करते हैं। इसके अलावा, रोग की अभिव्यक्तियों में ब्रोन्किइक्टेसिस शामिल हैं - फेफड़ों में रोग परिवर्तन। लक्षण हैं सांस की तकलीफ, सीने में दर्द, कभी-कभी हेमोप्टाइसिस। पाचन अंगों में भड़काऊ फॉसी की उपस्थिति भी संभव है, मूत्र तंत्र, श्लेष्मा झिल्ली पर। जोड़ों में सूजन और दर्द समय-समय पर देखा जाता है।
रोग के लिए नैदानिक मानदंड
पहले नैदानिक मानदंड में लगातार रुग्णता शामिल होनी चाहिए। ब्रूटन की बीमारी से पीड़ित बच्चे प्रति वर्ष 10 से अधिक संक्रमणों के साथ-साथ महीने के दौरान कई बार पीड़ित होते हैं। रोग एक दूसरे को दोहरा सकते हैं या बदल सकते हैं (ओटिटिस मीडिया, टॉन्सिलिटिस, निमोनिया)। ग्रसनी की जांच करते समय, टॉन्सिल की अतिवृद्धि नहीं होती है। यही बात परिधीय लिम्फ नोड्स के तालमेल पर भी लागू होती है। आपको टीकाकरण के बाद बच्चे की प्रतिक्रिया पर भी ध्यान देना चाहिए। में महत्वपूर्ण परिवर्तन देखे गए हैं प्रयोगशाला परीक्षण. केएलए में, एक भड़काऊ प्रतिक्रिया (ल्यूकोसाइट्स की संख्या में वृद्धि, त्वरित ईएसआर) के संकेत हैं। इसी समय, प्रतिरक्षा कोशिकाओं की संख्या कम हो जाती है। यह ल्यूकोसाइट सूत्र में परिलक्षित होता है: लिम्फोसाइटों की एक छोटी संख्या और बढ़ी हुई सामग्रीन्यूट्रोफिल। एक महत्वपूर्ण अध्ययन इम्युनोग्राम है। यह एंटीबॉडी की कमी या अनुपस्थिति को दर्शाता है। यह संकेत आपको निदान करने की अनुमति देता है। यदि डॉक्टर को संदेह है, तो आनुवंशिक परीक्षण किया जा सकता है।
ब्रूटन रोग और समान विकृति के बीच अंतर
यह विकृति अन्य प्राथमिक और माध्यमिक इम्युनोडेफिशिएंसी से अलग है। इनमें स्विस-टाइप एग्माग्लोबुलिनमिया, डिजॉर्ज सिंड्रोम, एचआईवी शामिल हैं। इन विकृति के विपरीत, ब्रूटन की बीमारी को केवल हास्य प्रतिरक्षा के उल्लंघन की विशेषता है। यह इस तथ्य से प्रकट होता है कि शरीर वायरल एजेंटों से लड़ने में सक्षम है। यह कारक स्विस-प्रकार के एग्माग्लोबुलिनमिया से अलग है, जिसमें हास्य और सेलुलर प्रतिरक्षा प्रतिक्रिया दोनों बिगड़ा हुआ है। व्यतीत करना क्रमानुसार रोग का निदानडिजॉर्ज सिंड्रोम के साथ, एक एक्स-रे आवश्यक है छाती(थाइमस अप्लासिया) और कैल्शियम की मात्रा निर्धारित करें। एचआईवी संक्रमण को बाहर करने के लिए, लिम्फ नोड्स का तालमेल, एलिसा किया जाता है।
एग्माग्लोबुलिनमिया के उपचार के तरीके
दुर्भाग्य से, ब्रूटन की बीमारी को पूरी तरह से हराना असंभव है। एग्माग्लोबुलिनमिया के उपचार के तरीकों में प्रतिस्थापन और रोगसूचक उपचार शामिल हैं। मुख्य लक्ष्य हासिल करना है सामान्य स्तररक्त में इम्युनोग्लोबुलिन। एंटीबॉडी की मात्रा 3 ग्राम/ली के करीब होनी चाहिए। इसके लिए शरीर के वजन के 400 मिलीग्राम/किलोग्राम की दर से गामा ग्लोब्युलिन का उपयोग किया जाता है। तीव्र संक्रामक रोगों के दौरान एंटीबॉडी की सांद्रता बढ़ाई जानी चाहिए, क्योंकि शरीर अपने आप उनका सामना नहीं कर सकता है। इसके अलावा, रोगसूचक उपचार किया जाता है। सबसे अधिक बार निर्धारित जीवाणुरोधी दवाएं"सेफ्ट्रिएक्सोन", "पेनिसिलिन", "सिप्रोफ्लोक्सासिन"। त्वचा की अभिव्यक्तियों के लिए स्थानीय उपचार. श्लेष्म झिल्ली को एंटीसेप्टिक समाधान (गले और नाक की सिंचाई) के साथ धोने की भी सिफारिश की जाती है।
ब्रूटन के एग्माग्लोबुलिनमिया के लिए पूर्वानुमान
आजीवन प्रतिस्थापन चिकित्सा के बावजूद, एग्माग्लोबुलिनमिया के लिए रोग का निदान अनुकूल है। संक्रामक प्रक्रियाओं का निरंतर उपचार और रोकथाम घटनाओं को कम करता है। रोगी आमतौर पर सक्षम और सक्रिय रहते हैं। उपचार के लिए गलत दृष्टिकोण के साथ, जटिलताएं सेप्सिस तक विकसित हो सकती हैं। उन्नत संक्रमण के मामले में, रोग का निदान खराब है।
ब्रूटन रोग की रोकथाम
रिश्तेदारों में विकृति या इसके संदेह की उपस्थिति में, गर्भावस्था के पहले तिमाही के दौरान एक आनुवंशिक परीक्षा आयोजित करना आवश्यक है। इसके अलावा, निवारक उपायों में हवा के संपर्क में आना, पुराने संक्रमणों की अनुपस्थिति और शामिल होना चाहिए हानिकारक प्रभाव. गर्भावस्था के दौरान, तनाव को contraindicated है। माध्यमिक रोकथाम में विटामिन थेरेपी, गामा ग्लोब्युलिन की शुरूआत, स्वस्थ जीवन शैलीजिंदगी। संक्रमित लोगों के संपर्क में आने से बचना भी जरूरी है।
ब्रूटन की बीमारी, या ब्रूटन का एग्माग्लोबुलिनमिया, एक वंशानुगत इम्युनोडेफिशिएंसी है जो ब्रूटन के टाइरोसिन किनसे जीन एन्कोडिंग में उत्परिवर्तन के कारण होता है। इस रोग का वर्णन सबसे पहले 1952 में ब्रूटन ने किया था, जिसके नाम पर दोषपूर्ण जीन का नाम रखा गया था। ब्रूटन के टाइरोसिन किनेसेस परिपक्व बी कोशिकाओं के विभेदन के लिए पूर्व-बी कोशिकाओं की परिपक्वता में महत्वपूर्ण हैं। Bruton tyrosine kinase जीन Xq21.3 से Xq22 तक बैंड में X गुणसूत्र की लंबी भुजा पर पाया गया था; इसमें 19 एक्सॉन के साथ 37.5 किलोबेस होते हैं जो 659 अमीनो एसिड को एनकोड करते हैं; ये अमीनो एसिड हैं जो साइटोसोलिक के गठन को पूरा करते हैं टाइरोसिन किनसे। इस जीन में, 341 अद्वितीय आणविक घटनाएं पहले ही दर्ज की जा चुकी हैं। उत्परिवर्तन के अलावा, बड़ी संख्या में प्रकार या बहुरूपता पाए गए हैं।
एगामाग्लोबुलिनमिया ब्रूटन। कारण
जीन में उत्परिवर्तन जो ब्रूटन की बीमारी के अंतर्गत आते हैं, बी-लिम्फोसाइटों और उनकी संतानों के विकास और कार्य में हस्तक्षेप करते हैं। मूल विचार यह है कि एक स्वस्थ व्यक्ति में, प्री-बी कोशिकाएं लिम्फोसाइटों में परिपक्व होती हैं। और इस रोग से ग्रसित लोगों में प्री-बी सेल्स या तो कम संख्या में होते हैं, या उन्हें कार्यक्षमता में समस्या हो सकती है।
एगामाग्लोबुलिनमिया ब्रूटन। pathophysiology
एक सामान्य प्रोटीन की अनुपस्थिति में, बी-लिम्फोसाइट्स अंतर नहीं करते हैं या पूरी तरह से परिपक्व नहीं होते हैं। परिपक्व बी-लिम्फोसाइटों के बिना, एंटीबॉडी-उत्पादक प्लाज्मा कोशिकाएं भी अनुपस्थित होंगी। नतीजतन, रेटिकुलोएन्डोथेलियल और लिम्फोइड अंग जिनमें ये कोशिकाएं बढ़ती हैं, अंतर करती हैं, और स्टोर खराब विकसित होती हैं। प्लीहा, टॉन्सिल, एडेनोइड्स, आंतों और परिधीय लिम्फ नोड्स सभी आकार में कम हो सकते हैं या एक्स-लिंक्ड एग्माग्लोबुलिनमिया वाले व्यक्तियों में पूरी तरह से अनुपस्थित हो सकते हैं।
प्रत्येक जीन क्षेत्र में उत्परिवर्तन इस बीमारी को जन्म दे सकता है। सबसे आम आनुवंशिक घटना मिसाइल उत्परिवर्तन है। अधिकांश उत्परिवर्तन के परिणामस्वरूप प्रोटीन काट-छाँट होता है। ये उत्परिवर्तन साइटोप्लाज्मिक प्रोटीन में महत्वपूर्ण अवशेषों को प्रभावित करते हैं और अत्यधिक परिवर्तनशील और समान रूप से पूरे अणु में वितरित होते हैं। हालाँकि, विशिष्ट उत्परिवर्तन का उपयोग करके रोग की गंभीरता का अनुमान नहीं लगाया जा सकता है। लगभग एक तिहाई बिंदु उत्परिवर्तन सीजीजी साइटों को प्रभावित करते हैं, जिनमें आमतौर पर आर्गिनिन अवशेषों के लिए कोड होता है।
यह महत्वपूर्ण प्रोटीन बी-लिम्फोसाइटों के प्रसार और विभेदन के लिए आवश्यक है। प्रोटीन असामान्यताओं वाले पुरुषों में पूर्ण या लगभग पूर्ण अनुपस्थितिप्लाज्मा कोशिकाओं में लिम्फोसाइट्स।
एगामाग्लोबुलिनमिया ब्रूटन। लक्षण और अभिव्यक्तियाँ
आवर्तक संक्रमण बचपन में शुरू होता है और पूरे वयस्कता में बना रहता है।
ब्रूटन रोग या ब्रूटन के एग्माग्लोबुलिनमिया की सबसे आम अभिव्यक्ति है, हीमोफिलस इन्फ्लुएंजा संक्रमण, और कुछ स्यूडोमोनास प्रजातियों जैसे इनकैप्सुलेटेड प्यूरुलेंट बैक्टीरिया के लिए संवेदनशीलता में वृद्धि। रोग के रोगियों में त्वचा संक्रमण मुख्य रूप से समूह ए स्ट्रेप्टोकोकी और स्टेफिलोकोसी के कारण होता है, और यह इम्पेटिगो, सेल्युलाइटिस, फोड़े या फोड़े के रूप में उपस्थित हो सकता है।
एक्जिमा का एक रूप जो एटोपिक जिल्द की सूजन जैसा दिखता है, स्पष्ट हो सकता है, साथ ही पायोडर्मा गैंग्रीनोसम, विटिलिगो, एलोपेसिया और स्टीवंस-जॉनसन सिंड्रोम (नशीली दवाओं के उपयोग में वृद्धि के कारण) के मामलों में वृद्धि के साथ। अन्य संक्रमण जो आमतौर पर इस बीमारी के साथ मौजूद होते हैं उनमें शामिल हैं: एंटरोवायरल संक्रमण, सेप्सिस, मेनिन्जाइटिस और बैक्टीरियल डायरिया। मरीजों को ऑटोइम्यून रोग, थ्रोम्बोसाइटोपेनिया, न्यूट्रोपेनिया भी हो सकता है। हीमोलिटिक अरक्ततातथा रूमेटाइड गठिया. लगातार एंटरोवायरस संक्रमण बहुत कम ही घातक एन्सेफलाइटिस या डर्माटोमायोसिटिस-मेनिंगोएन्सेफलाइटिस सिंड्रोम का कारण बनता है। न्यूरोलॉजिकल परिवर्तनों के अलावा, इस सिंड्रोम के नैदानिक अभिव्यक्तियों में एडिमा और एक्स्टेंसर जोड़ों पर त्वचा पर एक एरिथेमेटस दाने शामिल हैं।
नर असामान्य रूप से गंभीर और/या रुक-रुक कर विकसित हो सकते हैं मध्यकर्णशोथऔर निमोनिया। सबसे आम रोगज़नक़ एस निमोनिया है, इसके बाद इन्फ्लूएंजा बी वायरस, स्टेफिलोकोसी, मेनिंगोकोकी और मोरैक्सेला कैटरलिस है।
12 साल से कम उम्र के बच्चों में, विशिष्ट संक्रमण इनकैप्सुलेटेड बैक्टीरिया के कारण होते हैं। इस आयु वर्ग में आम संक्रमणों में बार-बार होने वाला निमोनिया, साइनसाइटिस और एस निमोनिया और इन्फ्लूएंजा बी वायरस के कारण होने वाले ओटिटिस मीडिया शामिल हैं, जिनका इस उम्र में इलाज करना मुश्किल है।
वयस्कता में, त्वचा की अभिव्यक्तियाँअधिक सामान्य हो जाते हैं, आमतौर पर स्टेफिलोकोकस ऑरियस और समूह ए स्ट्रेप्टोकोकस के कारण। ओटिटिस मीडिया द्वारा प्रतिस्थापित किया जाता है पुरानी साइनसाइटिस, और फेफड़ों की बीमारी एक निरंतर समस्या बन जाती है, दोनों एक प्रतिबंधात्मक रूप में और एक अवरोधक रूप में।
शिशुओं और वयस्कों दोनों को ऑटोइम्यून रोग हो सकते हैं। आमतौर पर, इन विकारों में गठिया, ऑटोइम्यून हेमोलिटिक एनीमिया, ऑटोइम्यून थ्रोम्बोसाइटोपेनिया, ऑटोइम्यून न्यूट्रोपेनिया और सूजन आंत्र रोग शामिल हैं। सूजन आंत्र रोग को नियंत्रित करना बहुत मुश्किल हो सकता है और अक्सर पुराने वजन घटाने और कुपोषण में योगदान देता है। अतिसार आम है और जिआर्डिया या कैम्पिलोबैक्टर प्रजातियों के कारण होता है। मरीजों को एंटरो होने का खतरा होता है विषाणु संक्रमणपोलियोवायरस सहित।
शारीरिक जाँच
ब्रूटन के एग्माग्लोबुलिनमिया वाले पुरुष शिशु शारीरिक रूप से बिना बीमारी के पुरुष शिशुओं की तुलना में छोटे हो सकते हैं, जो कि बार-बार होने वाले संक्रमण से अवरुद्ध विकास और विकास के कारण होता है।
परीक्षा पर लिम्फ नोड्स, टॉन्सिल और अन्य लिम्फोइड ऊतक बहुत छोटे या पूरी तरह से अनुपस्थित हो सकते हैं।
रोग का निदान तब होता है जब बच्चा बार-बार किसकी उपस्थिति में बीमार हो जाता है विभिन्न संक्रमणओटिटिस या स्टेफिलोकोकल त्वचा संक्रमण और नेत्रश्लेष्मलाशोथ जो एंटीबायोटिक चिकित्सा का जवाब नहीं देते हैं। ये गंभीर संक्रमण न्यूट्रोपेनिया से जुड़े हो सकते हैं।
पायोडर्मा गैंग्रीनोसम, जैसे अल्सर और सेल्युलाइटिस निचला सिराकुछ रोगियों में भी विचार किया जा सकता है।
एगामाग्लोबुलिनमिया ब्रूटन। निदान
प्रणालीगत और फुफ्फुसीय संक्रमण से प्रारंभिक रुग्णता और मृत्यु को रोकने के लिए प्रारंभिक पहचान और निदान आवश्यक है। निदान की पुष्टि असामान्य रूप से निम्न स्तर या कोई परिपक्व बी लिम्फोसाइट्स नहीं है, और लिम्फोसाइट सतह पर कम या कोई μ भारी श्रृंखला अभिव्यक्ति नहीं है। दूसरी ओर, टी-लिम्फोसाइटों का स्तर ऊंचा हो जाएगा। रोग का अंतिम निर्धारक आणविक विश्लेषण है। प्रसवपूर्व निदान के लिए आणविक विश्लेषण का भी उपयोग किया जाता है, जो कोरियोनिक विलस सैंपलिंग या एमनियोसेंटेसिस के साथ किया जा सकता है जब मां को दोषपूर्ण जीन के वाहक के रूप में जाना जाता है। 100 मिलीग्राम / डीएल से कम आईजीजी स्तर निदान का समर्थन करते हैं।
शायद ही, वयस्कों में उनके जीवन के दूसरे दशक में निदान किया जा सकता है। ऐसा माना जाता है कि इसकी पूर्ण अनुपस्थिति के बजाय प्रोटीन में उत्परिवर्तन के कारण होता है।
प्रयोगशाला परीक्षण
पहला कदम आईजीजी, आईजीएम, इम्युनोग्लोबुलिन ई (आईजीई), और इम्युनोग्लोबुलिन ए (आईजीए) की मात्रा निर्धारित करना है। आईजीजी के स्तर को पहले मापा जाना चाहिए, अधिमानतः 6 महीने की उम्र के बाद जब मातृ आईजीजी के स्तर में गिरावट शुरू हो जाती है। दूसरा, 100 mg/dL से नीचे का IgG स्तर आमतौर पर ब्रूटन रोग का संकेत होता है। एक नियम के रूप में, IgM और IgA का पता नहीं लगाया जाता है।
एक बार एंटीबॉडी स्तर असामान्य रूप से कम होने के लिए निर्धारित किया गया है, निदान की पुष्टि बी-लिम्फोसाइट और टी-लिम्फोसाइट मार्करों के विश्लेषण से प्राप्त की जाएगी। CD19+ B सेल का स्तर 100 mg/dL से नीचे। टी सेल परख मूल्य (सीडी 4+ और सीडी 8+) में वृद्धि होती है।
टी-आश्रित और टी-स्वतंत्र प्रतिजनों के लिए आईजीजी प्रतिक्रियाओं का पता लगाकर, टीकाकरण द्वारा आगे का विश्लेषण किया जा सकता है, उदाहरण के लिए असंबद्ध 23-वैलेंट न्यूमोकोकल या डिप्थीरिया, टेटनस और एच इन्फ्लूएंजा टाइप बी टीकों के प्रशासन के बाद।
आणविक आनुवंशिक परीक्षण जन्मजात agammaglobulinemia के निदान की एक प्रारंभिक पुष्टि स्थापित कर सकता है।
अन्य परीक्षण
फेफड़े की बीमारी की निगरानी के लिए फेफड़े के कार्य अध्ययन केंद्रीय हैं। उन्हें सालाना उन बच्चों में किया जाना चाहिए जो परीक्षण कर सकते हैं (आमतौर पर 5 साल की उम्र से)।
प्रक्रियाओं
सीमा और प्रगति का आकलन करने के लिए एंडोस्कोपी और कोलोनोस्कोपी का उपयोग किया जा सकता है सूजन की बीमारीआंत ब्रोंकोस्कोपी पुरानी फेफड़ों की बीमारी और संक्रमण के निदान और ट्रैकिंग में सहायक हो सकती है।
एगामाग्लोबुलिनमिया ब्रूटन। इलाज
इस बीमारी का कोई इलाज नहीं है। इम्युनोग्लोबुलिन की शुरूआत रोग को नियंत्रित करने का मुख्य तरीका है। 400-600 मिलीग्राम/किलोग्राम/माह की विशिष्ट खुराक हर 3-4 सप्ताह में दी जानी चाहिए। व्यक्तिगत नैदानिक प्रतिक्रियाओं के आधार पर खुराक और अंतराल को समायोजित किया जा सकता है। थेरेपी 10-12 सप्ताह की उम्र से शुरू होनी चाहिए। आईजीजी के साथ थेरेपी 500-800 मिलीग्राम / डीएल के न्यूनतम स्तर से शुरू होनी चाहिए। थेरेपी 10-12 सप्ताह की उम्र से शुरू होनी चाहिए।
Ceftriaxone का उपयोग पुराने संक्रमण, निमोनिया या सेप्सिस के इलाज के लिए किया जा सकता है। यदि संभव हो तो, चिकित्सकों को एंटीबायोटिक संवेदनशीलता संस्कृतियां प्राप्त करनी चाहिए, क्योंकि कई जीव पहले से ही कई एंटीबायोटिक दवाओं के लिए प्रतिरोध दिखा रहे हैं। स्ट्रेप संक्रमण, विशेष रूप से, सीफ्रीट्रैक्सोन, सेफोटैक्सिम या वैनकोमाइसिन की आवश्यकता हो सकती है।
ब्रोन्कोडायलेटर्स, स्टेरॉयड इनहेलर, और नियमित फेफड़े के कार्य परीक्षण (वर्ष में कम से कम 3-4 बार) एंटीबायोटिक दवाओं के अलावा चिकित्सा का एक आवश्यक हिस्सा हो सकते हैं।
जीर्ण त्वचा संबंधी अभिव्यक्तियाँ ऐटोपिक डरमैटिटिसऔर एक्जिमा को विशेष लोशन और स्टेरॉयड के साथ त्वचा के दैनिक मॉइस्चराइजिंग द्वारा नियंत्रित किया जाता है।
शल्य चिकित्सा
सर्जरी गंभीर तक सीमित हो सकती है तीव्र संक्रमण. सबसे आम प्रक्रियाओं में वे शामिल हैं जिनका उपयोग आवर्तक ओटिटिस मीडिया वाले रोगियों और क्रोनिक साइनसिसिस वाले रोगियों के इलाज के लिए किया जाता है।
एगामाग्लोबुलिनमिया ब्रूटन। जटिलताओं
जटिलताओं में शामिल हैं जीर्ण संक्रमण, केंद्र के एंटरोवायरस संक्रमण तंत्रिका प्रणाली, विकास की आवृत्ति में वृद्धि स्व - प्रतिरक्षित रोगसाथ ही त्वचा में संक्रमण। मरीजों के पास है बढ़ा हुआ खतरालिम्फोमा का विकास।
एगामाग्लोबुलिनमिया ब्रूटन। भविष्यवाणी
अधिकांश रोगी अपने जीवन के चौथे दशक के अंत तक जीवित रह सकते हैं। जब तक रोगियों का निदान किया जाता है और नियमित अंतःशिरा गामा ग्लोब्युलिन थेरेपी के साथ जल्दी इलाज किया जाता है, तब तक रोग का निदान अच्छा होता है।
गंभीर एंटरोवायरस संक्रमण और पुरानी फेफड़ों की बीमारी अक्सर वयस्कता में घातक होती है।
डंकन (डंकन) सिंड्रोम एक इम्युनोडेफिशिएंसी है जो एपस्टीन-बार वायरस के प्रति अतिसंवेदनशीलता की विशेषता है। वायरस के प्रति संवेदनशीलता में वृद्धि के लिए जीन को एक्स गुणसूत्र पर स्थानीयकृत किया जाता है, रोग की विरासत का प्रकार पुनरावर्ती होता है, इसलिए लड़के बीमार हो जाते हैं। जिन रोगियों को संक्रामक मोनोन्यूक्लिओसिस हुआ है, वे लंबे समय तक ज्वर की स्थिति, लिम्फैडेनोपैथी (बढ़े हुए लिम्फ नोड्स), परिधीय रक्त लिम्फोसाइटोसिस, हेपेटो- और स्प्लेनोमेगाली विकसित करते हैं। बाद में, बी-सेल लिंफोमा विकसित होता है, अधिक बार टर्मिनल वर्गों में। छोटी आंतजिससे बीमार लोगों की मौत हो जाती है। घातक परिणाम एपस्टीन-बार वायरस के कारण होने वाले विनाशकारी हेपेटाइटिस के कारण भी होते हैं।
प्यूरीन न्यूक्लियोसाइड फॉस्फोराइलेज की कमी।
प्यूरीन न्यूक्लियोसाइड फॉस्फोराइलेज (पीएनपी) की कमी एक ऑटोसोमल रिसेसिव तरीके से विरासत में मिली है। बच्चे हाइपोप्लास्टिक एनीमिया और बेहद कम टी-सेल फ़ंक्शन से पीड़ित हैं।
ओरोटासिड्यूरिया।
ओरोटासिड्यूरिया - वंशानुगत रोगपाइरीमिडीन का संश्लेषण, जो मूत्र में ऑरोटिक एसिड (ओरोटेट) के बढ़े हुए उत्सर्जन, टी-लिम्फोसाइटों की अपर्याप्तता, मेगालोब्लास्टिक एनीमिया और मानसिक और शारीरिक मंदता से प्रकट होता है। इस रोग में ओरोटिडाइल पाइरोफॉस्फोरीलेस और ओरोटिडाइल डिकार्बोक्सिलेज एंजाइम की गतिविधि कम हो जाती है, जो ऑरोटिक एसिड को न्यूक्लियोटाइड-ऑरोटीडीन मोनोफॉस्फेट में बदल देती है, जो न्यूक्लिक एसिड के संश्लेषण के लिए आवश्यक है।
बायोटिन-निर्भर फेरमेंटोपैथी।
बायोटिन-आश्रित फेरमेंटोपैथी भी सेलुलर इम्युनोडेफिशिएंसी (बायोटिनिडेज़ में वंशानुगत दोष और बायोटिन-आश्रित एंजाइम पाइरूवेट कार्बोक्सिलेज़ और प्रोपियोनेट कार्बोक्सिलेज़ में शाखित श्रृंखला अमीनो एसिड - वेलिन, ल्यूसीन, आइसोल्यूसीन) के चयापचय में शामिल है। रोग पहले से ही नवजात अवधि में केटोएसिडोसिस, न्यूरोलॉजिकल लक्षण, खालित्य, त्वचा पर चकत्ते और प्रोटीन असहिष्णुता (उल्टी, खराब पाचन, निर्जलीकरण) के एपिसोड के साथ प्रकट होता है। मूत्र में बड़ी मात्रा में कार्बनिक अम्ल होते हैं। बच्चे शारीरिक विकास में पिछड़ रहे हैं। संक्रामक प्रक्रियाओं में से, कैंडिडिआसिस और केराटोकोनजिक्टिवाइटिस सबसे अधिक बार विकसित होते हैं। बायोटिन एक अच्छा चिकित्सीय प्रभाव देता है।
हास्य प्रतिरक्षा की प्राथमिक कमी।
प्राथमिक हास्य प्रतिरक्षा कमियों में निम्नलिखित मुख्य सिंड्रोम शामिल हैं:
ब्रूटन सिंड्रोम (ब्रूटन का प्रकार एग्माग्लोबुलिनमिया)
वेस्ट सिंड्रोम (IgA की कमी)
आईजीजी की कमी
ट्रांसकोबालामिन II की कमी
हाइपर आईजीएम सिंड्रोम
हाइपर-आईजीई सिंड्रोम (जॉब सिंड्रोम, स्टैफिलोकोकस ऑरियस सिंड्रोम हाइपर-आईजीई के साथ)
हाइपर-आईजीडी सिंड्रोम (वैन डेर मीर सिंड्रोम)
देर से प्रतिरक्षा शुरू।
ब्रूटन सिंड्रोम और देर से प्रतिरक्षा शुरू होने के अपवाद के साथ, ह्यूमर इम्युनिटी की वंशानुगत कमियों को सामान्य शब्द के तहत जोड़ा जाता है डिसगैमाग्लोबुलिनमिया. डिस्गैमाग्लोबुलिनमिया के कुछ रूपों में, रक्त में इम्युनोग्लोबुलिन का एक सामान्य या ऊंचा स्तर और श्लेष्म झिल्ली के स्राव का निर्धारण किया जाता है।
ब्रूटन सिंड्रोम।
ब्रूटन सिंड्रोम (ब्रुटन का प्रकार एग्माग्लोबुलिनमिया) सभी वर्गों के इम्युनोग्लोबुलिन की कमी है। रोग एक वंशानुगत प्रकृति (ओ जी ब्रूटन, 1952) की पहली अध्ययन की गई प्रतिरक्षाविहीनता थी। वंशानुक्रम का प्रकार पुनरावर्ती होता है, जो X गुणसूत्र से जुड़ा होता है। जीवन के पहले वर्षों में, संक्रामक जटिलताएं विकसित होती हैं, मुख्यतः जीवाणु। इसी समय, रोगियों में वायरल संक्रमण, एक नियम के रूप में, आसानी से होता है। इम्युनोडेफिशिएंसी के पहले लक्षण जीवन के दूसरे वर्ष में ध्यान देने योग्य हो जाते हैं, हालांकि 8 महीने के शिशु और 3 साल के बच्चे दोनों में बार-बार संक्रमण हो सकता है। लगभग एक तिहाई रोगियों में सुस्त गठिया विकसित होता है, रुमेटीइड गठिया के समान, बड़े जोड़ों में से एक की गुहा में एक बाँझ प्रवाह के साथ।
इस घटना में कि बार-बार संक्रमण से पहले प्रतिस्थापन चिकित्सा (इम्यूनोग्लोबुलिन की तैयारी का प्रशासन) शुरू हो जाती है, गंभीर रूपात्मक परिवर्तन (उदाहरण के लिए, ब्रोन्किइक्टेसिस, क्रोनिक निमोनिया और श्वसन विफलता) का कारण बनता है, तत्काल रोग का निदान बहुत अच्छा है। हालांकि, किशोरावस्था और किशोरावस्था में, एक धीरे-धीरे प्रगतिशील तंत्रिका संबंधी रोग अक्सर विकसित होता है, एक धीमी गति से वायरल संक्रमण जैसा दिखता है और गंभीर एडिमा और पेरिवास्कुलर लिम्फोहिस्टियोप्लास्मोसाइटिक घुसपैठ के साथ एक डर्माटोमायोसिटिस-जैसे सिंड्रोम के रूप में प्रकट होता है। यह गंभीर प्रणालीगत रोग घातक है। ऐसा माना जाता है कि यह एंटरोवायरस संक्रमण के कारण होता है (एंटरोवायरस को बार-बार रोगियों और मृतकों के रक्त और मस्तिष्कमेरु द्रव से अलग किया जाता है)। सामान्य तौर पर, इन रोगियों की एंटरोवायरस के प्रति उच्च संवेदनशीलता पर ध्यान दिया जाना चाहिए। इसलिए, ब्रूटन सिंड्रोम वाले बच्चों में पोलियो होने की संभावना अधिक होती है, और यह उनके लिए अधिक गंभीर होता है।
ब्रूटन की बीमारी एक दुर्लभ घटना है, लेकिन फिर भी होती है। यह रोग एक आनुवंशिक प्रवृत्ति पर आधारित है, यानी शरीर में एंटीबॉडी के उत्पादन में कमी के साथ जो वायरस का विरोध कर सकते हैं।
पैथोलॉजी के बारे में थोड़ा
यह विकृति एक इम्युनोडेफिशिएंसी विरासत में मिली है और ब्रूटन के टाइरोसिन किनसे या इंट्रासेल्युलर सिग्नल एक्सचेंज को एन्कोडिंग के लिए जीन में उत्परिवर्तनीय परिवर्तनों के कारण होती है। पिछली शताब्दी के वर्ष 52 में एक बार एक वैज्ञानिक द्वारा इस रोग को सही ढंग से तैयार किया गया था, और उसी के नाम पर जीन का नाम रखा गया था।
अणु अंतरकोशिकीय स्तर पर परिपक्वता और ऊर्जा विनिमय में शामिल होते हैं। जीन एक्स गुणसूत्र पर पाया गया था, जो टाइरोसिन किनसे के अंतिम गठन के लिए आवश्यक 500 से अधिक अमीनो एसिड को कूटबद्ध करता है।
रोग में पारस्परिक परिवर्तन बी-लिम्फोसाइटों को भविष्य में विकसित और कार्य करने की अनुमति नहीं देते हैं, जिसका उद्देश्य एंटीबॉडी और स्मृति कोशिकाओं का उत्पादन है। एक स्वस्थ व्यक्ति की पहचान इस तथ्य से होती है कि ये कोशिकाएं बी-लिम्फोसाइटों में विकसित होती हैं, जबकि बीमार लोगों में इनकी संख्या कम होती है और वे कम सक्रिय होते हैं।
इस विकृति वाले रोगियों में प्लीहा, एडेनोइड्स, आंतों, लिम्फ नोड्स और टॉन्सिल जैसे अंगों के छोटे आकार के पैरामीटर होते हैं या पूरी तरह से अनुपस्थित हो सकते हैं। हाइपोगैमाग्लोबुलिनमिया - यह विकृति एंटीबॉडी के आकार और संख्या में कमी के संबंध में बी-लिम्फोसाइट कोशिकाओं की कमी के कारण होती है।

रोग के लक्षण
इस बीमारी को भड़काने वाले संक्रमण कम उम्र में अपना विकास शुरू कर सकते हैं और जीवन भर एक ही स्तर पर बने रह सकते हैं। ब्रूटन का एग्माग्लोबुलिनमिया वायरल रोगों के लिए शरीर की भेद्यता में प्रकट होता है, जिसमें प्युलुलेंट भड़काऊ प्रक्रियाएं, हीमोफिलिया और स्यूडोमोनास एरुगिनोसा शामिल हैं।
समूह ए स्ट्रेप्टोकोकी और स्टेफिलोकोसी द्वारा त्वचा के घावों को उकसाया जाता है। एपिडर्मिस पर प्रकट होना एक फोड़ा, फुरुनकल और सेल्युलाइटिस के रूप में हो सकता है। एक्जिमा एलर्जी त्वचा पर चकत्ते जैसा दिखता है।
अन्य संक्रामक रोगों में बैक्टीरियल डायरिया, मेनिन्जाइटिस और सेप्सिस जैसी अभिव्यक्तियाँ शामिल हैं। रोगी ऑटोइम्यून वंशानुगत विकृति, गठिया और थ्रोम्बोसाइटोपेनिया से प्रभावित हो सकते हैं।
संक्रमण के लिए रोगी के नियमित संपर्क से मेनिंगोएन्सेफलाइटिस या एन्सेफलाइटिस हो सकता है, जो बाद में घातक होता है। और जोड़ों के विस्तार के स्थानों पर शरीर पर फुफ्फुस और त्वचा पर चकत्ते भी दिखाई देते हैं।

उम्र के अनुसार लक्षण
मजबूत सेक्स के प्रतिनिधि ऐसी बीमारियों को विकसित कर सकते हैं:
- ओटिटिस मीडिया का अंतिम चरण;
- निमोनिया;
- इन्फ्लूएंजा बी वायरस;
- मेनिंगोकोकी और स्टेफिलोकोसी।
12 वर्ष से कम उम्र के बच्चों में, इस विकृति के कारण, अलग-अलग कैप्सूल में संलग्न बैक्टीरियोसिस विकसित होता है। बाहरी नकारात्मक कारकों से प्राप्त संक्रमण से ओटिटिस मीडिया, निमोनिया, साइनसाइटिस और इन्फ्लूएंजा बी वायरस विकसित होते हैं। इन सभी प्राप्त बीमारियों का इलाज करना मुश्किल है।
वयस्कता में, स्टैफिलोकोकल या स्ट्रेप्टोकोकल संक्रमणों की निरंतर आपूर्ति के कारण त्वचा पर चकत्ते से जुड़ी समस्याएं लंबे समय तक रहती हैं, और ओटिटिस मीडिया धीरे-धीरे क्रोनिक साइनसिसिस में विकसित होता है।
छोटे बच्चे और किसी भी उम्र के लोग ऑटोइम्यून बीमारियों से प्रभावित हो सकते हैं।
विशेषज्ञों द्वारा जांच के आधार पर डेटा से पता चलता है कि नर शिशुओं के वजन और ऊंचाई के लिए छोटे पैरामीटर होते हैं, इस तथ्य के कारण कि वे ब्रूटन रोग के कारण विकसित नहीं हो सकते हैं। जांच के दौरान लिम्फ नोड्स या टॉन्सिल बिल्कुल भी निर्धारित नहीं हो सकते हैं, या बहुत छोटे हो सकते हैं।
पैथोलॉजी का पता तभी लगाया जा सकता है जब बच्चा खराब महसूस करता है, यानी वह बीमार हो जाता है विषाणुजनित रोगऔर नहीं चिकित्सा तैयारीएंटीबायोटिक्स सहित, मदद नहीं कर पाएंगे। लेकिन त्वचा पर अल्सर के रूप में गैंग्रीन का विकास और निचले छोरों पर सेल्युलाईट की उपस्थिति को भी बाहर नहीं किया जाता है।
रोग की नैदानिक तस्वीर
बच्चे के जन्म के बाद, पैथोलॉजी खुद को किसी भी चीज़ में प्रकट नहीं करती है, क्योंकि इम्युनोग्लोबुलिन की सामग्री सामान्य स्तर पर होती है। लेकिन जीवन के 3-5 महीनों में, सेप्सिस या पायोडर्मा हो सकता है, जिसका इलाज एंटीबायोटिक दवाओं से नहीं किया जा सकता है। इसके अलावा, रोग फेफड़ों, मध्य कान और जठरांत्र संबंधी मार्ग को प्रभावित करता है। मैनिंजाइटिस, ऑस्टियोमाइलाइटिस और पैनसिनुसाइटिस जैसी विकृतियाँ नोट की जाती हैं।
पैथोलॉजी का निदान
ब्रूटन की बीमारी का जल्द पता लगाने से इसके आगे के विकास और संक्रमण और फेफड़ों की बीमारियों से होने वाली मौतों से बचने में मदद मिलेगी। पैथोलॉजी के तथ्य की पुष्टि बी लिम्फोसाइटों की अनुपस्थिति या बहुत कम स्तर से होती है, जबकि साथ ही टी लिम्फोसाइटों का एक उच्च स्तर होता है।
यह सब आणविक विश्लेषण के आधार पर निर्धारित किया जाता है, जो गर्भावस्था के स्तर पर एक माँ में किया जा सकता है जो इस तरह के जीन को वहन करती है। 100 यूनिट से कम दिखाने वाला इम्युनोग्लोबुलिन परीक्षण इस बीमारी की पुष्टि का संकेत देता है। कभी-कभी 20 साल की उम्र के बाद ब्रूटन की बीमारी का पता चलता है, क्योंकि प्रोटीन में एक उत्परिवर्तन हुआ है।

प्रयोगशाला परीक्षणों में शामिल हैं:
- इम्युनोग्लोबुलिन ई और ए के मात्रात्मक संकेतकों के माप का संचालन, एंटीबॉडी के लिए परीक्षण, बाद में मातृ एंटीबॉडी में कमी की अवधि के दौरान 6 महीने तक पहुंचने के बाद सबसे अच्छा मापा जाता है। यदि इन संकेतकों की 100 से कम इकाइयाँ पाई जाती हैं, तो इसका मतलब है कि ब्रूटन की बीमारी मौजूद है।
- एंटीबॉडी के निषेधात्मक रूप से निम्न स्तर का निर्धारण करने के बाद, मूल्य के इस पता लगाने की पुष्टि करना आवश्यक है। यदि बी-लिम्फोसाइटों की सतह पर स्थित प्रोटीन भी 100 यूनिट से कम है, लेकिन टी-सेल लिम्फोसाइटों के विश्लेषण के लिए मूल्य बढ़ जाता है।
- इसके बाद न्यूमोकोकल जैसे टीकों के प्रति संवेदनशीलता निर्धारित करने के लिए आवश्यक विश्लेषण आता है।
इस तरह, आप ब्रूटन रोग की उपस्थिति को सत्यापित कर सकते हैं।
मुख्य चल रहे अध्ययनों के साथ, फेफड़ों की स्थिति की लगातार निगरानी की जानी चाहिए, एक नियम के रूप में, यह 5 वर्ष और उससे अधिक उम्र के बच्चों के लिए किया जाता है।

रोग का उपचार
शरीर के महत्वपूर्ण कार्यों को बनाए रखने के लिए, जीवन भर चिकित्सा आवश्यक है। एक नियम के रूप में, स्वस्थ दाताओं से लिए गए इम्युनोग्लोबुलिन या देशी प्लाज्मा के साथ अंतःशिरा टीकाकरण का उपयोग किया जाता है।
जब पैथोलॉजी को पहली बार पहचाना जाता है, तो 400 यूनिट से अधिक इम्युनोग्लोबुलिन के सामान्य स्तर तक संतृप्त करने के लिए प्रतिस्थापन उपचार किया जाता है। यदि इस समय रोगी में भड़काऊ और शुद्ध प्रक्रियाएं नहीं होती हैं, तो आप इस टीके को प्रोफिलैक्सिस के रूप में रखना जारी रख सकते हैं।
यदि प्युलुलेंट फोड़ा जैसी कोई बीमारी है, तो इसके स्थान की परवाह किए बिना, एंटीबायोटिक दवाओं के साथ उपचार की आवश्यकता होती है।
रोग के लक्षणों के उपचार में, नाक के साइनस को कीटाणुनाशक से धोना, छाती की कंपन मालिश और फेफड़ों के पोस्टुरल ड्रेनेज का प्रदर्शन किया जाता है।

पैथोलॉजी भविष्यवाणियां
यदि किसी व्यक्ति में ब्रूटन रोग पाया जाता है प्रारंभिक अवस्था, इसकी अधिक गंभीर अभिव्यक्ति की शुरुआत से पहले, फिर सही ढंग से निर्धारित और समय पर की गई चिकित्सा सामान्य जीवन गतिविधि को बनाए रखने में मदद करेगी।
लेकिन, फिर भी, आंकड़े इस बात की पुष्टि करते हैं कि भड़काऊ प्रक्रियाओं की अवधि में बीमारी के कई मामलों का पता देर से चलता है, फिर यह परिस्थिति विकृति विज्ञान के प्रतिकूल आगे के विकास की धमकी देती है।
निवारक कार्रवाई
इस रोग का एक आनुवंशिक मूल है, इसलिए कोई भी निवारक उपायप्रभाव यहाँ शक्तिहीन हैं। पैथोलॉजी की अभिव्यक्ति को रोकने के लिए, बच्चे के जन्म से पहले जोड़ों की जांच की जानी चाहिए और किसी विशेषज्ञ से सलाह लेनी चाहिए। यदि नवजात शिशु में इस रोग के लक्षण हों तो निम्न उपाय करने चाहिए:
- चिकित्सीय उपाय करना;
- अच्छी तरह से निर्धारित चिकित्सा;
- निष्क्रिय दवाओं के साथ टीकाकरण।
अध्याय 3. प्रतिरक्षा की स्थिति
इम्यूनोडिफ़िशिएंसी राज्यों की परिभाषा, नैदानिक अभिव्यक्तियाँ और वर्गीकरण। प्राथमिक आईडीएस का वर्गीकरण। बी-सेल लिंक के एक प्रमुख घाव के साथ अनुकूली प्रतिरक्षा के प्राथमिक आईडीएस। टी-सेल लिंक के प्रमुख घाव के साथ अनुकूली प्रतिरक्षा के प्राथमिक आईडीएस। संयुक्त टी- और बी-इम्यूनोडेफिशिएंसी। जन्मजात प्रतिरक्षा के फागोसाइटिक लिंक की प्राथमिक कमियां। पूरक प्रणाली की प्राथमिक कमियां। प्राथमिक आईडीएस का प्रारंभिक निदान। परिभाषा, माध्यमिक इम्युनोडेफिशिएंसी के गठन का मुख्य कारण। शारीरिक (उम्र से संबंधित) इम्युनोडेफिशिएंसी। माध्यमिक आईडीएस की घटना में पहले से मौजूद बीमारियों, आईट्रोजेनिक कारकों, प्रतिकूल पर्यावरणीय कारकों और जीवन शैली जोखिम कारकों की भूमिका।
प्रतिरक्षा प्रणाली के कामकाज में, शरीर की किसी भी अन्य प्रणाली की तरह, गड़बड़ी हो सकती है जो इस प्रणाली की मुख्य रूप से विशेषता वाले रोगों के विकास की ओर ले जाती है। इस तरह के विकारों के सबसे आम प्रकारों में से एक इम्युनोडेफिशिएंसी स्टेट्स (आईडीएस) है, जो एक सामान्य प्रतिरक्षा प्रतिक्रिया विकसित करने के लिए प्रतिरक्षा प्रणाली की अक्षमता की विशेषता है।
इम्युनोडेफिशिएंसी स्टेट्स (आईडीएस) में कमी है कार्यात्मक गतिविधिप्रतिरक्षा प्रणाली के मुख्य घटकों में से, प्रतिरक्षात्मक प्रतिक्रिया के उल्लंघन के लिए अग्रणी, कमी या अपर्याप्त जन्मजात या अनुकूली प्रतिरक्षा प्रतिक्रिया के गठन के लिए विभिन्न प्रकार के रोगजनकों और एंटीजन, मुख्य रूप से संक्रामक लोगों के लिए।
इम्युनोडेफिशिएंसी की अवधारणा को इम्यूनोलॉजिकल टॉलरेंस की अवधारणा से अलग करना आवश्यक है, जिसमें प्रतिरक्षा प्रतिक्रिया भी कम या अनुपस्थित है। इम्युनोडेफिशिएंसी के विपरीत, इम्यूनोलॉजिकल टॉलरेंस हमेशा विशिष्ट होता है, अर्थात यह केवल एक विशेष एंटीजन या एंटीजन के समूह के खिलाफ बनता है। इम्युनोडेफिशिएंसी राज्यों में, एक नियम के रूप में, सामान्य रूप से प्रतिरक्षात्मक प्रतिक्रिया कम हो जाती है।
आईडीएस की उपस्थिति मुख्य रूप से शरीर की संक्रमण-रोधी रक्षा में कमी की ओर ले जाती है, जो चिकित्सकीय रूप से संक्रामक रुग्णता में वृद्धि में प्रकट होती है।
अनुकूली प्रतिरक्षा के बी-सेल लिंक के प्रमुख घाव वाले आईडीएस के लिएस्टेफिलोकोसी, स्ट्रेप्टोकोकी, न्यूमोकोकी, रोगजनकों के कारण होने वाले आवर्तक संक्रमणों की घटना की विशेषता आंतों में संक्रमणऔर आदि।
अनुकूली प्रतिरक्षा के टी-सेल लिंक के एक प्रमुख घाव के साथ आईडीएस मेंकई जीवाणु संक्रमणों के अलावा, कैंडिडा कवक, वायरस (दाद, साइटोमेगालोवायरस, एडेनोवायरस), न्यूमोसिस्टिस, इंट्रासेल्युलर बैक्टीरिया (माइकोबैक्टीरिया, यूरियाप्लाज्म, आदि) जैसे अवसरवादी वनस्पतियों के कारण होने वाले संक्रामक रोग हैं। तपेदिक संक्रमण के सामान्यीकरण की प्रवृत्ति भी विशेषता है, और हेलमनिथेसिस की आवृत्ति बढ़ जाती है।
प्राथमिक आईडीएस जन्मजात प्रतिरक्षा के घटकों में दोषों के कारण भी हो सकता है। ये दोष जन्मजात प्रतिरक्षा प्रणाली के विभिन्न हिस्सों को प्रभावित कर सकते हैं: पूरक प्रणाली के घटक और अवरोधक, फागोसाइटिक कोशिकाओं में दोष, एनके कोशिकाएं, रिसेप्टर्स और परिवहन अणु (टीएआर) एंटीजन प्रसंस्करण में शामिल हैं। इस क्षेत्र में गहन शोध के संबंध में, जो आधुनिक आनुवंशिक और आणविक जैविक विधियों का उपयोग करके किया जाता है, जन्मजात प्रतिरक्षा के प्राथमिक आईडीएस के अधिक से अधिक नए रूपों के साथ-साथ जन्मजात और अनुकूली प्रतिरक्षा के संयुक्त आईडीएस की पहचान की जा रही है। एक नियम के रूप में, जन्मजात प्रतिरक्षा के प्राथमिक आईडीएस संक्रामक रोगों की एक विस्तृत विविधता के रूप में प्रकट होते हैं, उदाहरण के लिए:
· पूरक घटकों की कमी(C1, C4, C2; C3, C5-9, आदि) इनकैप्सुलेटेड सूक्ष्मजीवों (निसेरिया मेनिंगिटिडिस, न्यूमोकोकस, हीमोफिलस इन्फ्लुएंजा) के कारण आवर्तक सामान्यीकृत संक्रमण की ओर जाता है। प्रणालीगत ल्यूपस एरिथेमेटोसस आम है।
· फागोसाइटिक प्रणाली में दोषचिकित्सकीय रूप से अधिक बार त्वचा और पैरेन्काइमल अंगों के संक्रामक घावों के रूप में प्रकट होता है, उदाहरण के लिए, क्रोनिक ग्रैनुलोमेटस रोग में स्टेफिलोकोसी और क्लेबसिएला के कारण होता है।
आईडीएस की नैदानिक अभिव्यक्तियों में हेमटोलॉजिकल विकार (लिम्फैडेनोपैथी, ल्यूकेमिया) भी शामिल हैं, घावों की घटना विशेषता है जठरांत्र पथमुख्य रूप से जठरांत्र संबंधी मार्ग की बिगड़ा हुआ स्थानीय प्रतिरक्षा के कारण होता है। अक्सर, आईडीएस ऑटोइम्यून और एलर्जी रोगों की घटना के साथ होता है। एक विशेष स्थान ऑन्कोलॉजिकल रोगों का है। आईडीएस के रोगियों में अक्सर हेमोब्लास्टोस, लिम्फोप्रोलिफेरेटिव रोग, कपोसी का सारकोमा होता है।
सभी इम्युनोडेफिशिएंसी को आमतौर पर प्राथमिक, या जन्मजात, और माध्यमिक, या अधिग्रहित में विभाजित किया जाता है।माध्यमिक आईडीएस आनुवंशिक रूप से निर्धारित नहीं होते हैं, प्रतिरक्षा प्रणाली में ऐसे दोष जीवन के दौरान प्राप्त होते हैं और प्रतिरक्षा प्रणाली पर किसी भी हानिकारक प्रभाव या अन्य बीमारियों की उपस्थिति का परिणाम होते हैं।
प्राथमिक इम्युनोडेफिशिएंसी राज्य
प्राथमिक आईडीएस एक या अधिक घटकों में आनुवंशिक दोषों से जुड़े जन्मजात और/या अनुकूली प्रतिरक्षा प्रणाली के वंशानुगत विकार हैं। अनुकूली प्रतिरक्षा प्रणाली के प्राथमिक आईडीएसइसके बी-सेल और टी-सेल लिंक में प्रमुख दोषों के कारण, कई मामलों में दोनों लिंक के संयुक्त घाव होते हैं। सबसे अधिक अध्ययन किया गया जन्मजात प्रतिरक्षा के प्राथमिक आईडीएसआईडीएस पूरक प्रणाली और फागोसाइटिक प्रणाली में आनुवंशिक दोषों के कारण होते हैं।
विकास की अंतर्गर्भाशयी अवधि में गर्भावस्था के सामान्य पाठ्यक्रम में, बच्चा बाँझ परिस्थितियों में होता है। जन्म के तुरंत बाद उसके शरीर में सूक्ष्म जीवाणुओं की भरमार होने लगती है। चूंकि व्यक्ति के आसपास का माइक्रोफ्लोरा रोगजनक नहीं है, इस उपनिवेश से बीमारी नहीं होती है। इसके बाद, रोगजनक सूक्ष्मजीवों के साथ एक बैठक जिसे बच्चा अभी तक नहीं मिला है, एक उपयुक्त के विकास का कारण बनता है स्पर्शसंचारी बिमारियों. रोगज़नक़ के साथ प्रत्येक संपर्क प्रतिरक्षाविज्ञानी स्मृति के विस्तार की ओर जाता है और दीर्घकालिक प्रतिरक्षा बनाता है।
जन्मजात प्रतिरक्षा रक्षा के दो मुख्य घटक, फागोसाइटोसिस और पूरक, साथ ही अनुकूली रक्षा के दो घटक, बी-सेल (एंटीबॉडी) और टी-सेल, शरीर को रोगजनक वायरस, बैक्टीरिया, कवक के निरंतर हमलों से बचाने में शामिल हैं। और प्रोटोजोआ। इनमें से प्रत्येक घटक स्वतंत्र रूप से कार्य कर सकता है, लेकिन अधिकतर वे निकट जटिल अंतःक्रिया में कार्य करते हैं। इनमें से किसी एक लिंक के जन्मजात दोष समग्र रूप से शरीर की सुरक्षा का उल्लंघन करते हैं और चिकित्सकीय रूप से प्रकट होते हैं विभिन्न विकल्पप्राथमिक इम्युनोडेफिशिएंसी।
वर्तमान में, कई प्राथमिक इम्युनोडेफिशिएंसी के रोगजनन में अंतर्निहित आणविक विकारों की पहचान के कारण, और बड़ी परिवर्तनशीलता के कारण नैदानिक तस्वीरयह स्पष्ट हो गया कि इस प्रकार की विकृति पहले की तुलना में बहुत अधिक सामान्य है।
प्राथमिक इम्युनोडेफिशिएंसी के कई रूपों वाले रोगियों के लिए प्रारंभिक निदान और पर्याप्त उपचार आवश्यक है। समय पर सही निदान और पर्याप्त उपचार के बिना, जीवन के पहले वर्ष के दौरान, एक नियम के रूप में, बच्चे की मृत्यु हो जाती है। प्रत्येक प्रकार की इम्युनोडेफिशिएंसी की अपनी, पहले से ही विकसित उपचार रणनीति होती है, और प्रतिरक्षा प्रणाली के अधिकांश प्राथमिक दोष वर्तमान में सुधार के अधीन हैं। प्राथमिक इम्युनोडेफिशिएंसी का समय पर निदान और उपचार समग्र रूप से जनसंख्या में रुग्णता, मृत्यु दर और विकलांगता को कम करने के लिए अप्रयुक्त भंडार में से एक है।
प्राथमिक CID में आमतौर पर होता है वंशानुगत प्रकृति,इसलिए उन्हें आनुवंशिक रूप से निर्धारित आईडीएस भी कहा जाता है। अधिकतर, प्राथमिक CIDs इनहेरिट किए जाते हैं आवर्ती प्रकार. ऐसे मामलों में जहां आनुवंशिक दोष विशिष्ट प्रतिरक्षा कारकों (एंटीबॉडी गठन, अनुकूली प्रतिरक्षा प्रतिक्रिया के सेलुलर रूप) को प्रभावित करते हैं, उन्हें विशिष्ट आईडीएस भी कहा जाता है, गैर-विशिष्ट (जन्मजात) रक्षा घटकों (फागोसाइटोसिस, पूरक प्रणाली, आदि) में दोषों के विपरीत।
कभी-कभी "जन्मजात" शब्द का प्रयोग प्राथमिक आईडीएस के संबंध में किया जाता है, जिसका अर्थ है कि भ्रूण की अवधि में उत्पन्न होने वाले वंशानुगत दोषों के आधार पर एक बीमारी की संभावना, उदाहरण के लिए, अंतर्गर्भाशयी रूबेला के परिणामस्वरूप एक चयनात्मक IgA की कमी।
प्राथमिक इम्युनोडेफिशिएंसी विविध हैं, और साहित्य में उनका विवरण और वर्गीकरण लगातार बदल रहा है। अनुकूली प्रतिरक्षा प्रणाली की इम्युनोडेफिशिएंसी के पहले वर्गीकरणों में से एक 1974 में यू.एम. द्वारा प्रस्तावित किया गया है। लोपुखिन और आर.वी. पेट्रोव वर्गीकरण, जो आनुवंशिक ब्लॉकों के स्तर पर आधारित है विभिन्न चरणटी- और बी-लिम्फोसाइटों का विभेदन।
इस वर्गीकरण के अनुसार, अनुकूली प्रतिरक्षा प्रणाली के आईडीएस के सभी रूपों को तीन समूहों में बांटा गया है:
1. प्राथमिक आईडीएस टी-सिस्टम (ब्लॉक II, VI) के प्रमुख घाव के साथ।
2. प्राथमिक आईडीएस बी-सिस्टम (ब्लॉक III, IV, V) के प्रमुख घाव के साथ।
3. एक साथ क्षति के साथ संयुक्त प्राथमिक आईडीएस टी-और वी-सिस्टम(ब्लॉक I, ब्लॉक V + VI, आदि)।
 मैं
मैं
तना III
hematopoietic
|
|
|
चित्रा 42. टी- और बी-प्रतिरक्षा के प्राथमिक आईडीएस के वर्गीकरण के लिए रोगजनक योजना
(आर.वी. पेट्रोव, यू.एम. लोपुखिन)
ब्लॉक I। व्यावहारिक रूप से कोई हेमटोपोइएटिक स्टेम सेल नहीं हैं। हेमटोपोइएटिक और लिम्फोइड ऊतक के सामान्यीकृत अप्लासिया की विशेषता है। न तो टी- और न ही बी-लिम्फोसाइट्स बनते हैं।
इस ब्लॉक में गंभीर संयुक्त प्रतिरक्षाविज्ञानी कमी (एससीआईडी) शामिल थी, जो विभिन्न रूपों में होती है।
ब्लॉक II। इंट्राथाइमिक टी-लिम्फोसाइटों के विकास के प्रारंभिक चरण में ब्लॉक करें। सेलुलर अनुकूली प्रतिरक्षा का पूर्ण शटडाउन। ऐसे रोगियों को गंभीर आवर्तक वायरल संक्रमण की घटना की विशेषता होती है, जिससे कम उम्र में (1 वर्ष तक) मृत्यु हो जाती है; उच्च आवृत्ति जन्मजात विसंगतियांविकास; विकसित होने का 100-1000 गुना अधिक जोखिम घातक ट्यूमर; रोगी का शरीर विदेशी प्रत्यारोपण को अस्वीकार नहीं करता है।
इस ब्लॉक का प्रतिनिधित्व, विशेष रूप से, थाइमस (डिजॉर्ज सिंड्रोम) के अप्लासिया या हाइपोप्लासिया द्वारा किया जाता है।
ब्लॉक III। यह ब्लॉक एक्स क्रोमोसोम (लड़के बीमार हो जाते हैं) से जुड़े एग्माग्लोबुलिनमिया की विशेषता है। ऐसे बच्चों में, व्यावहारिक रूप से एंटीबॉडी का उत्पादन नहीं होता है, जो मुख्य रूप से लगातार, गंभीर जीवाणु संक्रमण की ओर जाता है। इम्युनोडेफिशिएंसी के इस प्रकार को ब्रूटन रोग कहा जाता है, इसका आमतौर पर जीवन के दूसरे भाग में निदान किया जाता है, क्योंकि पहले महीनों के दौरान बच्चे के शरीर को मातृ एंटीबॉडी द्वारा संरक्षित किया जाता है जो प्लेसेंटा से होकर गुजरते हैं और मां के दूध में निहित होते हैं।
ब्लॉक IV। बी-लिम्फोसाइटों की संख्या कुछ हद तक कम हो जाती है। मैक्रोग्लोबुलिनमिया के साथ हाइपोगैमाग्लोबुलिनमिया, चूंकि आईजीएम संश्लेषण संरक्षित या बढ़ा हुआ है, जबकि आईजीजी और आईजीए का स्तर तेजी से कम हो जाता है।
ब्लॉक वी। आईजीए की चयनात्मक कमी। मुख्य स्रावी इम्युनोग्लोबुलिन की कमी के कारण, ऐसे बच्चे मुख्य रूप से नासॉफिरिन्क्स, श्वसन पथ, जठरांत्र संबंधी मार्ग और मूत्रजननांगी पथ के श्लेष्म झिल्ली से जुड़े संक्रामक रोगों का विकास करते हैं।
ब्लॉक VI. यह परिधीय लिम्फोइड अंगों और रक्तप्रवाह में टी-लिम्फोसाइटों की परिपक्वता और रिलीज की प्रक्रियाओं को प्रभावित करता है। टी-सेल प्रतिरक्षा के कार्यों के एक प्रमुख घाव के साथ संयुक्त विकृति विशेषता है।
वर्तमान में, जन्मजात और अनुकूली प्रतिरक्षा प्रणाली दोनों के 70 से अधिक जन्म दोषों की पहचान की गई है। संभवतः, जैसे-जैसे आणविक इम्यूनोडायग्नोस्टिक्स के तरीकों में सुधार होगा, उनकी संख्या बढ़ेगी। अंतर्जात, एक नियम के रूप में, प्रतिरक्षा प्रणाली के घटकों में से एक में आनुवंशिक रूप से निर्धारित दोष शरीर की संपूर्ण रक्षा प्रणाली का उल्लंघन करते हैं और चिकित्सकीय रूप से प्राथमिक इम्युनोडेफिशिएंसी राज्य के रूपों में से एक के रूप में पाए जाते हैं। चूंकि प्रतिरक्षा प्रणाली के सामान्य कामकाज के दौरान कई प्रकार की कोशिकाएं और सैकड़ों अणु जटिल प्रतिरक्षा प्रतिक्रिया में शामिल होते हैं, प्राथमिक आईडीएस के नैदानिक रूपों का रोगजनन कई प्रकार के दोषों पर आधारित होता है।
पर पिछले साल काइस तथ्य का एहसास हुआ कि प्राथमिक आईडीएस की नैदानिक अभिव्यक्तियाँ न केवल नवजात शिशुओं में देखी जा सकती हैं, बल्कि बाद की उम्र में भी देखी जा सकती हैं। यह इस तथ्य के कारण है कि प्रतिरक्षा के लिंक में से एक में दोष कुछ समय के लिए बढ़ी हुई संक्रामक रुग्णता के रूप में नैदानिक रूप से प्रकट नहीं हो सकता है, क्योंकि प्रतिरक्षा के अन्य सभी घटक संरक्षित हैं और इस दोष की भरपाई तब तक करते हैं जब तक कि उनकी आरक्षित क्षमताएं नहीं होती हैं। समाप्त।
प्राथमिक सीआईडी अपेक्षाकृत दुर्लभ बीमारियां हैं, जिनकी औसत घटना 1/25,000 - 1/100,000 है, हालांकि चयनात्मक IgA की कमी अधिक आम है: 1/500 - 1/700 लोग। 1997 के प्राथमिक सीआईडी के यूरोपीय रजिस्टर के अनुसार, यूरोप में पंजीकृत प्राथमिक सीडीआई की आवृत्ति औसत जनसंख्या का 1/96,000 थी, जबकि कुछ देशों में यह काफी अधिक थी: 1/38,000 (यूके); 1/12500 (स्विट्जरलैंड); 1/10000 (स्वीडन)। सबसे अधिक संभावना है, इस तरह के अंतर विभिन्न देशों में दवा के विकास के स्तर के कारण हैं, और प्राथमिक आईडीएस की वास्तविक आवृत्ति प्रकाशित औसत आंकड़ों की तुलना में काफी अधिक है।
वर्तमान में, प्राथमिक सीआईडी के निम्नलिखित सरलीकृत वर्गीकरण को आम तौर पर स्वीकार किया जाता है:
I. प्राथमिक आईडीएस विनोदी अनुकूली प्रतिरक्षा के एक प्रमुख घाव के साथ
1. एक्स-लिंक्ड अगम्मा (हाइपोगामा) ग्लोब्युलिनमिया - ब्रूटन रोग।
2. कॉमन वेरिएबल इम्यूनोलॉजिकल डेफिसिएंसी (CVID) - कॉमन वेरिएबल हाइपोगैमाग्लोबुलिनमिया।
3. बच्चों में क्षणिक हाइपोगैमाग्लोबुलिनमिया (धीमी प्रतिरक्षाविज्ञानी शुरुआत)।
4. इम्युनोग्लोबुलिन की चयनात्मक कमी (IgA की चयनात्मक कमी)।
द्वितीय. प्राथमिक आईडीएस टी-सेल अनुकूली प्रतिरक्षा के एक प्रमुख घाव के साथ
1. डिजॉर्ज सिंड्रोम (हाइपो-, थाइमस का अप्लासिया)।
2. क्रोनिक म्यूकोक्यूटेनियस कैंडिडिआसिस।
III. अनुकूली प्रतिरक्षा की संयुक्त टी- और बी-प्रतिरक्षा की कमी
1. गंभीर संयुक्त प्रतिरक्षाविज्ञानी कमी (एससीआईडी):
ए) एक्स-लिंक्ड;
बी) ऑटोसोमल रिसेसिव।
2. गतिभंग - टेलैंगिएक्टेसिया (लुई-बार सिंड्रोम)।
3. विस्कॉट-एल्ड्रिच सिंड्रोम।
4. इम्यूनोडिफ़िशिएंसी के साथ बढ़ा हुआ स्तरआईजीएम (एक्स क्रोमोसोम से जुड़ा हुआ)।
5. बौनापन के साथ प्रतिरक्षण क्षमता।
चतुर्थ। फागोसाइटिक प्रणाली की कमियां
1. क्रोनिक लिम्फोग्रानुलोमैटोसिस।
2. चेदिएक-हिगासी सिंड्रोम।
3. हाइपर-आईजीई सिंड्रोम (जॉब सिंड्रोम)।
V. पूरक प्रणाली की कमियां
1. पूरक घटकों की कमी के कारण प्राथमिक आईडीएस।
2. प्राथमिक आईडीएस पूरक प्रणाली निष्क्रियकर्ताओं की कमी के कारण होता है।
एक प्रमुख घाव के साथ प्राथमिक आईडीएस
हास्य अनुकूली प्रतिरक्षा
ब्रूटन की बीमारी
1952 में पहली बार, अमेरिकी बाल रोग विशेषज्ञ ब्रूटन (ब्रुटन) ने एक 8 वर्षीय लड़के का वर्णन किया, जो विभिन्न संक्रामक रोगों से पीड़ित था, जिसे 4 साल की उम्र तक 14 बार निमोनिया, बार-बार ओटिटिस, साइनसाइटिस, सेप्सिस और मेनिन्जाइटिस का सामना करना पड़ा था। अध्ययन के दौरान उनके रक्त सीरम में कोई एंटीबॉडी नहीं पाई गई। यह पहला विवरण था प्राथमिक इम्युनोडेफिशिएंसीवैज्ञानिक चिकित्सा साहित्य में, एक स्वतंत्र नोसोलॉजिकल रूप के रूप में प्रतिष्ठित।
ब्रूटन की बीमारी एक्स-लिंक्ड रिसेसिव है और केवल लड़कों को प्रभावित करती है। इस रोग को एक्स-लिंक्ड एग्माग्लोबुलिनमिया भी कहा जाता है। जनसंख्या के 1/1000000 की आवृत्ति के साथ होता है। यूके में, इस इम्युनोडेफिशिएंसी की घटना 1/100,000 है।
ब्रूटन की बीमारी साइटोप्लाज्मिक टाइरोसिन किनसे एंजाइम में एक दोष पर आधारित है, जो बी-लिम्फोसाइटों के नाभिक को इसके सक्रियण के लिए एक प्लाज्मा सेल में बाद के परिवर्तन के साथ एक संकेत प्रेषित करता है। इस प्रकार, इम्युनोग्लोबुलिन का संश्लेषण असंभव हो जाता है।
रोग के पहले लक्षण 7-8 महीने से 2-3 साल तक दिखाई देते हैं। इम्युनोग्लोबुलिन का ट्रांसप्लासेंटल ट्रांसफर आमतौर पर बच्चों को जीवन के पहले कुछ महीनों के दौरान संक्रमण से बचने के लिए पर्याप्त एंटीबॉडी प्रदान करता है। भविष्य में, एंटीबॉडी संश्लेषण की अनुपस्थिति, एक नियम के रूप में, आवर्तक की घटना की ओर ले जाती है जीवाण्विक संक्रमणमुख्य रूप से श्वसन पथ और त्वचा का। आमतौर पर रोगजनक स्ट्रेप्टोकोकी, स्टेफिलोकोसी और ग्राम-नकारात्मक बैक्टीरिया होते हैं। संक्रमण फैलता है, जिससे सेप्टीसीमिया और मेनिन्जाइटिस होता है। हालांकि, ये बच्चे वायरल संक्रमण के प्रति प्रतिरोधी रहते हैं, क्योंकि सेलुलर प्रतिरक्षा क्षीण नहीं होती है।
वस्तुनिष्ठ परीक्षा परअसामान्य रूप से छोटे, चिकने टॉन्सिल, छोटे लिम्फ नोड्स का पता लगाएं, प्लीहा बढ़े हुए नहीं हैं। इस तथ्य पर विशेष ध्यान देता है कि लिम्फ नोड्स, यकृत और प्लीहा शरीर में संक्रामक और भड़काऊ प्रक्रिया में वृद्धि के साथ प्रतिक्रिया नहीं करते हैं, जो एक महत्वपूर्ण नैदानिक संकेत है।
आंतों के म्यूकोसा में, प्लाज्मा कोशिकाएं पूरी तरह से गायब हो जाती हैं, हालांकि आम तौर पर वे वहां पर्याप्त मात्रा में निहित होती हैं। बड़ी संख्या में. इस संबंध में, अवशोषण विकार देखे जाते हैं, पुरानी आंत्रशोथ अक्सर विकसित होती है। आंत में, आंतों के क्रिप्ट में क्षयकारी ल्यूकोसाइट्स के संचय के साथ अक्सर फोड़े का पता लगाया जाता है।
प्रयोगशाला परीक्षा के दौरानपरिधीय रक्त में बी-लिम्फोसाइटों की तेज कमी या अनुपस्थिति, निम्न स्तर या इम्युनोग्लोबुलिन के सभी वर्गों की अनुपस्थिति होती है।
इलाज:इम्युनोग्लोबुलिन के साथ स्थायी प्रतिस्थापन चिकित्सा। इम्युनोग्लोबुलिन की तैयारी प्रति माह 200-600 मिलीग्राम / किग्रा की खुराक पर अंतःशिरा में प्रशासित की जाती है। घटना के मामले में स्पर्शसंचारी बिमारियोंइसके अतिरिक्त, विशिष्ट इम्युनोग्लोबुलिन (एंटी-स्टैफिलोकोकल, एंटी-स्ट्रेप्टोकोकल, एंटी-खसरा, आदि) प्रशासित किए जाते हैं।
भविष्यवाणी:एक सही निदान और समय पर उपचार के साथ, यह अपेक्षाकृत अनुकूल है।