3.3. Rasvade süntees
Rasvad sünteesitakse glütseroolist ja rasvhapetest. Glütseriin kehas tekib rasva (toidu või enda) lagunemisel ning moodustub kergesti ka süsivesikutest. Rasvhapped sünteesitakse atsetüülkoensüümist A, mis on organismi universaalne metaboliit. See süntees nõuab endiselt vesinikku (NADPH 2 kujul) ja ATP energiat. Keha sünteesib ainult küllastunud ja monoküllastumata aineid (millel on üks kaksikside) rasvhape. Happed, mille molekulis on kaks või enam kaksiksidet (polüküllastumata), ei sünteesita kehas ja neid tuleb varustada toiduga. Rasva sünteesiks võib kasutada ka rasvhappeid – toidu hüdrolüüsiprodukte ja oma rasvu.
Kõik rasvade sünteesis osalejad peavad olema aktiivses vormis: glütserool glütserofosfaadi kujul ja rasvhapped atsüül-koensüümi A kujul. Rasvade süntees toimub rakkude tsütoplasmas (peamiselt rasvkoes, maksas, peensoolde) ja toimib järgmise skeemi järgi
Tuleb rõhutada, et glütserooli ja rasvhappeid saab süsivesikutest. Seetõttu, millal ületarbimine süsivesikud istuva eluviisi taustal arendab rasvumist.
Loeng 4. Valkude ainevahetus
4.1. Valkude katabolism
Keha rakke moodustavad valgud alluvad ka pidevale lagunemisele rakusisese toimel proteolüütilised ensüümid helistas intratsellulaarsed proteinaasid või katepsiinid. Need ensüümid paiknevad spetsiaalsetes intratsellulaarsetes organellides - lüsosoomides. Katepsiinide toimel muudetakse ka kehavalgud aminohapeteks. (Oluline on märkida, et nii toidu kui ka keha enda valkude lagunemisel tekivad samad 20 tüüpi aminohappeid.) Päevas laguneb ligikaudu 200 g kehavalke. Seetõttu ilmub kehasse päeva jooksul umbes 300 g vabu aminohappeid.
4.2. Valkude süntees
Enamikku aminohappeid kasutatakse valkude sünteesiks. Valkude süntees toimub nukleiinhapete kohustuslikul osalemisel.
Valkude sünteesi esimene samm on transkriptsioon- viiakse läbi raku tuumas, kasutades geneetilise teabe allikana DNA-d. Geneetiline informatsioon määrab sünteesitud valgu polüpeptiidahelate aminohapete järjestuse. Seda teavet kodeerib DNA molekuli lämmastikualuste järjestus. Iga aminohapet kodeerib kolme lämmastiku aluse kombinatsioon, mida nimetatakse koodon, või kolmik. DNA molekuli osa, mis sisaldab teavet konkreetse valgu kohta, nimetatakse "geen". Messenger RNA (mRNA) sünteesitakse selles DNA piirkonnas transkriptsiooni käigus vastavalt komplementaarsuse põhimõttele. See nukleiinhape on vastava geeni koopia. Saadud mRNA lahkub tuumast ja siseneb tsütoplasmasse. Samamoodi toimub DNA-l, nagu ka maatriksil, ribosomaalse (rRNA) ja transpordi (tRNA) süntees.
Teise etapi ajal - äratundmine tsütoplasmas esinev (äratundmine) seonduvad aminohapped selektiivselt oma kandjatega - ülekande-RNA-ga (tRNA). Iga tRNA molekul on lühike polünukleotiidahel, mis sisaldab ligikaudu 80 nukleotiidi ja on osaliselt keerdunud topeltheeliksiks, mis viib "kõvera ristikulehe" konfiguratsioonini. Polünukleotiidahela ühes otsas on kõigil tRNA-del adeniini sisaldav nukleotiid. Selle tRNA molekuli otsa külge on kinnitatud aminohape. Aminohappe kinnituskoha vastas olev silmus sisaldab antikoodonit, mis koosneb kolmest lämmastiku alusest ja on ette nähtud järgnevaks seondumiseks komplementaarse mRNA koodoniga. Üks tRNA molekuli külgsilmustest tagab tRNA kinnitumise ensüümiga, mis osaleb äratundmine, ja teine, külgmine, on vajalik tRNA kinnitumiseks ribosoomile valgusünteesi järgmises etapis.
Selles etapis kasutatakse ATP molekuli energiaallikana. Äratundmise tulemusena moodustub aminohappe-tRNA kompleks. Sellega seoses nimetatakse valgusünteesi teist etappi aminohapete aktiveerimiseks.
Kolmas samm valgusünteesis on saade- Esineb ribosoomidel. Iga ribosoom koosneb kahest osast – suurest ja väikesest alamosakestest. Keemilise koostise poolest koosnevad mõlemad alamosakesed rRNA-st ja valkudest. Ribosoomid on võimelised kergesti lagunema alamosakesteks, mida saab taas omavahel kombineerida, moodustades ribosoomi. Translatsioon algab ribosoomi dissotsiatsioonist alamosakesteks, mis kinnituvad kohe tuumast tuleva mRNA molekuli algosa külge. Sel juhul jääb alamosakeste vahele ruum (nn tunnel), kus asub väike mRNA piirkond. Seejärel kinnitatakse saadud ribosoomi-mRNA kompleksiga aminohapetega seotud tRNA-d. tRNA kinnitumine selle kompleksiga toimub, sidudes ühe tRNA külgahelatest ribosoomiga ja tRNA antikoodoni sidudes selle komplementaarse mRNA koodoniga, mis asub ribosoomi subühikute vahelises tunnelis. Samal ajal saavad ribosoomi-mRNA kompleksiga liituda ainult kaks aminohapetega tRNA-d.
tRNA antikoodonite spetsiifilise seondumise tõttu mRNA koodonitega liituvad tunnelis paikneva mRNA molekuli lõiguga ainult nende tRNA molekulid, milles antikoodonid on komplementaarsed mRNA koodonitega. Seetõttu tarnivad need tRNA-d ribosoomidesse ainult rangelt määratletud aminohappeid. Lisaks ühendatakse aminohapped üksteisega peptiidsidemega ja moodustub dipeptiid, mis on seotud ühe tRNA-ga. Pärast seda liigub ribosoom mööda mRNA-d täpselt ühe koodoni võrra (seda ribosoomi liikumist nimetatakse marsruudi asukoht).
Translokatsiooni tulemusena lõhustatakse ribosoomist vaba (ilma aminohappeta) tRNA ning tunnelitsooni tekib uus koodon, mille külge kinnitub komplementaarsuse põhimõttel teine tRNA sellele koodonile vastava aminohappega. . Tarnitud aminohape ühineb eelnevalt moodustunud dipeptiidiga, mis viib peptiidahela pikenemiseni. Sellele järgnevad uued translokatsioonid, uute aminohapetega tRNA-de sisenemine ribosoomi ja peptiidahela edasine pikenemine.
Seega määrab sünteesitud valgu aminohapete järjestuse mRNA koodonite järjestus. Polüpeptiidahela süntees on lõppenud, kui tunnelisse siseneb spetsiaalne koodon, mis ei kodeeri aminohappeid ja millega ei saa liituda ükski tRNA. Selliseid koodoneid nimetatakse terminatsioonikoodoniteks.
Selle tulemusena sünteesitakse kirjeldatud kolme etapi tõttu polüpeptiidid, st moodustub valgu esmane struktuur. Kõrgemad (ruumilised) struktuurid (sekundaarne, tertsiaarne, kvaternaarne) tekivad spontaanselt.
Valkude süntees on energiamahukas protsess. Ainult ühe aminohappe lisamiseks sünteesitud valgu molekuli on vaja vähemalt kolme ATP molekuli.
4.3. Aminohapete metabolism
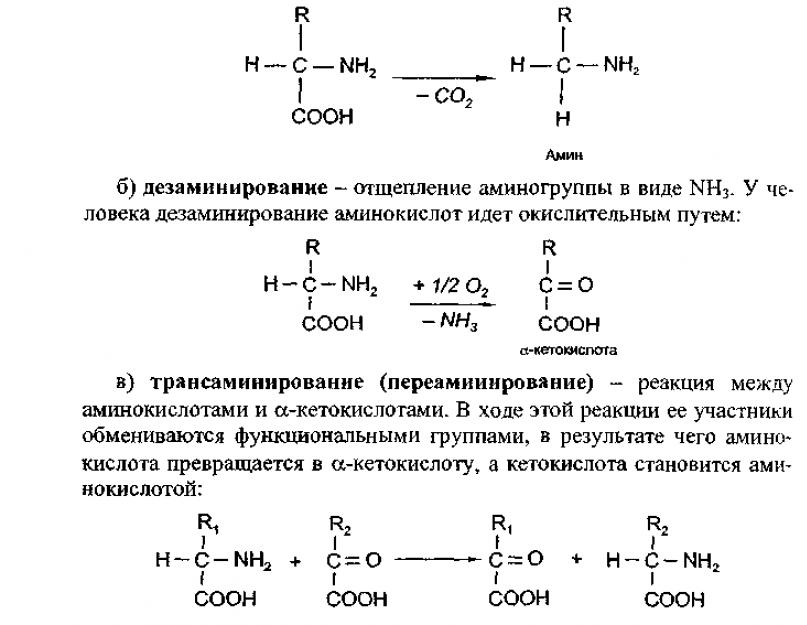
Aminohappeid kasutatakse lisaks valkude sünteesile ka erinevate suure bioloogilise tähtsusega mittevalguliste ühendite sünteesiks. Osa aminohapetest laguneb ja muutub lõppproduktideks: CO 2 , H 2 0 ja NH 3 Lagunemine algab reaktsioonidest, mis on omased enamikule aminohapetele.
Need sisaldavad:
a) dekarboksüülimine - lõhustamine karboksüülrühma aminohapetest süsinikdioksiidi kujul:

Kõik aminohapped läbivad transamiinimise. See reaktsioon hõlmab koensüümi - fosfopüridoksaali, mille moodustamiseks on vaja B6-vitamiini - püridoksiini.
Transamiinimine on peamine aminohapete muundumine organismis, kuna selle kiirus on palju suurem kui dekarboksüülimise ja deaminatsiooni reaktsioonide oma.
Transaminatsioonil on kaks peamist funktsiooni:
a) transamiinimise tõttu võivad mõned aminohapped muutuda teisteks. Sel juhul aminohapete koguarv ei muutu, kuid nendevaheline suhe muutub. Toiduga satuvad organismi võõrvalgud, milles aminohapped on organismi valkudega võrreldes erinevas vahekorras. Transamineerimisega korrigeeritakse organismi aminohapete koostist.
b) on lahutamatu osa kaudne (kaudne) deamineerimine aminohapped – protsess, millest algab enamiku aminohapete lagunemine.
Selle protsessi esimeses etapis astuvad aminohapped α-ketoglutaarhappega transamiinimisreaktsiooni. Sel juhul muundatakse aminohapped α-ketohapeteks ja α-ketoglutaarhape glutamiinhappeks (aminohape).
Teises etapis deamineeritakse saadud glutamiinhape, NH3 eraldatakse sellest ja moodustub uuesti α-ketoglutaarhape. Saadud α-ketohapped lagunevad veelgi ja muutuvad lõppsaadusteks CO 2 ja H 2 0. Igal 20 ketohappel (neid moodustub nii palju kui on aminohappetüüpe) on oma spetsiifilised lagunemisteed. Mõne aminohappe lagunemisel tekib aga vaheproduktina püroviinamarihape, millest saab sünteesida glükoosi. Seetõttu nimetatakse aminohappeid, millest sellised ketohapped tekivad glükogeenne. Teised ketohapped ei moodusta lagunemise käigus püruvaati. Nende vaheprodukt on atsetüülkoensüüm A, millest on võimatu saada glükoosi, küll aga saab sünteesida ketokehasid. Sellistele ketohapetele vastavaid aminohappeid nimetatakse ketogeenseteks.
Aminohapete kaudse deamineerimise teine toode on ammoniaak. Ammoniaak on kehale väga mürgine. Seetõttu on kehal selle neutraliseerimiseks molekulaarsed mehhanismid. NH 3 moodustumisel seostub see kõigis kudedes glutamiinhappega, moodustades glutamiini. seda ajutine ammoniaagi neutraliseerimine. Verevooluga siseneb glutamiin maksa, kus see laguneb uuesti glutamiinhappeks ja NH3-ks. Saadud glutamiinhape koos verega siseneb uuesti organitesse, et neutraliseerida uued ammoniaagi portsjonid. Sünteesiks kasutatakse eralduvat ammoniaaki, aga ka maksas leiduvat süsihappegaasi uurea.
Karbamiidi süntees on tsükliline, mitmeetapiline protsess, mis kulutab suur hulk energiat. Aminohape ornitiin mängib uurea sünteesis väga olulist rolli. Seda aminohapet valkudes ei leidu. Ornitiin moodustub teisest aminohappest - arginiin, mis esineb valkudes. Seoses ornitiini olulise rolliga nimetatakse karbamiidi sünteesi ornitiini tsükkel.
Sünteesi käigus seotakse ornitiiniga kaks ammoniaagi molekuli ja süsinikdioksiidi molekul ning ornitiin muutub arginiiniks, millest eraldub koheselt karbamiid ja tekib uuesti ornitiin. Koos ornitiini ja arginiiniga osalevad uurea moodustumisel ka aminohapped: glutamiin ja asparagiinhape. Glutamiin on ammoniaagi tarnija ja asparagiinhape on selle kandja.
Karbamiidi süntees on ammoniaagi lõplik neutraliseerimine. Maksast koos verega siseneb uurea neerudesse ja eritub uriiniga. Päevas moodustub 20-35 g uureat. Karbamiidi eritumine uriiniga iseloomustab valkude lagunemise kiirust organismis.
Jaotis 3. Lihaskoe biokeemia
Loeng 5. Lihaste biokeemia
5.1. Raku struktuur lihaskiud
Loomadel ja inimestel on kahte peamist tüüpi lihaseid: triibuline ja sile. Vöötlihased on kinnitatud luude ehk luustiku külge ja seetõttu nimetatakse neid ka skeletideks. Vöötlihaskiud moodustavad ka südamelihase – müokardi – aluse, kuigi müokardi ja skeletilihaste struktuuris on teatud erinevusi. Siledad lihased moodustavad seina lihaskonna veresooned, sooled, imbuvad kude siseorganid ja nahk.
Iga vöötlihas koosneb mitmest tuhandest kiust, mida ühendavad sidekoekihid ja sama kest - sidekirme. Lihaskiud (müotsüüdid) on väga piklikud suured mitmetuumalised rakud pikkusega kuni 2-3 cm, mõnel lihasel isegi üle 10 cm Lihasrakkude paksus on umbes 0,1-0,2 mm.
Nagu iga rakk müotsüüt sisaldab selliseid kohustuslikke organelle nagu tuumad, mitokondrid, ribosoomid, tsütoplasmaatiline retikulum ja rakusein. Müotsüütide tunnus, mis eristab neid teistest rakkudest, on kontraktiilsete elementide olemasolu - müofibrillid.
Tuumadümbritsetud kestaga - nukleolemmaga ja koosnevad peamiselt nukleoproteiinidest. Tuum sisaldab geneetilist teavet valgusünteesi jaoks.
Ribosoomid- rakusisesed moodustised, mis on keemiliselt nukleoproteiinid. Valkude süntees toimub ribosoomidel.
Mitokondrid- mikroskoopilised mullid suurusega kuni 2-3 mikronit, mis on ümbritsetud topeltmembraaniga. Mitokondrites oksüdeeritakse süsivesikud, rasvad ja aminohapped molekulaarse hapniku (õhuhapniku) abil süsinikdioksiidiks ja veeks. Oksüdatsiooni käigus vabaneva energia tõttu toimub mitokondrites ATP süntees. Treenitud lihastes on mitokondreid palju ja need paiknevad piki müofibrillid.
tsütoplasmaatiline retikulum(sarkoplasmaatiline retikulum, sarkoplasmaatiline retikulum) koosneb membraanidest moodustunud ja üksteisega ühendatud tuubulitest, tuubulitest ja vesiikulitest. Sarkoplasmaatiline retikulum on spetsiaalsete torude abil, mida nimetatakse T-süsteemiks, ühendatud lihasraku kestaga - sarkolemmaga. Erilist tähelepanu väärivad sarkoplasmaatilises retikulumis vesiikulid, mida nimetatakse tsisternidmeie ja mis sisaldavad suures kontsentratsioonis kaltsiumiioone. Tsisternides on Ca 2+ ioonide sisaldus umbes tuhat korda suurem kui tsütosoolis. Selline kaltsiumiioonide kõrge kontsentratsioonigradient tekib tänu ensüümi - kaltsiumadenosiini tri- fosfataas(kaltsiumi ATPaas), mis on manustatud paagi seina. See ensüüm katalüüsib ATP hüdrolüüsi ja tagab sel juhul vabaneva energia tõttu kaltsiumiioonide ülekande mahutitesse. Seda kaltsiumiioonide transpordimehhanismi nimetatakse piltlikult kaltsiumpump, või kaltsiumi pump.
Tsütoplasma(tsütosool, sarkoplasma) hõivab müotsüütide siseruumi ja on kolloidne lahus, mis sisaldab valke, glükogeeni, rasvatilku ja muid lisandeid. Sarkoplasmaatilised valgud moodustavad 25-30% kõigist lihasvalkudest. Sarkoplasmaatiliste valkude hulgas on aktiivseid ensüüme. Nende hulka kuuluvad peamiselt glükolüüsi ensüümid, mis lagundavad glükogeeni või glükoosi püroviinamari- või piimhappeks. Teine oluline sarkoplasmaatiline ensüüm on kreatiinkinaas osalevad lihastöö energiavarustuses. Erilist tähelepanu väärib sarkoplasmaatiline valk müoglobiin, mis on struktuurilt identne verevalgu ühe alaühiku, hemoglobiiniga. Müoglobiin koosneb ühest polüpeptiidist ja ühest heemist. Müoglobiini ülesanne on siduda molekulaarset hapnikku. Tänu sellele valgule tekib lihaskoes teatud varu hapnikuga. AT viimased aastad Müoglobiini teine funktsioon on kindlaks tehtud - see on 0 2 ülekandmine sarkolemmast lihaste mitokondritesse.
Lisaks valkudele sisaldab sarkoplasma mittevalgulisi lämmastikku sisaldavaid aineid. Erinevalt valkudest nimetatakse neid ekstraheerivateks aineteks, kuna neid on lihtne veega ekstraheerida. Nende hulgas on ATP, ADP, AMP ja teiste nukleotiidide adenüülnukleotiidid, kus ATP on ülekaalus. ATP kontsentratsioon rahuolekus on umbes 4-5 mmol/kg. Ekstraktid hõlmavad ka kreatiinfosfaat, selle eelkäija – kreatiin ja kreatiinfosfaadi pöördumatu lagunemise saadus – kreatiniin. AT kreatiinfosfaadi kontsentratsioon puhkeolekus on tavaliselt 15-25 mmol/kg. Aminohapetest glutamiinhape ja glutamiin.
Peamine süsivesik lihaskoes on glükogeen. Glükogeeni kontsentratsioon on vahemikus 0,2-3%. Sarkoplasmas sisalduv vaba glükoos sisaldub väga väikeses kontsentratsioonis - sellest on ainult jäljed. Lihasetöö protsessis sarkoplasmas akumuleeruvad süsivesikute ainevahetuse tooted - laktaat ja püruvaat.
protoplasmaatiline rasv seondub valkudega ja on saadaval kontsentratsioonis 1%. Varu rasv koguneb vastupidavusalaks treenitud lihastesse.
5.2. Sarkolemma struktuur
Iga lihaskiud on ümbritsetud rakumembraaniga - sarkolemma. Sarcolemma on umbes 10 nm paksune liloproteiini membraan. Väljaspool on sarkolemma ümbritsetud kollageenivalgu põimunud ahelate võrgustikuga. Lihaste kokkutõmbumise ajal tekivad kollageenümbrises elastsed jõud, mille tõttu lõdvestunud lihaskiud venivad ja naasevad algsesse olekusse. Motoorsete närvide otsad lähenevad sarkolemmale. Närvilõpu ja sarkolemma kokkupuutepunkti nimetatakse neuromuskulaarne sünaps, või terminaalne närviplaat.
Kontraktsioonielemendid - müofibrillid- hõivavad suurema osa lihasrakkude mahust, nende läbimõõt on umbes 1 mikron. Treenimata lihastes on müofibrillid hajutatud ja treenitud lihastes on nad rühmitatud kimpudeks nn. Conheimi väljad.
5.3. Anisotroopsete ja isotroopsete ketaste struktuur
Müofibrillide struktuuri mikroskoopiline uurimine näitas, et need koosnevad vahelduvatest heledatest ja tumedatest aladest ehk ketastest. Lihasrakkudes on müofibrillid paigutatud nii, et külgnevate müofibrillide heledad ja tumedad alad langevad kokku, mis tekitab mikroskoobiga nähtava kogu lihaskiu põikitriibu. Leiti, et müofibrillid on keerulised struktuurid, mis on ehitatud omakorda suurest hulgast kahte tüüpi lihaskiududest (protofibrillid või filamentid) - rasv ja õhuke. Paksude niitide läbimõõt on 15 nm, õhukeste - 7 nm.
Müofibrillid koosnevad vahelduvatest paralleelsete paksude ja õhukeste filamentide kimpudest, mis lähevad otstest üksteise sisse. Müofibrillide lõik, mis koosneb paksudest filamentidest ja nende vahel paiknevatest õhukeste filamentide otstest, on kaksikmurduv. Mikroskoobi all püüab see piirkond nähtava valguse või elektronide voolu kinni (elektronmikroskoobi kasutamisel) ja tundub seetõttu tume. Selliseid piirkondi nimetatakse anisotroopne, või tumedad, kettad (A-kettad).
Müofibrillide heledad alad koosnevad õhukeste filamentide keskosadest. Nad edastavad suhteliselt kergesti valguskiiri või elektronide voogu, kuna neil puudub kaksikmurdumine ja neid nimetatakse isotroopne või valgus, plaadid (I-kettad).Õhukeste filamentide kimbu keskel paikneb põiki õhuke valguplaat, mis fikseerib lihaskiudude asukoha ruumis. See plaat on mikroskoobi all selgelt nähtav I-kettal kulgeva joonena ja kannab nime Z- plaat.
Müofibrillide lõiku külgnevate 2-liinide vahel nimetatakse sarkomeer. Selle pikkus on 2,5-3 mikronit. Iga müofibrill koosneb mitmesajast sarkomeerist (kuni 1000).
5.4. Kokkutõmbuvate valkude struktuur ja omadused
Müofibrillide keemilise koostise uurimine näitas, et paksud ja õhukesed filamendid koosnevad ainult valkudest.
Paksud niidid koosnevad valkudest müosiin. Müosiin on umbes 500 kDa molekulmassiga valk, mis sisaldab kahte väga pikka polüpeptiidahelat. Need ahelad moodustavad topeltspiraali, kuid ühes otsas need niidid lahknevad ja moodustavad kerakujulise moodustise – kerakujulise pea. Seetõttu eristatakse müosiini molekulis kahte osa - kerakujuline pea ja saba. Paks filament sisaldab umbes 300 müosiini molekuli ja jämeda filamendi ristlõikes leidub 18 müosiini molekuli. Müosiini molekulid jämedates filamentides põimuvad nende sabadega ja nende pead ulatuvad jämedast filamendist korrapärase spiraalina välja. Müosiinipeades on kaks olulist kohta (keskust). Üks neist katalüüsib ATP hüdrolüütilist lõhustamist, st vastab ensüümi aktiivsele saidile. Müosiini ATPaasi aktiivsuse avastasid esmakordselt vene biokeemikud Engelhardt ja Lyubimova. Müosiinipea teine osa tagab paksude filamentide ühendamise õhukeste filamentide valguga lihaste kokkutõmbumise ajal - akmuda.
Õhukesed kiud koosnevad kolmest valgust: aktiin, troponiin ja tropomüosiin.
Õhukeste filamentide peamine valk - aktiin. Aktiin on globulaarne valk molekulmassiga 42 kDa. Sellel valgul on kaks olulist omadust. Esiteks on sellel kõrge polümerisatsioonivõime pikkade ahelate, nn fibrillaarneaktinoom(võib võrrelda helmeste nööriga). Teiseks, nagu juba märgitud, võib aktiin ühenduda müosiinipeadega, mis põhjustab põikisildade või adhesioonide moodustumist õhukeste ja paksude filamentide vahel.
Peenikese niidi aluseks on kahe fibrillaarse aktiini ahela kaksikheeliks, mis sisaldab umbes 300 globulaarse aktiini molekuli (nagu kaks helmikahelat, mis on keerdunud topeltheeliksiks, iga tera vastab globulaarsele aktiinile).
Veel üks õhukeste filamentide valk - tropomüosiin- on ka topeltheeliksi kujul, kuid see spiraal on moodustatud polüpeptiidahelatest ja on palju väiksem kui aktiini topeltheeliksil. Tropomüosiin asub fibrillaarse aktiini kaksikheeliksi soones.
Kolmas õhukeste filamentide valk - troponiin- kinnitub tropomüosiini külge ja fikseerib selle positsiooni aktiini soones, mis blokeerib müosiinipeade vastasmõju õhukeste filamentide globulaarse aktiini molekulidega.
5.5. Lihaste kokkutõmbumise mehhanism
lihaste kokkutõmbumine on keerukas mehaaniline keemiline protsess, mille käigus ATP hüdrolüütilise lagunemise keemiline energia muundatakse lihase poolt tehtavaks mehaaniliseks tööks.
Praegu pole seda mehhanismi veel täielikult välja selgitatud. Kuid kindlasti on teada järgmine:
Lihaste tööks vajalik energiaallikas on ATP.
ATP hüdrolüüsi, millega kaasneb energia vabanemine, katalüüsib müosiin, millel, nagu juba märgitud, on ensümaatiline aktiivsus.
Lihaste kontraktsiooni käivitav mehhanism on Ca ioonide kontsentratsiooni suurenemine müotsüütide sarkoplasmas, mis on põhjustatud motoorsest närviimpulsist.
Lihaste kokkutõmbumise ajal tekivad müofibrillide paksude ja õhukeste filamentide vahele ristsillad ehk adhesioonid.
Lihaste kokkutõmbumise ajal libisevad õhukesed filamendid mööda jämedaid, mis viib müofibrillide ja kogu lihaskiu kui terviku lühenemiseni.
On palju hüpoteese, mis püüavad selgitada lihaste kontraktsiooni molekulaarset mehhanismi. Praegu on kõige mõistlikum sõudepaadi hüpotees”, või X. Huxley „sõudmise” hüpotees. Lihtsustatud kujul on selle olemus järgmine.
Puhkeseisundis olevas lihases ei ole jämedad ja õhukesed müofibrillide filamendid omavahel ühendatud, kuna aktiini molekulide seondumiskohad on suletud tropomüosiini molekulidega.
Lihaste kokkutõmbumine toimub motoorse närviimpulsi mõjul, mis on piki närvikiudu leviv membraani suurenenud läbilaskvuse laine.
See suurenenud läbilaskvuse laine kandub neuromuskulaarse ristmiku kaudu sarkoplasmaatilise retikulumi T-süsteemi ja jõuab lõpuks tsisternideni, mis sisaldavad suures kontsentratsioonis kaltsiumioone. Mahutite seinte läbilaskvuse olulise suurenemise tulemusena väljuvad kaltsiumiioonid paakidest ja nende kontsentratsioon sarkoplasmas väga lühikese aja jooksul (umbes 3 ms) suureneb 1000 korda. Kõrge kontsentratsiooniga kaltsiumiioonid kinnituvad õhukeste filamentide valgu - troponiini - külge ja muudavad selle ruumilist kuju (konformatsiooni). Troponiini konformatsiooni muutumine viib omakorda selleni, et tropomüosiini molekulid nihkuvad mööda fibrillaarse aktiini soont, mis moodustab õhukeste filamentide aluse, ja vabastab aktiini molekulide sidumisala. müosiinipeadele. Selle tulemusena ilmub müosiini ja aktiini vahele (st paksude ja õhukeste filamentide vahele) põiksild, mis asub 90 ° nurga all. Kuna suur hulk müosiini ja aktiini molekule (igaüks umbes 300) sisaldub paksudes ja õhukestes filamentides, moodustub lihaskiudude vahel üsna palju põikisildu ehk adhesioone. Aktiini ja müosiini vahelise sideme moodustumisega kaasneb viimase ATPaasi aktiivsuse suurenemine, mille tulemuseks on ATP hüdrolüüs:
ATP + H 2 0 ADP + H 3 P0 4 + energia
ATP lõhenemisel vabaneva energia tõttu pöördub müosiinipea nagu paadi liigend või aer ning jämedate ja õhukeste filamentide vaheline sild on 45° nurga all, mis viib lihase libisemiseni. filamendid üksteise poole. Pärast pöörde sooritamist katkevad sillad jämedate ja õhukeste niitide vahel. Selle tulemusena väheneb müosiini ATPaasi aktiivsus järsult ja ATP hüdrolüüs peatub. Kuid kui motoorne närviimpulss jätkab lihasesse sisenemist ja sarkoplasmasse jääb kõrge kaltsiumiioonide kontsentratsioon, moodustuvad uuesti ristsillad, suureneb müosiini ATPaasi aktiivsus ja taas toimub ATP uute osade hüdrolüüs, mis annab energiat pööramiseks. ristsillad koos nende järgneva purunemisega. See toob kaasa jämedate ja õhukeste niitide edasise liikumise üksteise suunas ning müofibrillide ja lihaskiudude lühenemise.
Hariduslik – metoodilinekeerulinepealdistsipliini peal pealbiokeemia. 2. Järgmine...
Haridus-metoodiline kompleks erialade kaupa (83)
Koolitus- ja metodoloogiakompleksOsakonnad) Täisnimi Autor_____Rodina Elena Jurievna____________________________________ hariv-metoodilinekeerulinepealdistsipliini MOLEKULAARBIOLOOGIA (nimi) Eriala... õpikutega peal näidatud molekulaarbioloogia õpikud pealbiokeemia. 2. Järgmine...
Inimkehas võivad rasvade biosünteesi lähteaineks olla toidust saadavad süsivesikud, taimedes aga fotosünteesi kudedest saadav sahharoos. Näiteks rasvade (triatsüülglütseroolide) biosüntees valmivates õliseemnetes on samuti tihedalt seotud süsivesikute ainevahetusega. Küpsemise varases staadiumis on seemnete põhikudede - idulehtede ja endospermi - rakud täidetud tärkliseteradega. Alles siis, hilisemates küpsemise faasides, asendatakse tärklise terad lipiididega, mille põhikomponendiks on triatsüülglütserool.
Rasvasünteesi peamised etapid hõlmavad glütserool-3-fosfaadi ja rasvhapete moodustumist süsivesikutest ning seejärel estersidemeid glütserooli alkoholirühmade ja rasvhapete karboksüülrühmade vahel:
Joonis 11 – Üldskeem rasva sünteesiks süsivesikutest
Vaatleme üksikasjalikumalt süsivesikutest rasva sünteesi põhietappe (vt joonis 12).
Glütserool-3-fosfaadi süntees
I etapp – vastavate glükosidaaside toimel hüdrolüüsitakse süsivesikuid koos monosahhariidide moodustumisega (vt punkt 1.1.), mis osalevad glükolüüsi protsessis rakkude tsütoplasmas (vt joonis 2). Glükolüüsi vaheproduktid on fosfodioksüatsetoon ja 3-fosfoglütseraldehüüd.
II etapp. Glütserool-3-fosfaat moodustub glükolüüsi vaheprodukti fosfodioksüatsetooni redutseerimise tulemusena:

Lisaks võib fotosünteesi pimedas faasis tekkida glütsero-3-fosfaat.
Lipiidide ja süsivesikute vaheline seos
Rasvade süntees süsivesikutest

Joonis 12 – süsivesikute lipiidideks muundamise skeem
Rasvhapete süntees
Rasvhapete sünteesi ehitusplokk raku tsütosoolis on atsetüül-CoA, mis tekib kahel viisil: kas püruvaadi oksüdatiivse dekarboksüülimise tulemusena. (vt joonis 12, III etapp), või rasvhapete -oksüdatsiooni tulemusena (vt joonis 5). Tuletame meelde, et glükolüüsi käigus moodustunud püruvaadi muundumine atsetüül-CoA-ks ja selle moodustumine rasvhapete β-oksüdatsiooni käigus toimub mitokondrites. Rasvhapete süntees toimub tsütoplasmas. Mitokondrite sisemembraan on atsetüül-CoA-le mitteläbilaskev. Selle sisenemine tsütoplasmasse toimub hõlbustatud difusiooni tüübi abil tsitraadi või atsetüülkarnitiini kujul, mis tsütoplasmas muundatakse atsetüül-CoA-ks, oksaloatsetaadiks või karnitiiniks. Kuid peamine viis atsetüül-coA ülekandmiseks mitokondritest tsütosooli on tsitraat (vt joonis 13).
Esialgu interakteerub intramitokondriaalne atsetüül-CoA oksaloatsetaadiga, mille tulemusena moodustub tsitraat. Reaktsiooni katalüüsib ensüüm tsitraadi süntaas. Saadud tsitraat transporditakse spetsiaalse trikarboksülaadi transpordisüsteemi abil läbi mitokondriaalse membraani tsütosooli.
Tsütosoolis reageerib tsitraat HS-CoA ja ATP-ga, lagunedes uuesti atsetüül-CoA-ks ja oksaloatsetaadiks. Seda reaktsiooni katalüüsib ATP-tsitraatlüaas. Juba tsütosoolis naaseb oksaloatsetaat tsütosoolse dikarboksülaadi transpordisüsteemi osalusel mitokondriaalsesse maatriksisse, kus see oksüdeeritakse oksaloatsetaadiks, viies sellega lõpule nn süstikutsükli:

Joonis 13 – atsetüül-CoA mitokondritest tsütosooli ülekande skeem
Küllastunud rasvhapete biosüntees toimub nende -oksüdatsioonile vastupidises suunas, rasvhapete süsivesinike ahelate kasv toimub kahe süsiniku fragmendi (C 2) - atsetüül-CoA järjestikuse lisamise tõttu nende otstesse. (vt joonis 12, etapp IV).
Rasvhapete biosünteesi esimene reaktsioon on atsetüül-CoA karboksüülimine, milleks on vaja CO 2, ATP, Mn ioone. Seda reaktsiooni katalüüsib ensüüm atsetüül-CoA-karboksülaas. Ensüüm sisaldab proteesrühmana biotiini (H-vitamiini). Reaktsioon toimub kahes etapis: 1 - biotiini karboksüülimine ATP ja II osalusel - karboksüülrühma ülekandmine atsetüül-CoA-le, mille tulemusena moodustub malonüül-CoA:

Malonüül-CoA on esimene spetsiifiline rasvhapete biosünteesi produkt. Sobiva ensüümsüsteemi juuresolekul muundub malonüül-CoA kiiresti rasvhapeteks.
Tuleb märkida, et rasvhapete biosünteesi kiiruse määrab suhkrute sisaldus rakus. Glükoosi kontsentratsiooni suurenemine inimeste, loomade rasvkoes ja glükolüüsi kiiruse suurenemine stimuleerib rasvhapete sünteesi. See näitab, et rasvade ja süsivesikute ainevahetus on omavahel tihedalt seotud. Olulist rolli mängib siin atsetüül-CoA karboksüülimise reaktsioon selle muundumisega malonüül-CoA-ks, mida katalüüsib atsetüül-CoA karboksülaas. Viimaste aktiivsus sõltub kahest tegurist: suure molekulmassiga rasvhapete ja tsitraadi olemasolust tsütoplasmas.
Rasvhapete akumuleerumine pärsib nende biosünteesi; pärsivad karboksülaasi aktiivsust.
Eriline roll on tsitraadil, mis on atsetüül-CoA karboksülaasi aktivaator. Tsitraat mängib samal ajal seost süsivesikute ja rasvade ainevahetuse vahel. Tsütoplasmas on tsitraadil rasvhapete sünteesi stimuleerimisel kahekordne toime: esiteks atsetüül-CoA karboksülaasi aktivaatorina ja teiseks atsetüülrühmade allikana.
Rasvhapete sünteesi väga oluline tunnus on see, et kõik sünteesi vaheühendid on kovalentselt seotud atsüülkandjavalguga (HS-ACP).
HS-ACP on madala molekulmassiga valk, mis on termostabiilne, sisaldab aktiivset HS-rühma ja mille proteesrühmas on pantoteenhape (vitamiin B3). HS-ACP funktsioon on sarnane ensüümi A (HS-CoA) funktsiooniga rasvhapete β-oksüdatsioonis.
Rasvhappeahela ehitamisel moodustavad vaheühendid estersidemeid loomsete kõrvalsaaduste ahelaga (vt joonis 14):

Rasvhappeahela pikenemise tsükkel sisaldab nelja reaktsiooni: 1) atsetüül-APB (C2) kondenseerimine malonüül-APB-ga (C3); 2) taastumine; 3) dehüdratsioon ja 4) rasvhapete teine taastumine. Joonisel fig. 14 on näidatud rasvhapete sünteesi skeem. Üks rasvhappeahela pikendamise tsükkel hõlmab nelja järjestikust reaktsiooni.

Joonis 14 - Rasvhapete sünteesi skeem
Esimeses reaktsioonis (1) - kondensatsioonireaktsioonis - interakteeruvad atsetüül- ja malonüülrühmad üksteisega, moodustades atsetoatsetüül-ABP koos samaaegse CO 2 (C 1) vabanemisega. Seda reaktsiooni katalüüsib kondenseeruv ensüüm -ketoatsüül-ABP süntetaas. Malonüül-APB-st lõhustatud CO2 on sama CO2, mis osales atsetüül-APB karboksüülimisreaktsioonis. Seega tekib kondensatsioonireaktsiooni tulemusena kahe (C 2) ja kolme süsiniku (C 3) komponendist neljasüsinikuline ühend (C 4).
Teises reaktsioonis (2) muudetakse -ketoatsüül-ACP reduktaasi, atsetoatsetüül-ACP poolt katalüüsitud redutseerimisreaktsioon -hüdroksübutürüül-ACB-ks. Redutseerija on NADPH + H +.
Dehüdratsioonitsükli kolmandas reaktsioonis (3) eraldub veemolekul -hüdroksübutürüül-APB-st, moodustades krotonüül-APB. Reaktsiooni katalüüsib -hüdroksüatsüül-ACP dehüdraas.
Tsükli neljas (viimane) reaktsioon (4) on krotoniil-APB redutseerimine butürüül-APB-ks. Reaktsioon kulgeb enoüül-ACP reduktaasi toimel. Redutseerija rolli täidab siin teine molekul NADPH + H + .
Seejärel korratakse reaktsioonide tsüklit. Oletame, et palmitiinhapet (C 16) sünteesitakse. Sel juhul viiakse butürüül-ACB moodustumine lõpule alles esimese 7-st tsüklist, millest igaühe algus on molonüül-ACB molekuli (3) lisamine - reaktsioon (5) kasvu karboksüülotsa. rasvhapete ahel. Sel juhul eraldatakse karboksüülrühm CO 2 (C1) kujul. Seda protsessi saab kujutada järgmiselt:
C 3 + C 2 C 4 + C 1 - 1 tsükkel
C 4 + C 3 C 6 + C 1 - 2 tsükkel
C 6 + C 3 C 8 + C 1 -3 tsükkel
C 8 + C 3 C 10 + C 1 - 4 tsükkel
C 10 + C 3 C 12 + C 1 - 5 tsükkel
C 12 + C 3 C 14 + C 1 - 6 tsükkel
C 14 + C 3 C 16 + C 1 - 7 tsükkel
Sünteesida saab mitte ainult kõrgemaid küllastunud rasvhappeid, vaid ka küllastumata rasvhappeid. Monoküllastumata rasvhapped tekivad küllastunud rasvhapetest oksüdatsiooni (desaturatsiooni) tulemusena, mida katalüüsib atsüül-CoA oksügenaas. Erinevalt taimsetest kudedest on loomsetel kudedel väga piiratud võime muuta küllastunud rasvhappeid küllastumata rasvhapeteks. On kindlaks tehtud, et kaks levinumat monoküllastumata rasvhapet, palmitooleiin- ja oleiinhape, sünteesitakse palmitiin- ja steariinhappest. Imetajate, sealhulgas inimeste kehas ei saa steariinhappest (C 18:0) tekkida näiteks linoolhape (C 18:2) ja linoleenhape (C 18:3). Need happed on klassifitseeritud asendamatuteks rasvhapeteks. Asendamatute rasvhapete hulka kuulub ka arahhiidhape (C 20:4).
Koos rasvhapete desaturatsiooniga (kaksiksidemete moodustumine) toimub ka nende pikenemine (pikenemine). Lisaks saab neid mõlemaid protsesse kombineerida ja korrata. Rasvhappeahela pikenemine toimub kahe süsiniku fragmendi järjestikuse lisamisega vastavale atsüül-CoA-le malonüül-CoA ja NADPH+H+ osalusel.
Joonisel 15 on kujutatud palmitiinhappe transformatsiooniteed desaturatsiooni- ja pikenemisreaktsioonides.

Joonis 15 – Küllastunud rasvhapete muundamise skeem
küllastumatuks
Mis tahes rasvhappe süntees viiakse lõpule HS-ACP lõhustamisega atsüül-ACB-st deatsülaasi ensüümi mõjul. Näiteks:

Saadud atsüül-CoA on aktiivne vorm rasvhape.
Rasvad sünteesitakse glütseroolist ja rasvhapetest.
Glütseriin tekib organismis rasvade (toidu ja enda) lagunemisel ning moodustub kergesti ka süsivesikutest.
Rasvhapped sünteesitakse atsetüülkoensüümist A. Atsetüülkoensüüm A on universaalne metaboliit. Selle sünteesiks on vaja vesinikku ja ATP energiat. Vesinik saadakse NADP.H2-st. Kehas sünteesitakse ainult küllastunud ja monoküllastunud (ühe kaksiksidemega) rasvhappeid. Rasvhapped, mille molekulis on kaks või enam kaksiksidet, mida nimetatakse polüküllastumata rasvhapeteks, ei sünteesita kehas ja neid tuleb varustada toiduga. Rasva sünteesiks võib kasutada rasvhappeid – toidu ja enda rasvade hüdrolüüsi saadusi.
Kõik rasva sünteesis osalejad peavad olema aktiivses vormis: glütserool kujul glütserofosfaat, ja rasvhapped kujul atsetüülkoensüüm A. Rasvade süntees toimub rakkude tsütoplasmas (peamiselt rasvkoes, maksas, peensooles) Rasvade sünteesi teed on näidatud diagrammil.
Tuleb märkida, et glütserooli ja rasvhappeid saab süsivesikutest. Seetõttu tekib nende liigsel tarbimisel istuva eluviisi taustal rasvumine.
DAP - dihüdroatsetoonfosfaat,
DAG on diatsüülglütserool.
TAG, triatsüülglütserool.
üldised omadused lipoproteiinid. Veekeskkonnas (ja seega ka veres) olevad lipiidid on lahustumatud, seetõttu moodustuvad lipiidide transportimiseks verega kehas lipiidide kompleksid valkudega - lipoproteiinid.
Igat tüüpi lipoproteiinidel on sarnane struktuur – hüdrofoobne tuum ja hüdrofiilne kiht pinnal. Hüdrofiilse kihi moodustavad valgud, mida nimetatakse apoproteiinideks, ja amfifiilsed lipiidimolekulid, mida nimetatakse fosfolipiidideks ja kolesterooliks. Nende molekulide hüdrofiilsed rühmad on suunatud vesifaasi poole, samas kui hüdrofoobsed osad on suunatud lipoproteiini hüdrofoobse tuuma poole, mis sisaldab transporditavaid lipiide.
Apoproteiinid täidab mitmeid funktsioone:
Moodustab lipoproteiinide struktuuri;
Suhelge rakkude pinnal olevate retseptoritega ja määrake seega, millised koed seda tüüpi lipoproteiine hõivavad;
Toimib ensüümide või ensüümide aktivaatoritena, mis toimivad lipoproteiinidele.
Lipoproteiinid. Organismis sünteesitakse järgmist tüüpi lipoproteiine: külomikronid (XM), väga madala tihedusega lipoproteiinid (VLDL), keskmise tihedusega lipoproteiinid (IDL), madala tihedusega lipoproteiinid (LDL) ja kõrge tihedusega lipoproteiinid (HDL). Iga LP tüüp on moodustub erinevates kudedes ja transpordib teatud lipiide. Näiteks XM transpordib eksogeenseid (toidurasvu) soolestikust kudedesse, nii et triatsüülglütseroolid moodustavad kuni 85% nende osakeste massist.
lipoproteiinide omadused. LP lahustuvad veres hästi, ei ole opalestseeruvad, kuna neil on väike suurus ja negatiivne laeng.
pinnad. Mõned ravimid läbivad kergesti veresoonte kapillaaride seinu ja viivad rakkudesse lipiide. HM suur suurus ei võimalda neil tungida läbi kapillaaride seinte, mistõttu sisenevad nad kõigepealt soolerakkudest. lümfisüsteem ja seejärel läbi peamise rindkere kanali voolavad koos lümfiga verre. Rasvhapete, glütserooli ja jääkülomikronite saatus. LP-lipaasi toimel XM rasvadele tekivad rasvhapped ja glütserool. Põhiline rasvhapete mass tungib kudedesse. Rasvkoes ladestuvad imendumisperioodil rasvhapped triatsüülglütseroolide kujul, südamelihases ja töötavates skeletilihastes kasutatakse neid energiaallikana. Teine rasvade hüdrolüüsi produkt, glütserool, lahustub veres ja transporditakse maksa, kus seda saab imendumisperioodil kasutada rasvade sünteesiks.
Hüperkülomikroneemia, hüpertriglütseroneemia. Pärast rasvu sisaldava toidu allaneelamist tekib füsioloogiline hüpertriglütseroneemia ja vastavalt hüperkülomikroneemia, mis võib kesta kuni mitu tundi HM-i vereringest eemaldamise kiirus sõltub:
LP-lipaasi aktiivsus;
HDL-i olemasolu, mis varustab HM-i apoproteiine C-II ja E;
ApoC-II ja apoE tegevuste ülekandmine HM-is.
Mis tahes CM metabolismis osaleva valgu geneetilised defektid põhjustavad perekondliku hüperkülomikroneemia, I tüüpi hüperlipoproteineemia arengut.
Sama liigi taimede puhul võib rasva koostis ja omadused varieeruda sõltuvalt kasvu kliimatingimustest. Rasvade sisaldus ja kvaliteet loomses tooraines oleneb ka tõust, vanusest, rasvumusastmest, soost, aastaajast jne.
Rasvu kasutatakse laialdaselt paljude toiduainete valmistamisel, need on kõrge kalorsusega ja toiteväärtusega, tekitavad pikaajalist küllastustunnet. Rasvad on toidu valmistamise protsessis olulised maitse- ja struktuurikomponendid, millel on oluline mõju välimus toit. Praadimisel täidab rasv soojuskandja rolli.
|
Toote nimi |
Toote nimi |
Ligikaudne rasvade sisaldus toiduainetes, % märgmassist |
|
|
rukkileib | |||
|
Päevalill |
Värsked köögiviljad | ||
|
Värsked puuviljad | |||
|
Veiseliha | |||
|
kakao oad | |||
|
maapähkli pähklid |
Lambaliha | ||
|
Kreeka pähklid (tuumad) |
Kala | ||
|
Teravili: |
lehmapiim | ||
|
Või | |||
|
Margariin | |||
Taimsetest ja loomsetest kudedest saadud rasvad võivad lisaks glütseriididele sisaldada vabu rasvhappeid, fosfatiide, steroole, pigmente, vitamiine, lõhna- ja maitseaineid, ensüüme, valke jne, mis mõjutavad rasvade kvaliteeti ja omadusi. Rasvade maitset ja lõhna mõjutavad ka säilitamisel rasvades tekkivad ained (aldehüüdid, ketoonid, peroksiid jt ühendid).
Inimese kehas olevaid rasvu tuleb toiduga pidevalt varustada. Rasvade vajadus sõltub vanusest, töö iseloomust, kliimatingimustest ja muudest teguritest, kuid keskmiselt vajab täiskasvanu päevas 80–100 g rasva. Igapäevane toit peaks sisaldama ligikaudu 70% loomseid ja 30% taimseid rasvu.
Rasvad sünteesitakse glütseroolist ja rasvhapetest.
Glütseriin tekib organismis rasvade (toidu ja enda) lagunemisel ning moodustub kergesti ka süsivesikutest.
Rasvhapped sünteesitakse atsetüülkoensüümist A. Atsetüülkoensüüm A on universaalne metaboliit. Selle sünteesiks on vaja vesinikku ja ATP energiat. Vesinik saadakse NADP.H2-st. Kehas sünteesitakse ainult küllastunud ja monoküllastunud (ühe kaksiksidemega) rasvhappeid. Rasvhapped, mille molekulis on kaks või enam kaksiksidet, mida nimetatakse polüküllastumata rasvhapeteks, ei sünteesita kehas ja neid tuleb varustada toiduga. Rasva sünteesiks võib kasutada rasvhappeid – toidu ja enda rasvade hüdrolüüsi saadusi.
Kõik rasva sünteesis osalejad peavad olema aktiivses vormis: glütserool kujul glütserofosfaat, ja rasvhapped kujul atsetüülkoensüüm A. Rasva süntees toimub rakkude (peamiselt rasvkoes, maksas, peensooles) tsütoplasmas. Rasvade sünteesi teed on näidatud diagrammil.
Tuleb märkida, et glütserooli ja rasvhappeid saab süsivesikutest. Seetõttu tekib nende liigsel tarbimisel istuva eluviisi taustal rasvumine.
DAP - dihüdroatsetoonfosfaat,
DAG on diatsüülglütserool.
TAG, triatsüülglütserool.
Lipoproteiinide üldised omadused. Veekeskkonnas (ja seega ka veres) olevad lipiidid on lahustumatud, seetõttu moodustuvad lipiidide transportimiseks verega kehas lipiidide kompleksid valkudega - lipoproteiinid.
Igat tüüpi lipoproteiinidel on sarnane struktuur – hüdrofoobne tuum ja hüdrofiilne kiht pinnal. Hüdrofiilse kihi moodustavad valgud, mida nimetatakse apoproteiinideks, ja amfifiilsed lipiidimolekulid, fosfolipiidid ja kolesterool. Nende molekulide hüdrofiilsed rühmad on suunatud vesifaasi poole, samas kui hüdrofoobsed osad on suunatud lipoproteiini hüdrofoobse tuuma poole, mis sisaldab transporditavaid lipiide.
Apoproteiinid täidab mitmeid funktsioone:
Moodustab lipoproteiinide struktuuri;
Suhelge rakkude pinnal olevate retseptoritega ja määrake seega, millised koed seda tüüpi lipoproteiine hõivavad;
Toimib ensüümide või ensüümide aktivaatoritena, mis toimivad lipoproteiinidele.
Lipoproteiinid. Organismis sünteesitakse järgmist tüüpi lipoproteiine: külomikronid (XM), väga madala tihedusega lipoproteiinid (VLDL), keskmise tihedusega lipoproteiinid (IDL), madala tihedusega lipoproteiinid (LDL) ja kõrge tihedusega lipoproteiinid (HDL). Iga LP tüüp on moodustub erinevates kudedes ja transpordib teatud lipiide. Näiteks XM transpordib eksogeenseid (toidurasvu) soolestikust kudedesse, nii et triatsüülglütseroolid moodustavad kuni 85% nende osakeste massist.
lipoproteiinide omadused. LP-d lahustuvad veres hästi, ei ole opalestseeruvad, kuna neil on väike suurus ja negatiivne laeng
pinnad. Mõned ravimid läbivad kergesti veresoonte kapillaaride seinu ja viivad rakkudesse lipiide. HM-i suur suurus ei võimalda neil tungida läbi kapillaaride seinte, nii et soolerakkudest satuvad nad esmalt lümfisüsteemi ja seejärel läbi peamise rindkere kanali koos lümfiga verre. Rasvhapete, glütserooli ja jääkülomikronite saatus. LP-lipaasi toimel XM rasvadele tekivad rasvhapped ja glütserool. Põhiline rasvhapete mass tungib kudedesse. Rasvkoes ladestuvad imendumisperioodil rasvhapped triatsüülglütseroolide kujul, südamelihases ja töötavates skeletilihastes kasutatakse neid energiaallikana. Teine rasvade hüdrolüüsi produkt, glütserool, lahustub veres ja transporditakse maksa, kus seda saab imendumisperioodil kasutada rasvade sünteesiks.
Hüperkülomikroneemia, hüpertriglütseroneemia. Pärast rasvu sisaldava toidu allaneelamist tekib füsioloogiline hüpertriglütseroneemia ja vastavalt hüperkülomikroneemia, mis võib kesta kuni mitu tundi HM-i vereringest eemaldamise kiirus sõltub:
LP-lipaasi aktiivsus;
HDL-i olemasolu, mis varustab HM-i apoproteiine C-II ja E;
ApoC-II ja apoE tegevuste ülekandmine HM-is.
Mis tahes CM metabolismis osaleva valgu geneetilised defektid põhjustavad perekondliku hüperkülomikroneemia, I tüüpi hüperlipoproteineemia arengut.
Sama liigi taimede puhul võib rasva koostis ja omadused varieeruda sõltuvalt kasvu kliimatingimustest. Rasvade sisaldus ja kvaliteet loomses tooraines oleneb ka tõust, vanusest, rasvumusastmest, soost, aastaajast jne.
Rasvu kasutatakse laialdaselt paljude toiduainete valmistamisel, need on kaloririkkad ja toiteväärtus põhjustada pikaajalist küllastustunnet. Rasvad on toidu valmistamise protsessis olulised maitse- ja struktuurikomponendid, millel on oluline mõju toidu välimusele. Praadimisel täidab rasv soojuskandja rolli.
| Toote nimi | Toote nimi | Ligikaudne rasvasisaldus toiduained, % märgkaal | |
| Seemned: | rukkileib | 1,20 | |
| Päevalill | 35-55 | Värsked köögiviljad | 0,1-0,5 |
| kanep | 31-38 | Värsked puuviljad | 0,2-0,4 |
| moon | Veiseliha | 3,8-25,0 | |
| kakao oad | Sealiha | 6,3-41,3 | |
| maapähkli pähklid | 40-55 | Lambaliha | 5,8-33,6 |
| Kreeka pähklid (tuumad) | 58-74 | Kala | 0,4-20 |
| Teravili: | lehmapiim | 3,2-4,5 | |
| Nisu | 2,3 | Või | 61,5-82,5 |
| Rukis | 2,0 | Margariin | 82,5 |
| kaer | 6,2 | Munad | 12,1 |
Taimsetest ja loomsetest kudedest saadud rasvad võivad lisaks glütseriididele sisaldada vabu rasvhappeid, fosfatiide, steroole, pigmente, vitamiine, lõhna- ja maitseaineid, ensüüme, valke jne, mis mõjutavad rasvade kvaliteeti ja omadusi. Rasvade maitset ja lõhna mõjutavad ka säilitamisel rasvades tekkivad ained (aldehüüdid, ketoonid, peroksiid jt ühendid).
Rasvadest süsivesikute sünteesi protsessi saab kujutada üldise skeemi abil:
Joonis 7 – Üldskeem süsivesikute sünteesiks rasvadest
Üks peamisi lipiidide laguprodukte, glütserool, on kergesti kasutatav süsivesikute sünteesil glütseraldehüüd-3-fosfaadi moodustumisel ja selle sisenemisel gluneogeneesi. Taimedes ja mikroorganismides on see kergesti kasutatav ka süsivesikute ja teise olulise lipiidide laguprodukti – rasvhapete (atsetüül-CoA) sünteesiks läbi glüoksülaadi tsükli.
Aga üldine skeem ei kajasta kõiki biokeemilisi protsesse, mis tekivad rasvadest süsivesikute moodustumisel.
Seetõttu kaalume selle protsessi kõiki etappe.
Süsivesikute ja rasvade sünteesi skeem on üksikasjalikumalt esitatud joonisel 8 ja see toimub mitmes etapis.
1. etapp. Rasva hüdrolüütiline lagunemine lipaasi ensüümi toimel glütserooliks ja kõrgemateks rasvhapeteks (vt punkt 1.2). Hüdrolüüsiproduktid peavad pärast rea muundumist muutuma glükoosiks.

Joonis 8 – Rasvadest süsivesikute biosünteesi skeem
2. etapp. Kõrgemate rasvhapete muundumine glükoosiks. Kõrgemad rasvhapped, mis tekkisid rasvade hüdrolüüsi tulemusena, hävivad peamiselt b-oksüdatsiooni teel (seda protsessi käsitleti varem punktis 1.2, lõigus 1.2.2). Selle protsessi lõpptooteks on atsetüül-CoA.
Glüoksülaadi tsükkel
Taimed, mõned bakterid ja seened võivad kasutada atsetüül-CoA-d mitte ainult Krebsi tsüklis, vaid ka tsüklis, mida nimetatakse glüoksülaadiks. See tsükkel mängib olulist rolli lülina rasvade ja süsivesikute ainevahetuses.
Glüoksülaadi tsükkel toimib eriti intensiivselt spetsiaalsetes rakulistes organellides, glüoksisoomides, õliseemnete idanemise ajal. Sel juhul muudetakse rasv seemiku arenguks vajalikeks süsivesikuteks. See protsess toimib seni, kuni seemikul tekib fotosünteesivõime. Kui varurasv on idanemise lõpus ammendunud, kaovad rakus olevad glüoksisoomid.
Glüoksülaadi rada on spetsiifiline ainult taimede ja bakterite jaoks, loomorganismides see puudub. Glüoksülaadi tsükli toimimise võimalikkus on tingitud asjaolust, et taimed ja bakterid on võimelised sünteesima ensüüme nagu nt. isotsitraatlüaas ja malaadi süntaas, mis koos mõnede Krebsi tsükli ensüümidega osalevad glüoksülaadi tsüklis.
Atsetüül-CoA oksüdatsiooni skeem glüoksülaadi raja kaudu on näidatud joonisel 9.

Joonis 9 - Glüoksülaadi tsükli skeem
Glüoksülaadi tsükli kaks algreaktsiooni (1 ja 2) on identsed trikarboksüülhappe tsükli reaktsioonidega. Esimeses reaktsioonis (1) kondenseeritakse atsetüül-CoA tsitraadi süntaasi abil oksaloatsetaadiga, moodustades tsitraadi. Teises reaktsioonis isomeriseerub tsitraat isotsitraadiks akonitaathüdrataasi osalusel. Järgmised glüoksülaadi tsüklile omased reaktsioonid katalüüsivad spetsiaalsed ensüümid. Kolmandas reaktsioonis lõhustatakse isotsitraat isotsitraatlüaasi toimel glüoksüülhappeks ja merevaikhappeks:

Neljanda reaktsiooni käigus, mida katalüüsib malaadi süntaas, kondenseerub glüoksülaat atsetüül-CoA-ga (teine atsetüül-CoA molekul, mis siseneb glüoksülaadi tsüklisse), moodustades õunhappe (malaadi):

Seejärel oksüdeeritakse malaat viiendas reaktsioonis oksaloatsetaadiks. See reaktsioon on identne trikarboksüülhappe tsükli lõppreaktsiooniga; see on ka glüoksülaadi tsükli viimane reaktsioon, sest saadud oksaloatsetaat kondenseerub uuesti uue atsetüül-CoA molekuliga, alustades seeläbi tsükli uut pööret.
Glüoksülaadi tsükli kolmandas reaktsioonis tekkinud merevaikhapet selles tsüklis ei kasutata, vaid see läbib edasisi muundumisi.