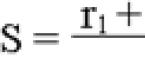ЗАНЯТИЕ 18
ПАТОЛОГИЯ ОБЩЕГО ОБЪЕМА КРОВИ. КРОВОПОТЕРЯ.
Патология общего объема крови. Классификация нарушений (по характеру нарушения объема циркулирующей крови и гематокритному показателю).
В норме общий объем крови составляет 6-8 % (1/13) массы тела, причем 1/3 этого объема депонирована в капиллярах и венозном отделе сосудистого русла скелетной мускулатуры, брыжейки, печени, селезенки и в случае необходимости (физическая нагрузка, кровопотеря и др.) поступает в циркуляторное русло.
Относительная плотность крови – 1050-1060 у.е., причем плотность плазмы составляет 1025-1034 у.е., а плотность форменных элементов – 1090 у.е.
Объем циркулирующей крови (ОЦК) является важным показателем гемодинамики, определяющим величину артериального давления. Его постоянство обеспечивается сложной регуляторной системой, включающей нервные и гуморальные механизмы.
Около 70% всего ОЦК находится в венах, 15% – в артериях, 12% – в капиллярах, 3% – в камерах сердца). До 75-80 % ОЦК находится в большом круге кровообращения, а 20-25 % – в малом.
Гематокритное число (условно «гематокрит» – Hct) – объемный процент форменных элементов от объема крови. В норме Hct равен 36% – 48%. В системе СИ гематокрит (Ht) выражают как 0,36-0,48.
При различных патологических состояниях может измениться как общий объем крови, так и Hct.
Выделяют три группы типовых форм нарушений: нормоволемия, гиповолемия и гиперволемия (плетора, полнокровие).
Нормоволемия
Гиперволемия
Гиповолемия – состояние, характеризующееся уменьшением ОЦК ниже соответствующих норм.
В зависимости от характера изменения Hct выделяют следующие виды гипо-, гипер- или нормоволемий:
·
· полицитемическую (Hct > 0,48),
· олигоцитемическую (Hct < 0,36).
Последствия изменения гематокритного показателя:
Снижение гематокритного показателя сопровождается снижением вязкости крови, при гиповолемических состояниях – развитием гемической гипоксии.
Полицитемические состояния, независимо от характера изменения ОЦК, характеризуются образованием агрегатов эритроцитов (сладж-синдром), тромбообразованием, ухудшением реологических свойств крови, что приводит к снижению перфузии капиллярного русла, нарушению микроциркуляции, развитию полиорганной недостаточности.
Изменение объема циркулирующей крови
Заштрихованная часть полосок соответствует гематокриту, а их общая длина – общему объему крови. 1-9 – основные типовые изменения:
1 – простая нормоволемия,
2 – олигоцитемическая нормоволемия,
3 – полицитемическая нормоволемия,
4 – простая гиперволемия,
5 – олигоцитемическая гиперволемия,
6 – полицитемическая гиперволемия,
7 – нормоцитемическая гиповолемия,
8 – олигоцитемическая гиповолемия,
9 – полицитемическая гиповолемия.
Нормоволемия. Виды, причины, последствия для организма.
Нормоволемия – состояние, при котором ОЦК соответствует среднестатистической норме, свойственной индивидуумам данной массы тела, пола и возраста.
В зависимости от характера изменения Hct выделяют следующие виды нормоволемий:
· простую (нормоцитемическую) (Hct в норме),
· полицитемическую (Hct > 0,48),
· олигоцитемическую (Hct < 0,36).
Простая нормоволемия наблюдается в обычном состоянии у здорового человека.
К нормоволемическим нарушениям относят состояния, при которых ОЦК сохраняется нормальным, но изменяется Hct .
Олигоцитемическая нормоволемия характеризуется снижением Hct на фоне нормального ОЦК. Наиболее часто является следствием разрушения эритроцитов, угнетения эритропоэза, а также отмечается во 2-ю (гидремическую) стадию компенсации острой кровопотери, когда ОЦК сравнительно быстро нормализуется в результате перехода жидкости из тканевого пространства в кровь, а число форменных элементов крови еще остается сниженным.
Проявления олигоцитемической нормоволемии определяются, главным образом, степенью снижения количества эритроцитов и выраженностью гемической гипоксии.
Полицитемическая нормоволемия характеризуется увеличением числа форменных элементов на фоне нормального ОЦК, и, следовательно, гематокрита. Данное нарушение может развиться при переливании эритроцитарной массы, в результате активации эритропоэза (у жителей высокогорья, болезни Вакеза).
Полицитемическая нормоволемия проявляется повышением артериального давления в связи с повышением вязкости крови и периферического сопротивления.
Гиперволемия. Виды, причины развития, последствия для организма.
Гиперволемия – состояние, при котором ОЦК превышает среднестатистические нормы.
В зависимости от характера изменения Hct выделяют следующие виды гиперволемий:
· простую (нормоцитемическую) (Hct в норме),
· полицитемическую (Hct > 0,48),
· олигоцитемическую (Hct < 0,36).
Для гиперволемий характерно увеличение сердечного выброса и артериального давления, что может привести к сердечной недостаточности.
Простая гиперволемия встречается редко и является следствием пропорциональногоувеличения объема форменных элементов и жидкой части крови, в связи с чем гематокрит остается в пределах нормы. Наблюдается при физических нагрузках, а также может развиться при переливании больших количеств донорской крови, острых гипоксических состояниях вследствие выброса крови из депо.
Олигоцитемическая гиперволемия представляет собой увеличение ОЦК вследствие преимущественного возрастания объема плазмы и снижением Hct. Физиологическим состоянием, при котором развивается олигоцитемическая гиперволемия, является беременность. Во время беременности ОЦК возрастает на 30-40% от исходного, при этом гематокрит снижается до 28-32%, что улучшает микроциркуляцию и обеспечивает нормальный трансплацентарный обмен.
Как патологическое состояние олигоцитемическая гиперволемия является результатом либо избыточного поступления жидкости в организм (патологическая жажда, гиперинфузия плазмы или плазмозаменителей), либо снижения выведения жидкости из организма (в результате нарушения экскреторной функции почек, при гиперпродукции антидиуретического гормона и др.).
Введение физраствора в объеме, 15-кратно превосходящем ОЦК, не приводит к повышению АД вследствие включения механизмов компенсации.
Полицитемическая гиперволемия характеризуется увеличением ОЦК вследствие преимущественного повышении количества эритроцитов крови, в связи с чем гематокрит повышается, возрастает вязкость крови, что ведет к повышению артериального давлении и вызывает нарушение микроциркуляции, а также повышает сердечный выброс и способствует развитию сердечной недостаточности. Полицитемическая гиперволемия развивается при эритремии (болезнь Вакеза), некоторых видах хронической гипоксии (пороки сердца и др.).
Открытый артериальный проток (ОАП) – наличие сообщения между аортой и лёгочной артерией, считающегося аномалией в постнатальном периоде.
Частота данного порока колеблется в пределах от 5 до 34%, чаще у лиц женского пола (2-4:1).
Как правило, ОАП сочетается с другими врожденными пороками сердца – коарктацией аорты, ДМЖП.
При дуктус-зависимых пороках сердца (ТМА, крайняя форма тетрады Фалло, критический стеноз аорты и лёгочной артерии, перерыв дуги аорты, синдром гипоплазии левого желудочка) данная сердечная аномалия является жизненно необходимой.
ОАП, в отличие от сосудов магистрального типа кровообращения, является сосудом мышечного типа с мощной вагусной иннервацией, что обеспечивает его способность к сокращению в раннем неонатальном периоде.
Гемодинамика .
В пренатальном периоде открытый артериальный проток и открытое овальное окно являются физиологическими плодовыми коммуникациями.
В силу того, что малый круг кровообращения не функционирует, около 2/3 объёма оксигенированной крови через открытый артериальный проток поступает в нисходящую аорту. В норме, вскоре после рождения, в открытом артериальном протоке происходит спазм гладкомышечных волокон, что приводит к функциональному закрытию протока. Анатомическое закрытие или облитерация происходит в течение первых 2-х недель постнатальной жизни.
Такие патологические состояния периода новорожденности как синдром дыхательных расстройств, врождённая пневмония, асфиксия в родах препятствуют закрытию ОАП. Физиологическое закрытие протока задерживается у недоношенных детей, причём чем меньше гестационный возраст ребёнка, тем более продолжительное время требуется для закрытия ОАП. Так, при массе тела менее 1000 г у 80% детей артериальный проток функционирует в течение нескольких месяцев.
Для развития нарушений гемодинамики имеет значение размер протока, угол его отхождения от аорты, разность давлений в большом и малом кругах кровообращения. При тонком, длинном и извилистом протоке, отходящим от аорты под острым углом, создается сопротивление току крови и выраженные нарушения гемодинамики не возникают; со временем проток может облитерироваться.
Короткий и широкий артериальный проток сопровождается значительным сбросом крови из аорты в легочную артерию. Такие протоки не способны к облитерации. Дополнительный объём крови, сбрасываемый из аорты в лёгочную артерию, будет приводить к развитию диастолической перегрузки и дилатации левых отделов сердца, особенно левого предсердия, гиперволемии в лёгких с формированием легочной гипертензии.
Клиническая картина будет зависеть от размера протока.
В неонатальном периоде у ребенка выслушивается систолический шум с р. мах – во II межреберье слева от грудины. Диастолический компонент шума отсутствует из-за неонатальной лёгочной гипертензии, характерной для этого периода жизни. По той же причине в неонатальном периоде через ОАП может происходить перекрёстный сброс крови, что клинически будет выражаться в появлении цианотической окраски кожных покровов во время крика, сосания, натуживания ребенка. По мере снижения давления в малом круге кровообращения лево-правый сброс крови осуществляется как в систолу, так и в диастолу, что приводит к феномену систоло-диастолического шума с «машинным» компонентом. В старшем возрасте по мере прогрессирования лёгочной гипертензии диастолический компонент шума вновь ослабевает вплоть до полного исчезновения. К аускультативным особенностям ОАП можно отнести также усиление и расщепление II тона над легочной артерией. В конечной стадии естественного течения порока можно отметить появление диастолического шума недостаточности лёгочной артерии – шума Грехема-Стилла.
Рентгенологически отмечается увеличение размеров кардиоторакального индекса (от минимального до кардиомегалии), признаки диастолической перегрузки левых отделов (сглаженность талии, погруженность верхушки сердца в диафрагму, выбухание восходящей части аорты). Увеличение левых отделов сердца хорошо выявляется в боковой и косых проекциях с одновременным контрастированием пищевода барием. В лёгких отмечается усиление легочного рисунка.
При электрокардиографии в начальных стадиях течения ОАП. регистрируются признаки перегрузки левого предсердия и гипертрофии левого желудочка. В дальнейшем к ним присоединяются признаки перегрузки и гипертрофии правых отделов.
ЭхоКГ позволяет определить косвенные признаки наличия ОАП и визуализировать его непосредственно, измерить размеры протока, определить степень лёгочной гипертензии.
При естественном течении продолжительность жизни больных составляет 20-25 лет. После 12-месячного возраста редко происходит спонтанное закрытие артериального протока. Основными осложнениями ОАП являются сердечная недостаточность, лёгочная гипертензия, инфекционный эндокардит, аневризма аорты и\или лёгочной артерии.
Оперативное лечение подразумевает перевязку или пересечение с ушиванием аортального и лёгочного концов протока, но в последнее время применяется и катетерная эндоваскулярная окклюзия протока. Терапевтический метод лечения подразумевает применение ингибиторов простагландинов в периоде новорожденности. Индометацин можно вводить как энтерально, так и внутривенно. В последнем случае эффективность лечения составляет 88-90%. Препарат вводят из расчета 0,1-0,2 мг/кг массы тела в 1-2 приема в течение 1-3 дней. Курсовая доза не должна превышать 0,6 мг/кг. Данный метод не получил широкого распространения, так как имеет существенные ограничения и противопоказания. Индометацин обладает антиагрегационными свойствами, что может привести к внутричерепным кровоизлияниям, желудочно-кишечным кровотечениям, транзиторным ренальным дисфункциям.
Дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки (ДМЖП) — встречается наиболее часто, причём как в изолированном виде, так и в составе многих других пороков сердца. Среди ВПС частота данного порока варьирует от 27,7 до 42%. Одинаково часто встречается как у мальчиков, так и у девочек.
В межжелудочковой перегородке выделяют 3 отдела:
верхняя часть – мембранозная, прилегает к центральному фиброзному телу,
средняя часть – мышечная,
и нижняя – трабекулярная.
Соответственно этим отделам называют и дефекты межжелудочковой перегородки, однако большинство из них имеют перимембранозную локализацию (до 80%). На долю мышечных ДМЖП приходится 20%. По размерам дефекты подразделяют на большие, средние и малые. Для правильной оценки величины дефекта его размер надо сравнивать с диаметром аорты. Мелкие дефекты размером 1-2 мм, расположенные в мышечной части МЖП, называются болезнью Толочинова–Роже . Вследствие хорошей аускультативной картины и отсутствия гемодинамических нарушений для их характеристики уместно выражение: «много шума из ничего». Отдельно выделяют множественные большие дефекты МЖП, по типу «швейцарского сыра», имеющие неблагоприятное прогностическое значение.
Внутрисердечные гемодинамические нарушения при ДМЖП начинают формироваться спустя некоторое время после рождения, как правило, на 3-5 сутки жизни. В раннем неонатальном периоде шум в сердце может отсутствовать вследствие одинакового давления в правом и левом желудочках из-за так называемой неонатальной легочной гипертензии. Постепенное падение давления в системе легочной артерии и в правом желудочке создаёт разность (градиент) давлений между желудочками, вследствие чего появляется сброс крови слева-направо (из области высокого давления в область низкого давления). Дополнительный объём крови, поступающий в правый желудочек и легочную артерию, приводит к переполнению сосудов малого круга кровообращения, где развивается легочная гипертензия.
Выделяют три стадии легочной гипертензии по В.И. Бураковскому. Застой крови (гиперволемическая стадия легочной гипертензии ) может приводить к отёку легких, частому присоединению инфекции, развитию пневмоний, манифестирующих в ранние сроки жизни, имеющих тяжелое течение и плохо поддающихся лечению. Если с гиперволемией не удается справиться консервативными методами, в таких случаях проводят паллиативную операцию – суживание легочной артерии по Мюллеру. Суть операции заключается в создании временного искусственного стеноза легочной артерии, который препятствует попаданию в МКК избыточного количества крови. Однако повышенная нагрузка, падающая при этом на правый желудочек, диктует в дальнейшем (спустя 3-6 месяцев) необходимость проведения радикальной операции.
При естественном течении порока со временем в сосудах малого круга кровообращения срабатывает рефлекс Китаева (спазмирование в ответ на перерастяжение), что приводит к развитию переходной стадии лёгочной гипертензии . В этот период ребенок перестает болеть, становится более активным, начинает прибавлять в весе. Стабильное состояние пациента в эту фазу является лучшим периодом для проведения радикальной операции. Давление в легочной артерии (и соответственно в правом желудочке) в эту фазу колеблется в пределах от 30 до 70 мм.рт.ст. Аускультативная картина характеризуется уменьшением интенсивности шума при появлении акцента II тона над лёгочной артерией.
В дальнейшем, если хирургическая коррекция ВПС не проводится, начинают формироваться процессы склерозирования сосудов легких (высокая легочная гипертензия – синдром Эйзенменгера ). Этот патологический процесс не имеет обратного развития и приводит к значительному повышению давления в легочной артерии (иногда до 100-120 мм.рт.ст.). Аускультативно можно выслушать резко выраженный акцент II тона над легочной артерией («металлический» оттенок). Систолический шум становится слабо-интенсивным, а в некоторых случаях может совсем отсутствовать. На этом фоне можно зафиксировать появление нового диастолического шума, обусловленного недостаточностью клапанов лёгочной артерии (шум Грехема-Стилла). В клинической картине заболевания отмечается множество патологических признаков: сердечный «горб», расширение границ относительной сердечной тупости, больше вправо. Над легкими выслушиваются участки ослабленного и жесткого дыхания, могут встречаться свистящие хрипы. Самым характерным признаком синдрома Эйзенменгера является постепенное нарастание цианоза, — сначала периферического, а в дальнейшем и диффузного. Это происходит вследствие перекрестного сброса крови в области дефекта межжелудочковой перегородки, который при превышении давления в правом желудочке становится право-левым, т.е. меняет свое направление. Наличие у пациента третьей стадии легочной гипертензии может стать основным мотивом отказа кардиохирургов от проведения операции.
Клиническая картина при ДМЖП заключается в симптомокомплексе сердечной недостаточности, развивающейся, как правило, на 1-3 месяцах жизни (в зависимости от размеров дефекта). Кроме признаков сердечной недостаточности ДМЖП может манифестировать ранними и тяжелыми пневмониями. При осмотре ребенка можно выявить тахикардию и одышку, расширение границ относительной сердечной тупости, смещение верхушечного толчка вниз и влево. В ряде случаев определяется симптом «кошачьего мурлыканья». Систолический шум, как правило, интенсивный, высушивается над всей областью сердца, хорошо проводится на правую сторону грудной клетки и на спину с punctum maximum в IV межреберье слева от грудины. При пальпации живота определяется увеличение печени и селезенки. Изменения периферической пульсации не характерны. У детей с ДМЖП и НК, как правило, быстро развивается гипотрофия.
Диагностика любого порока сердца складывается из рентгенологического исследования органов грудной полости, электрокардиографии и двухмерной допплерэхокардиографии.
При рентгенологическом исследовании органов грудной полости описывают форму сердца и состояние легочного рисунка, определяют размер кардио-торакального индекса (КТИ). Все эти показатели имеют свои особенности при разных степенях лёгочной гипертензии. В первой (гиперволемической) стадии выявляется сглаженность талии и погруженность верхушки в диафрагму, увеличение КТИ. Со стороны легочного рисунка отмечается его усиление, нечеткость, размытость. Крайней степенью гиперволемии в лёгких является отёк лёгких. В переходной стадии лёгочной гипертензии отмечается нормализация лёгочного рисунка, некоторая стабилизация размеров КТИ. Для склеротической стадии лёгочной гипертензии характерно значительное увеличение размеров сердца, причем в основном за счёт правых отделов, увеличение правого предсердия (формирование прямого атрио-вазального угла), выбухание дуги лёгочной артерии (индекс Мура более 50%), приподнятость верхушки сердца, которая образует с диафрагмой острый угол. Со стороны лёгочного рисунка часто описывается симптом «обрубленного дерева»: яркие, чёткие, увеличенные корни, на фоне которых лёгочный рисунок прослеживается только до определённого уровня. На периферии имеет место признаки эмфиземы. Грудная клетка имеет вздутую форму, ход ребер горизонтальный, диафрагма уплощена, стоит низко.
ЭКГ имеет свои закономерности, тесно связанные с фазой течения ВПС и степенью лёгочной гипертензии. Сначала выявляются признаки перегрузки левого желудочка – повышение его активности, затем развитие его гипертрофии. С течением времени присоединяются признаки перегрузки и гипертрофии правых отделов сердца – как предсердия, так и желудочка, — это свидетельствует о высокой лёгочной гипертензии. Электрическая ось сердца всегда отклонена вправо. Могут встречаться нарушения проводимости – от признаков неполной блокады правой ножки пучка Гиса до полной атрио-вентрикулярной блокады.
При Допплер-ЭхоКГ уточняется место расположения дефекта, его размер, определяется давление в правом желудочке и лёгочной артерии. В первой стадии лёгочной гипертензии давление в ПЖ не превышает 30 мм.рт.ст., во второй стадии – от 30 до 70 мм.рт.ст., в третьей — более 70 мм.рт.ст.
Лечение данного порока подразумевает консервативную терапию сердечной недостаточности и хирургическую коррекцию порока сердца. Консервативное лечение складывается из препаратов инотропной поддержки (симпатомиметики, сердечные гликозиды), мочегонных препаратов, кардиотрофиков. В случаях высокой легочной гипертензии назначаются ингибиторы ангиотензинпревращающего фермента – капотен или каптоприл. Оперативные вмешательства подразделяются на паллиативные операции (в случае ДМЖП – операция суживания лёгочной артерии по Мюллеру) и радикальную коррекцию порока – пластика дефекта межжелудочковой перегородки заплатой из листков перикарда в условиях искусственного кровообращения, кардиоплегии и гипотермии.
Нередко тромбоз легочной артерии приводит к разрушению новообразования или его части.
Объем появившихся тромбов может быть разным. От этого зависит степень проявления опаснейшей патологии — тромбоэмболии.
Группа риска
Это заболевание развивается в венах нижних конечностей и малого таза. В группу риска входят лица, страдающие:
- Нарушениями функционирования сердечных клапанов.
- Патологиями работы сердечной и сосудистой систем.
- Флетботромбозами.
- Тромбофелитами.
Также тромбоэмболия может развиться как осложнение во время послеоперационного периода.
Причины развития патологии
К основным провоцирующим факторам развития этого заболевания относятся:
- Генетическая предрасположенность.
- Нарушенная свертываемость крови.
- Долгий и мучительный постоперационный период, последовавший за сложным хирургическим вмешательством.
- Травмирование костей бедра и таза.
- Период вынашивания плода.
- Послеродовой период (ввиду изменения свертываемости крови, риск развития патологии повышается в 5 раз).
- Сердечные патологии.
- Злоупотребление никотином.
- Ожирение.
- Варикозная болезнь.
- Перенесенный в прошлом инсульт или инфаркт миокарда.
- Наличие опухоли злокачественного характера.
Симптоматика
Специалисты в области медицины подразделяют эту патологию на такие типы, как:
- массивная тромбоэмболия;
- субмассивная тромбоэмболия;
- немассивная тромбоэмболия.
Для массивной тромбоэмболии характерные такие симптомы, как острейшая недостаточность правого желудочка, сопровождаемая стремительным шоком и гипотонией. Наблюдаются следующие признаки:
- одышка;
- ярко выраженная тахикардия;
- утрата сознания.
Субмассивная тромбоэмболия проявляется нарушением функционирования правого сердечного желудочка. Ему сопутствует разрушение миокарда, свидетельствующее о развитии в легочной артерии гипертензии.
Симптомы немассивной тромбоэмболии выглядят следующим образом:
- кашель (надрывный), сопровождающийся кровохарканием;
- высокая температура тела;
- болезненные ощущения при дыхании.
Расширение легочной артерии
Аневризма легочной артерии по происхождению может быть приобретенной и врожденной. Приобретенная патология нередко образуется на фоне гипертензии (легочной вторичной).
Провоцирующие факторы
Аневризма легочной артерии развивается на фоне:
- Сифилиса.
- Туберкулеза.
- Атеросклероза.
- Периартериита узелкового.
Характерные симптомы
В течение длительного времени патология может никак не проявлять себя. В некоторых случаях наблюдаются симптомы, связанные с прогрессированием основного заболевания.
Протекание заболевания в большинстве случаев неблагоприятное. Многие пациенты умирают от развития осложнений.
Лечение заболевания заключается в своевременном хирургическом вмешательстве.
Медицинская помощь
Лечение больных проводится в условиях интенсивной терапии. В случае остановки сердца производится его реанимация. Для повышения уровня АД назначаются внутренние инъекции следующих препаратов:
- Допамина.
- Адреналина.
- Добутамина.
Купирование образования в крови тромбоцитов обеспечивается благодаря:
- Фондапаринуксу.
- Далтепарину натрия.
- Гепарину.
В некоторых случаях для нормализации в легочных артериях кровотока врач принимает решение удалить тромб.
Профилактические меры
К важным мерам профилактики относится предупреждение факторов риска этой опасной патологии. Немаловажно вовремя позаботиться относительно зондирования легочной артерии, которое позволяет измерить давление.
Норма давления в легочной артерии составляет не более двадцати шести миллиметров вод.ст. При нагрузках давление увеличивается до тридцати семи показателей.
Отличной профилактической мерой тромбоза и его последствий является ношение во время послеоперационного периода чулок (эластических) или бинтование нижних конечностей.
Симптомы сердечной недостаточности у женщин
Как проявляются и почему возникают симптомы сердечной недостаточности у женщин?
Как правило, серьезное заболевание сердца поражает людей старшего возраста, подвергающихся стрессам, злоупотребляющих алкоголем, курением, страдающих от атеросклероза, гипертонической болезни, сахарного диабета. Иногда перенесенное инфекционное заболевание, например, грипп, может способствовать развитию болезни сердца.
Женщины в период гормональной перестройки организма нередко страдают от сердечной слабости. Степень развития сосудистой патологии зависит от сопутствующих заболеваний и психического состояния человека. Химические реакции при стрессе ухудшают кровоснабжение сердца, ускоряют пульс, создают предпосылки для развития инфаркта миокарда или острой сердечной недостаточности.
В этом случае пациенту необходимо вовремя проводить лечение ослабленного сердца с целью предотвращения сердечного приступа.
Причины
Сердечная недостаточность проявляется в результате быстрого развития многих патологических процессов в сердечной мышце. Во многих случаях появляется кислородное голодание и нарушаются функции всех органов. Ослабление сердечной мышцы часто возникает при таких заболеваниях и вредных привычках, как:
- дистрофия миокарда;
- аритмия;
- гипертоническая болезнь;
- диабет;
- курение;
- алкоголизм.
В результате развития инфаркта миокарда наблюдается появление нарушений в работе левого желудочка сердца. Кровь застаивается в сосудах малого круга кровообращения, страдает питание мышцы сердца.
Нередко причиной развития недостаточности служит нарушение в работе правого и левого желудочков сердца. Артериальная гипертензия и избыточное поступление жидкости в организм также могут служить причиной появления сбоя в работе сердечной мышцы. На величину сердечного выброса влияют токсины, малокровие и повышенная функция щитовидной железы. Сердечная недостаточность у женщин развивается в результате стойкого повышения артериального давления и длительной аритмии.
Начальная фаза болезни
Признаки сердечной недостаточности появляются при поражении организма вирусами и бактериями, проникающими в миокард, и разрушающими структуру клеток. Плохая работа мышцы сердца приводит к развитию сердечной недостаточности. Увеличиваются размеры сердца, нарушается ритм, изменяется проводимость. Большие сосуды сжимаются отечной жидкостью, страдает кровоснабжение миокарда.
Многие больные испытывают слабость в течение суток, повышенную утомляемость, сердцебиение. Особенно тревожит женщину чувство тяжести в области сердца, субфебрильная температура. Прислушиваясь к своим ощущениям, пациентка отмечает тупую боль в левой половине грудной клетки, посинение кожи вокруг рта. Одновременно изменяется психическое состояние женщины. Появляется чувство постоянного беспокойства, неудовлетворенности, страха. Нередко больная обращает внимание на частое и шумное дыхание. Женщина страдает от симптомов интоксикации:
- слабость;
- головная боль;
- предобморочное состояние;
- повышенная потливость.
Физическое напряжение вызывает появление неприятных ощущений: аритмии, сердцебиения, одышки.
Симптомы левожелудочковой недостаточности
Симптомы левожелудочковой недостаточности проявляются как спазмы в груди слева, невозможность изменить положение тела, хрипы в легких, набухание шейных вен, кашель. Практика показывает: одышка возникает на ранних этапах болезни после физических нагрузок, а нередко - в состоянии покоя.
Острая недостаточность всегда опасна для жизни и здоровья женщины и проявляется такими симптомами, как:
- холодный пот;
- бледность кожи;
- аритмия;
Прогрессирующее нарушение функции сердечной мышцы приводит к изменению кровоснабжения, появлению высокого артериального давления, метаболическим нарушениям. У больной женщины наблюдают увеличение размеров печени, отеки ног и в области поясницы, набухание шейных вен.
У ВИЧ-инфицированных пациенток первые признаки недостаточности сопровождаются образованием инфильтратов в области проводящей системы сердца и появлением стойкой аритмии. Миокард при недостаточности страдает от нарушения обменных процессов.
Развитие осложнений
В молодом и зрелом возрасте существует разница между острой левожелудочковой недостаточностью у мужчин и женщин. Это объясняется защитным действием половых гормонов - эстрогенов. При левожелудочковой патологии у женщин появляется слабость сердечного клапана, анемия, кардиологические нарушения.
У девушки, страдающей патологией левого желудочка, часто развивается одышка, отек слизистой бронхов и легочной ткани. Физическая нагрузка ухудшает самочувствие больной. Женщина с трудом выдыхает воздух, появляется синюшность вокруг рта, увеличивается нагрузка на сердце и сосуды. Прогрессирование болезни приводит к появлению одышки и в состоянии покоя. Больная не может спать на низкой подушке, просыпается в ночное время от приступа удушья.
Застой крови и недостаточный тонус сосудов вызывают появление серьезных нарушений, значительно усугубляющих ситуацию. У больной возникает свистящее дыхание, небольшое покашливание или сильный кашель, повышается артериальное давление.
Опасное осложнение сердечной астмы - отек легких, требующий неотложной медицинской помощи.
Нарушение функции правого желудочка
Недостаточность, связанная с неполадками в работе сердечной мышцы, возникает при быстром переливании крови или ее заменителей. Одна из главных причин появления слабости правого желудочка - закрытие тромбом легочной артерии или развитие таких болезней, как астма, пневмоторакс, пневмония.
В случае появления сбоев в работе правого желудочка сердца женщина предъявляет жалобы на тахикардию, головную боль, синюшность кожи губ, уменьшение суточного количества мочи, появление отеков.
Следует помнить о том, что в результате уменьшения суточного диуреза в организме больной задерживается калий. Подобное состояние очень опасно для жизни женщины. Во время приступа сердечной астмы пациентка испытывает значительное облегчение, сидя на кровати или стуле. В этом случае улучшается отток крови от сосудов головного мозга, снижается кровенаполнение сердца, осуществляемое из нижней полой вены. Нередко больная ощущает тяжесть в животе из-за увеличенной в размерах печени, образовавшихся отеков на нижних конечностях и передней брюшной стенке.
В случае развития острой формы болезни пациентка предъявляет жалобы на сердцебиение, отеки в области нижней трети голени, боль в печени.
Первые признаки сердечной недостаточности правого желудочка сменяются более тяжелыми симптомами. Отеки охватывают поясницу, бедра, верхние конечности. Больную беспокоит тошнота, желтушность кожи и склер. Через несколько суток симптомы недостаточности усиливаются, холодеют конечности, появляется обильное мочеиспускание. Урина содержит значительное количество белка, а больная теряет аппетит, отказывается от приема лекарств.
Зная симптомы сердечной недостаточности, женщина может вовремя обратиться к врачу и сохранить здоровье на долгие годы.
Автореферат диссертации по медицине на тему Гиперволемия малого круга кровообращения и способы ее компенсации у больных ишемической болезнью сердца, гипертонической болезнью и пороками сердца
На пра>ах рукописи
^ ^ ЕВДОКИМОВА АННА ГРИГОРЬЕВНА
УДК 616.11-009.72; 615.835.12
ГИПЕРВОЛЕМИЯ МАЛОГО КРУГА КРОВООБРАЩЕНИЯ И СПОСОБЫ ЕЕ КОМПЕНСАЦИИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА, ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ И ПОРОКАМИ СЕРДЦА.
МОСКВА - 1995
Работа выполнена в Московском медицинском стоматологическом институте. Научный консультант:
Доктор медицинских наук, профессор А.Э. Радзевич Официальные оппоненты:
Доктор медицинских наук, профессор В.М. Панченко Доктор медицинских наук, профессор МА Гуревич Доктор медицинских наук, профессор А.Л. Сыркин Ведущее учреждение:
Российский университет дружбы народов
заседании специализированного Совета Д.084.08.01 в Московском медицинском стоматологическом институте (ул. Долгоруковская, 4).
С диссертацией можно ознакомиться в библиотеке института (ул. Вучетича, 10-а).
// ¿¿/<¿>¿-<4 1995 г.
Ученый секретарь специализированного Совета доктор медицинских наук, профессор
ЛЛ. Кириченко
АКТУАЛЬНОСТЬ ПРОБЛЕМЫ
Лечение отека легких у больных с сердечно-сосудистой патологией по-прежнему остается одной из актуальных задач современной кардиологии.
Исследованию состояния гемодинамики при развитии пшерволемии малого круга кровообращения у больных ншемической болезнью сердца, гипертонической золезнью и пороками сердца, лечению этих состояний посвящено много работ (Грацианский НА и соавт.,. 1979; Тополянский В.Д., 1982; Руда М.Я., 1982; Гасилш! B.C., 1987; Рябов ГА., 1988; Голиков А.П. и соавт., 1989; Радзевич А.Э., 1990; Сыр-<ин АЛ., 1991; WaUcenstein M.D. etal, 1985; Forrester J. etal, 1977).
При острой левожелудочковой недостаточности мероприятия направлены на эазгрузку малого круга кровообращения за счет улучшения насосной функции левого келудочка и уменьшения притока кропи к сердцу. Для этих целей наиболее часто трименяют сердечные гликозиды, периферические вазодилататоры, ганглиоблокато->ы, диуретические препараты (Панченко В.М. 1977, 1981; Голиков А.П. и соавт., 1978; Малая Л.Т. 1981; Чазов Е.И., 1982; Мгасайловнч D.A., 1990; Forrester J. etal, 1977). Однако не при всех типах гемодинамики можно применять вышеназванные руппы препаратов. Кроме того, действие их начинает проявляться только через 1015 минут, возможны различные осложнения: передозировка, чрезмерная гипотензия, клектролитные нарушения и т.д.
Известно, что темп развития альвеолярной стадии отека легких бывает порой ¡эстолько бурным, что часто не оставляет времени на реализацию терапевтических мероприятий. Нарастающая асфиксия белковой пеной быстро приводит к фатальной лпоксемии, а проведение искусственной вентиляции легких в режиме повышенного ¡апления в конце выдоха требует времени, специализированного аппаратного н ане- тезиологического обеспечения. Летальность составляет 30-50% (Рябов Г.А., 1988).
Это определяет актуальность создания модели пшерволемии малого круга ровообращения, когда представляется возможным изучение патофизиологических [еханизмов, возникающих в организме бального с сердечно-сосудистой патологией, данной ситуации, в частности, определить изменения со стороны гемодинамики, емостаза, микроциркуляции, функции внешнего дыхания, кислотно-щелочного со- тояния.
На основании выявленных нарушений разработать эффективный, быстродей- твующий и технологически доступный для практической кардиологической службы 1етод купирования отека легких и фатальной гипоксемин, позволяющим решить роблему дефицита времени, необходимого для проведения комплексной терапии
гиперволешш малого круга. В этом плане определенный интерес представляет использование метола дыхания под избыточным давлением (Мураховский К.И., 1979; Фомин И.О., 1985; Радзевич А.Э., 1990; Tompson L., 1987; Hunt N., 1987), с помощью которого уменьшатся явления централизации кровообращения.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Изучить состояние центральной и периферической гемодинамики, плазменного, тромбоцитарного и сосудистого гемостаза, микроциркуляции функции внешнего дыхания, кислотно-щелочного состояния при моделируемой гипервалемии малого круга кровообращения в условиях "сухой" иммерсии; разработать способ коррекции выявленных нарушений методом дыхания под избыточным давлением и оделить клиническую эффективность этого метода в комплексной терапии кардиоген- кого отека легких.
1. Изучить влияние "сухой" иммерсии, как модели гипервалемии малого круга кровообращения, на состояние центральной и периферической гемодинамики у здоровых лиц с пограничной артериальной гипергензией.
2. Определить состояние плазменного, тромбоцитарного и сосудистого гемостаза, микроциркуляции, кислотно-щелочного состояния и функции внешнего дыхания в условиях "сухой* иммерсии.
3. Сравнить результаты инвазивных и неинвазивных методов исследования при суховоздушном погружении в иммерсионную среду.
4. Изучить влияние дыхания под избыточным давлением, как способа коррекций гиперэолемии малого круга кровообращения, оценить его воздействие на центральную и периферическую гемодинамику, гемостаз, микроциркуляцию, КЩС, функцию внешнего дыхания.
5. Оценить клиническую эффективность применения метода дыхания под избыточным давлением в комплексной терапии отека легких у больных с сердечно-сосудистой патологией.
Исследования проводились с 1980 по 1995 год на базе 52 ГКБ (Главный врач Мишутин В.И.) совместно с Институтом медико-биологических проблем МЗ РФ и НИИ транспланталогии и искусственных органов МЗ РФ (в отделении рентгено- функциональной диагностики, зав. - д.м.н. Честухин В.В.).
Исследование явилось фрагментом плановой научной темы "Артериальная гипертензия, атеросклероз, ншемическая (коронарная) болезнь сердца", (№ гос.регистрации 01920017874).
НАУЧНАЯ НОВИЗНА
Впервые проведено комллекное исследова!ше центральной и периферической гемодинамики, изучено состояние плазменного, сосудистого и тромбоцотарного гемостаза, михпоциркуяяцни, функции внешнего дыхания, кислотно-щелрчного со-сгоетсий в условиях "сукой" кммерсии, как модели гаперволемии малого круга кровообращения. Доказано, что метод суховоздушного погружения в водноиммерсксн- ную среду позволяет моделировать гиперволемию малого круга кровообращения для изучения патогенетических механизмов, особенно в первые трое суток его применения.
Разработан способ адаптации в режиме "сухой" иммерсии (авт.свид № 1352690, ДСП).
Для коррекции выявленных нарушений в режиме "сухой" иммерсии был применен метод дыхания при избыточном даалении.
Впервые комплексно исследовано влияние дыхания под избыточным давлением на гемодинамику, гемостаз, микроциркуляцию, КЩС, функцию внешнего дыхания у больных с пограничной артериальной птертешией в возрасте 45-55 лет в условиях моделируемой гиперволемии малого круга кровообращения.
Покгзако, что выявленные патофизиологические сдвиги успешно компенсирует метод дыхания под избыточным давлением.
Разработан способ профилактики патологических реакций в "сухой" иммерсии (гвт.свид № 1531269) и способ профилактики циркулярных нарушений при снижении гравитации {авт.свид № 1724182).
Были отработаны оптимальные режимы дыхания под избыточным давлением + !0 см водного столба для применены у бальных сердечно-сосудистой патологией, осложнившейся отеком легких.
Доказано, что метод дыхания под избыточным, дгллением является высокоэффективном, 5ксгродействующим и технологически доступным для купирования кардиогг."гного отека легхих и фатальной гипоксемии и позволяет рев ть проблему дефицита зремени, необходимого хчя комплексного лечения острой сердечной не- достаточности.
ПРАКТИЧЕСКАЯ ЦЕННОСТЬ
Проведенные клшшко-экспсриментальные исследования показали, что метод "сухой" иммерсии позволяет моделировать состояние гиперволемии малого круга кровообращения дня изучения патогенетических механизмов и разработки эффективных способов их коррекции.
Гиперводемия малого крута кровооборащения в модельных исследованиях сопровождается гиперкоал -"яционным синдромом, ухудшением микроциркуляции, изменениями со стороны КЩС и ФВД.
Результаты проведенных исследований показали, что величина минутного объема сердца в условиях "сухой" иммерсии может определяться с помощью интегральной реографии с использованием коэффициента, согласующего показатели МОС, полученного методами интегральной реографии и термодилюции.
Доказано, что для коррекции нарушений, развивающихся в условиях моделируемой гиперволемии малого круга кровообращения, с высокой эффективностью может использоваться метод дыхания под избыточным давлением +10 см водного столба.
Применение дыхания под избыточным давлением +10 см водного столба в комплексной терапии отека легких у больных острым инфарктом миокарда, гипертонической болезнью, пороками сердца, позволяет купировать альвеолярную стадию отека легких за 10-20 минут без применения пеноггситслей.
Метод дыхания под избыточным давлением высокоэффективен для профилактики угрожающего кардиогенного отека легких.
Указанный метод можно применять в стационарах, в машине скорой помощи с использованием аппарата "НИМБ- 1", выпускаемого отечественной промышленностью, и аппарата "Выдох", разработанного на основе результатов настоящего исследования.
ВНЕДРЕНИЕ В ПРАКТИКУ
Разработаны и внедрены практические рекомедации по лечебной тактике интенсивной терапии отека легких у больных острым инфарктом миокарда, гипертонической болезнью, пороками сердца с применением метода дыхания под избыточным давлением. ■
На основании полученных данных оформлены заявки на 3 изобретения, на которые получены авторские свидетельства: "Способ оценки адаптации организма при моделировании состояния невесомости в условиях иммерсии" авт.свид.
6 1352690, 1988 г.; "Способ профилактики патологических реакций при сниженной равитации", авт.свид № 1531269, 1989 г.; "Способ профилактики циркуляторных ирушеиий при сниженной гравитации", авт.сви. N° 1724182, 1991 г.
Результаты исследования используются в научной работе и педагогическом [роцессе на кафедре терапии ФУВ ММСИ.
АПРОБАЦИЯ РАБОТЫ
Основные положения диссертации представлены на: Всесоюзной конференции Актуальны? проблемы космической биологии и медицины" (Москва, 1980 г.); XVIII ъеэде терапевтов (Ленинград, 1981 г.); научно-парктической конференщш ММСИ Здоровье человека и окружающая среда" (1983 г.); координационном совете ИМБП Москва, 1987 г.); XVIII Гагаринских чтегиях, 1988 г.; научно-практических конфе-«нциях ММСИ (1988, 1990, 1993 гг.).
Проведена школа-семинар по внедрению результатов исследования для врачей ". Москвы и Московской области (1988 г.) на тему "Нетрадиционные методы лече- шя".
ОБЪЕМ И СТРУКТУРА ДИССЕРТАЦИИ
Диссертация состоит из введения, 5 глав, заключения, выводов, практических >екомендаций и списка литературы, включающего 230 работ отечественных и 211 >абот иностранных ггторов. Объем составляет машинописного текста,
|ключает таблиц и_ рисунков.
ОБЩАЯ ХАРАКТЕРИСТИКА МАТЕРИАЛА И МЕТОДЫ ИССЛЕДОВАНИЯ
В первой клинико-экспериментальной части было обследовано 15 здоровых мужчин в возрасте от 32 до 41 года и 42 мужчин - больные пограничной аргериаль- юй гкпгртензней в возрасте от 35 до 54 лет. В зависимости от целей исследования ¡есь контингент обследуемых лиц был разбит на 4 группы.
В I группе были обследованы практически здоровые лица в возр; ; от 32 до И года (9 человек). Изучали сопоставимость результатов измерения минутного объела сердца в условиях "сухой" иммерсии методом термодняюции а интегрально?!
реография. МОС" измеряли до режима "сухой" иммерсии и со II по VI сутки иммерсии.
Во II группе обследовано 22 больных с пограничной артериальной гипертен- зией в возрасте от 45 до 53 лет. Изучали влияние иммерсик, как модели гиперво- лемин малого круга хровообракения, на показатели центральной и периферической гемодинамики; плазменный, сосудистый и тромбощгтарный гемостаз, микроцкрку-ляцгао, кислотно-щелочное состояние, функцию внесшего дыхашм. Контрольную группу составили 6 здоров: мужчин б возрасте от 30 до 40 лет.
В III группе обследовали 20 больны.: пограничной артериальной гилертензией в возрасте от 45 до 54 лет и 6 здоровых мужчин в возрасте с? 30 до 41 года.
В этой группе изучати влияние дыхания под избыточным дамением (ДИД + 10 см водного столба).
Исследования гемодинамики проводили до начала иммерсии, перед сеансом ДИД, на 15 и 30 минутах сеанса ДИД, сразу хе после сеанса и через" 30 и 60 минут после окончания сеанса ДИД.
Во нторсй части работы в клинических условиях исследовшия проведены у 4-х групп больных..
В I группа было обследозано 102 больных острым инфарктом миокарда; из них 52 больных составил! осиовную группу (в возрасте от 40 до 73 лет, из них мужчин - ЗЕ,"хе;пдин - 14).
Диагноз СИМ ставили на основании данных анамнеза, клинической карты, изменений ЗКГ к псБьшения активности спгцифнчзских фер»сектоз.
У 46 больных Сына. НКШ, б чгповзк составили бсльныз с НКГУ (по классификации "Ш1цр). Есгалгым это»: группы в комплексной терапии отека легких применялся метод ДИД.
Контрольную группу для оценки метода ДИД составили больныг (50 человек) с острым инфарктом миокарда, осложненным отеком легких, леченных периферическими вазодклататоргми и мочегонным»; средствами.
Беем больным ОИМ до начата исследования проводили общепринятую терапию: наркотические и неиаркотические анальгетики, вазедиягтаторы, мочегонные средства, капельно глкжозо-калий-инсулинозую поляризующую смесь е гепарином в дозах до 200-300 ед/кг/сутки. По показаниям применяли аитиархтмнчеезеие препараты (лидокаин, тримека1ш), интраназалько кислород. При ОСНГУст дополнительно применяли катгхаламины, глюкокоршкоиды (или сердечные гликозвды п крайних случаях).
II группу составили больные с митральным стенозом, 28 человек в возрасте от 22 до 63 лет (8 мужчин и 29 кенщин).
Всем больным с момента выявления отека легких проводилась терапия, включающая нейролептики, в части случаез, наркотические анальгетики, периферические ваяадклататсры, лазикс, оксигеиотерапию, по показаниям, сердечные гликозиды и положительно инстропны® средства при низком АД.
У 19 больных митральным стенозом на фоне общепринятой терапии применяли метод ДИД. ,
В III группе обследозгли 41 больного с аортальным стенозом в возрасте от 25 до 59 лет (15 мужчин и 26 женщин), из них у 19 больных на фоне развившегося отека легких проводилась комплексная терапия с применением ДИД.
В IV группе были обследованы 22 больных с гипертонической болезнью в возрасте от 44 до 69 лег (женщин - 12, мужчин - 8), у которых на фоке гипертонического криза развивался отек легких.
Всем больным с ОЛН проводилась гипотензивная терапия пшглноблокато- рами, кейрслгптихЕми, диуретикгми, зазедклгтаторами; кислород интргназально.
У 12 больных в комплексную терапию гипертонического криза и отека легких был акяючен метод ДИД.
ИСПОЛЬЗУЕМЫЕ СРЕДСТВА: моделирование гипервалешш малого круга кровообращения осуществляли методом "сухой" иммерсии, т.е. погружением в воду, однако, контакт кожи с водой был полностыэ исключен с помощью мягкой водоне- пре;гацаемой ткани. Это позволяло проводить любые клинические исследования в полном объеме (Е.Б. Шуяьженхо, ¡975).
Определение минутного объема сердца методом термодшиощш осуществляли с помощью катетера Swan-Ganz s термистсром и баллончиком (Edwards Lab. модель 93А-131-7F). Его располагали таким оврагом, чтобы гл стальное отверстие (и тер- мдгтор) находились в стволе легочной артерии, а проксимальное - в области правого .л. Гасчет производили на специальном компьютере Edwards Lab (США) с регистрацией на микгогргфг-32 (Siemens, Швеция).
В коронгркый синус имплантировали специальный катетер с термисторами (W. W. Lab., Calif, модель CCS-7F-90A).
Постоянную скорость введения термоиндихатора обеспечивала омпа "Sfge ínst., Orion Res.Mzs (модель 351), объемную скорость кровотока измеряли фдоумст-ром LF-300 (W.W.Lab).и регистрировали на самописце Omnisíriblí (Hcmtcn Jnä.).
Показатели работы левого желудочка.определяли при зондировании лучевой ида бедренной артерии, использсзгли катетеры Odkaa-Gans фирмы Eickatg (США) №7324067 или №73-2067 диаметром 7Г, длиной 110 см.
Кривые даале:-и1Я регистрировали алектромгномеграми "Statgam-P23Db" (США) и "Sinucens-746" (ФРГ), учитывая Апд... САД, средне® давление в правом предсердии (ГШ), систолическое, средне® и кокгчно-диастслическое давление в правом желудочке (КДДПЖ), легочной артерии (JIA) и дарение заклиштая в легочной артерии (ДЗЛА).
При катетеризации левого желудочка (ЛЖ) определяли конечно-диастоли- чесхое давление ЛЖ (КДДЯЖ) и показатели его сократимости cp/dtm - максимальная скорость нарастания вкугрижглудочхового давления, характеризующее максимальную скорость расслабления желудочка.
Рассчитывали СИ = ---л/мнн/м1
ОШ1С -------* 80 дин * с * см""
СИ (САД - КДЦЛА) ИУРЛЖ «-------------»13.6 г * м * м*
Общее легочное сопротивление (ОЛС) по формуле: СДИА-ПП
-----* 80 дин * с * см"1
ПД (перфузионное даакгние) по формуле: ЦД = САД - ДКС^,
где ßKC^ - средне® давление в коронарном синусе (мы рт.ст.).
Ресграфичгсксз исследование проводили по методах® (М.Тищенко, 1973) с регис^рашей интегральной реогргфии, реоэнцефалогргфик, ргопулъмакографии верхней в ккжней доли, реогепатографии, реозазогргфии предплечий и голеней. Реограммы, регистрировали с помощью реографа ЧРГ- 1 и регистратора "tvi интеграф.-34" (Швеция).
Эхохардиографическое исследование проводилось на аппарате "Echoview" фирмы "Picket" (США) с компьютерным расчетом основных показателей в одномерном. режиме по общепринятой методике.
Параметры кислотно-щелочного состояния (КЩС) определяли на анализаторе "Кориинг-168" (Англия) и AVL-940, содержание гемоглобина регистрировали прибором "Hemolux" AM-101 по гемоглобинцианидному методу.
Функцию внешнего дыхания (ФВД) изучали на аппарате Метатест-2.
Исследогише микрососудистого русла бульварной конъгокгави проводилось при помощи фэтощеяевой лампм фтни "On:, п" (ФРГ) по методике B.C. Волкова (1975), модификации В.В. Смирном (1978).
Адгезия и распластывание тромбоцитов изучались по методике ЕЛО. Васильевой, фахго? Виллебранда определяли михрэлп-рациошпаг,: методом по И.Ееспглъко. Агрегация тромбощгтоз изучалась по методу С.Зот и O"Brien на агрегометрах фирмы "Siesco" (США) и "ЕМ-840" (Италия) с реактивами фирмы "Serva".
Тромбсксан и простацивпш определяли радкокммунслогическнм методом с помощью коммерческих наборов фирмы "Seragen" (США).
Показатели плазменного звена гемостаза исследовались с помощью тромбо- эластсграфии на аппарате ГКГМ-4-02 (СССР). Фибриноген определяли по методике МЛ. Рутберг.
Непрерывное злетрокардисграфическое исследование в течение суток прсво- драюсь о использованием системы Medi"og MA-14 (Oxford Medical Systems, Англия).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
I. Хлктям-эксаеримеэталикг исслсдоветю.
Í. "сухой" Ег;.-г.!0рсии ¡;я показателя ЦГД у здоровых лац.
Погружение d иммгрсиогтую среду вызывает заметные изменения ряда параметров. Так, через 20 минут после погружения в ИМ ЦВД увеличивается на 1,2 ми рт.ст. (44%) (р<0,05), среднее ДЛА на 4-6 мм рт.ст. (39%) (р<0,01), работа правого желудочка сердца на 67% (о<0,01), СИ повышается на 0,5 л/мкн/м1 (14%) главным образом за счет увеличения ударного индекса на б мл/и" (11%). Сбъем крови в правых отделах сердца повышался от /99±18 до 371±16 мин (р<0,05). Тенденция к увеличению параметров ЦГД сохранилась до 6 часов режима КМ. В дальнейшем стала отмечаться тенденция к снижению СИ на 2-3 сутхи воздействия, снижение ДЯА, к 3-м суткам - ЦВД, к 6-7 суткам - АДС.
Таким образом, шалш показателей центральной гемодинамики указывает на развитие гипероадемни малого круга кровообращения, особенно d первые 3 суток режима ИМ, при этом формируются компенсаторные реакции, быстро включаются механизмы защиты (рефлекс Герип^Гаузра), не приводя к.перегрузке, особенно правых отделов сердца, за счет появления массивного диуреза и уменьшения О ЦК.
На этой же труппе больных кгм» были исследованы два метода определения МОС: термодилюцкей и интегральной ргографией, так хах было устгкоьгжно, что а условиях "сухой" иммерсии у человека увеличивается пстоотделе "ие, что влечет за
собой уменьшение постоянной омической составляющей реограммы, в среднем на 20%. Таким образом, абсолютные значения МОС, измеренные г иммерсии методом, интегральной ргографии, заиижега».
" Многократное синхронное измерение минутного объема сердца, как до ИМ, так и во время ИМ, показало, что в обычных условиях, в горизонтальном положении, средние величины МОС достоверно юе различаются: 7,б0±0,4 л/ммн (интегральная реография) и 7,53±0,28 л/мин (термодшпоция). В ИМ величины МОС, измеренные методом интггралья. реографии ниже в среднем на 1,73 л/мин. (табл.1).
Таблица 1.
Усрадпенаая давамша МОС-ТД и МОС-ИР.
Режим иммерсии МОС-ТД МОС-ИР Р
фон 7,53±0,29 п=14 7,60±0,35 11=11 . 0,39
II сутки б,01±0,25 п=9 4,03±0,21 п=11 <0,01
III сутки 6,64±0,26 5,72±0,27 <0,05
IV сутки 5,57±0,27 а=9" 4,28±0,23 п=9 <0,01
V сутки 6,80±0,20 . " п=18 5»24±С,16 п-16 <0,01
VI сутки 6,47±0,21 а=8 4,97±0,23 п=8 <0,01
Таким образом, в дальнейших исследованиях эта разница учитывалась при анализе средних показателей ЦГД, определяемых а условиях иммерсии.
2. Вляяаае "сухой" шмереш вд воказатмш гемодншамкки у лиц с ПАГ.
Изучение влияния ИМ на сердечно-сосудистую систему у больных с ПАГ показало, что, как и у здоровых лйц, имеют место ярко выраженные индивидуальные реакции различных показателей центральной и периферической гемодинамики.
Основные тенденции изменений МО, УО и \У (мощности левого желудочка) проявлялись в снижении их величин, начиная с гонца 1 суток иммерсии. У большинства исследуемых отмечалось стойкое снижение АД во время иммерсии (табл.2).
Таблица 2.
Динамика МОС (л/мая), САД (мм рт.ст.), А (кгм/мнп) ■ условиях аммерсин у лиц с ПАТ.
Реадаптация
Иммерсия (сутки) (сутки)
Показатели Фон I III V VII I III
М 6,79 4,92 5,67 . 5,39 15,51 6,73
МОС ±т 0,50 0,70 0,65 0,39 0,30 0,55
п 34 42 55 39 41 32
Р <0,05 >0,05. <0,05 <0,05 >0,05 >0,05
М 94,94 88,13 90,74 88,66 88,26 93,38 92,08
САД ±т 0,86 0,78 0,25 0,93 0,75 0,80 0,91
п 48 47 43 45 45 42 43
Р <0,01 <0,01 <0,01 <0,01 >0,05 >0,05
М 8,43 5,61 6,83 6,31 6,38 8,33 7,88
А ±т 0,71 0,88 0,81 0,43 0,41 0,82 0,61
п 16 16 16 15 15 15 15
Р <0,05 >0,05 <0,05 <0,05 >0,05 >0,05
Средние величины ЧСС в целом по группе были достаточно стабильны и колебания носили недостоверный характер.
Анализ пульсозого кровонаполне!шя головы, легких, предплечий, голеней и печени показал, что в условиях ИМ происходит выраженный процесс перераспределения крови, известный как "эффект централизации кровообращения" (Е.Б. Шуль-хенко, 1975, С.М. Беляев, 1982, О.Саиег, 1973). При этом отмечается увеличение сосудистых зон головы, легких и плечевого пояса с одновременным уменьшением этого параметра в нижних конечностях.
Так пульсовое кровенаполнение головы к 3 суткам ИМ увеличивает..я на 17% 1р<0,01), среднеиммерсионный уровень этого же параметра в легких составил 132- 166% (р<0,05), в сосудистой зоне голени - 61% (р<0,01) от исходного уровня, кровоток в печени уменьшатся на 36-43% (р<0,05) (табл.3).
Таблица 3.
Отяоснтельаыг изменения скорости нарастапия анакроты (V), диастоличсского индекса (ДИ) пульсового крововаполиешш (ПК) в легких н конечностях (в %%) (фоа - 100%) у лиц с ПАГ.
Иммерсия Реадаптация
Показатели I сутки III сутки V сутки VII сутки 1 сутки III сутки
Верхняя ПК 104,1 156,6 158,8 157,9 163,3 161,1
доля V 122,1 124,5 110,8 115,2 152,1 155,3
легкого ДИ 67,0 52,9 54,3 57,1 62,8 72,4
Нижняя ПК 186,8 152,2 135,8 123,9 125,4 109,8
доля V 144,5 132,5 135,8 122,1 130,7 121,6
легкого ДИ 75,0 75,1 70,4 78,2 Ь9$ 68,7
Пред- ПК 141,2 132,4 114,7 102,9 85,3 91,2
плечья V 117,2 " 98,5 82,2 84,6 78,8 70,1
ДИ 80,5 74,5 78,2 93,1 111,7 90,3
Голени ПК 66,0 67,0 62,3 58,5 74,5 88,7
V 96,2 99,8 89,4 94,5 78,2 89,4
ди- 75,1 81,4 78,3 81,5 91,8 95,7
Полученные данные свидетельствуют о том, что в услозши ИМ четко формируется гиперволемия малого круга кровообращения, наиболее выраженная в первые 3 суток суховоздушного погружения как у здоровых лиц, так и у больных с пограничной артериальной гипертензией.
По данным эхокардиографических исследований по мере увеличения пребывания в условиях иммерсии (через 24-48 часов) у большинства лиц происходит увеличение КДО, КСО, УО, МО (р>0,05), однако эти изменения по средним данным статистически недостоверны. Следует отметить выраженный индивидуальный характер эхокардиографических показателей. Что касается фракции выброса, то она практически не меняется за все время исследования.
3. Состояние гемостаза, микро циркуляции, КЩС, ФВД в условиях иммерсии.
Наиболее характерные изменения при моделировании гиперводемии малого круга кровообращения отмечались в гемостазе. Как у здоровых, так и у лиц с ПАГ, в »слопиях ИМ к 3 суткам максимально возрастал гемогокрит на 15% (у здоровых) и
25% (улиц о ГТЛГ). Адгезивная способность тромбоцитов регулируется содержанием в плазме фактора Виллебранда (ОВ). Оказалос что, как у здоровых, так и у болыи.>* с ПАТ, имеется выраженная корреляция между этими показателями. Ислн неходко его уровень приближался к верхней граница нормы или был выше ее (возрастная норма в 45-55 лет составляет 147,9±9,1%), то в процессе проведения исследования к 3-им суткам ИМ ДВ возрастал до 245-360%.
Кроме того, отмечалось увеличение числа тромбоцитов на 8-12%, увеличивалась степень и время агрегации и дезагрегации тромбоцитов, отмечалось угнетение фябршгодизз, снижение почти вдвое уровня 6-кето Пг F„ при практически неизменном уровне ТЖВГ
В период реадаптации у здоровых лиц все показатели гемостаза возвращаются к исходным значениям через двое суток, в отличие от лиц с ПАГ, у которых восстановление происходит к 5 суткам после окончания режима ИМ.
Таким образом, в режиме ИМ имеет место выраженный гилеркоагуляциошшй синдром с угрозой тромбообразозания.
В условиях ИМ ухудшается микроциркуляция. По данным конъюктивальной биомнкросхопин нарастает внутрисосудистая агрегация эр!ггроцитов (феномен Книзели) с замедлением сосудистого кровотока, нарушением проницаемости сосудистой стенки в виде появления периваскулярных геморрагий.
Со стороны КЩС отмечается развитие дыхательного ацидоза, увеличение Рсо, и снижение Рог
По данным исследования ФВД установлено, что в ИМ возникают функциональные нарушения вентиляции легких, которые имеют рестриктивный характер и проявляются снижение ДО, ЖЕЛ на 20-25% (у здоровых) и на 30-33% (у лнц с ПАГ), увеличивалась частота дыхания (с 14±1,1 до 18±1,2). Изменения были достоверными (р<0,01).
Таким образом, в результате проведенных исследований установлено, что ИМ вызывает гкперволемию малого круга кровообращения с целым рядом неблагоприятных синдромов, выраженность которых зависит от наличия патологии в сердечнососудистой системе, в частности ПАГ. Эти нарушения отмечаются в изменении гемодинамики, ухудшении плазменного, сосудистого и тромбоцитарного >е«остаза, микроциркуляции, ФВД, КЩС и наиболее выражены в первые трое cyi . иммерсии.
4. Применение дых*нмя сад избыточным доглеиием ш ыммеренш.
В качестве средства, коррешрующего выявленные ютофизиалотчесь"ие механизмы, нами предтожен метод дыхании под избыточным даяленигч (ДИД/ в первые
трое суток ИМ. Предварительно (по программе ИМБП) било установлено, что оптимальным режимом давления для компенсации гиперволемии малого круга кровообращения является +10 см водного столба.
Анализ результатов исследований показал, что сеансы ДИД в условиях ИМ приводят к умеренному снижению МО, УО, повышению АД, практически не оказывая влияния на величину мощности левого желудочка сердца (р>0,05), отмечалось увеличение ОПСС на 20%.
Состояние централы, л гемодинамики по данным эхокардиографии под воздействием ДИД существенно не мбнялось, т.е. сеансы дыхания под избыточным давлением как бы "смягчают" воздействие ИМ, стабилизируя функциональное состояние сердечно-сосудистой системы.
Наиболее выраженные изменения были в периферической гемодинамике: во время сеанса ДИД происходило уменьшение кровенаполнения сосудистых зон головы, легких и верхних конечностей; наряду с этим в значительной мере"увеличивалось кровенаполнение сосудов органов брюшной полости, в частности печени, и возрастал кровоток голеней (табл.4).
Такой характер перераспределения кровл свидетельствует о том, что ДИД способствует децентрализации кровотока, компенсируя гиперволемию малого круга кровообращения, создавая естественное депо в печени.
Отмечено, что сеансы ДИД-приводят к восстановлению парциального напряжения кислорода крови, сниженного во время иммерсии (компенсация дыхательного ацидоза), и способствуют увеличению насыщения кислородом тканей организма.
Кроме того, установлено, что сеансы ДИД оказывают гипокоагуляционный эффект как на показатели тромбоцитарного, так и плазменного и сосудистого гемостаза. При этом понижается агрегирующая активность тромбоцитов. На 3 сутки ИМ с применением сеансов ДИД агрегация тромбоцитов остается неизменной (до иммерсии - 44,4±4,45 отн%, на 3 сутки ИМ - 44,9±4,78 отн% при индукции АОФ -5М), 1, также не меняется. Аналогичным образом ведет себя агрегация тромбоцитов, индуцированная Адр и ристомицином, нормализуются показатели 6-кето Пг И, и Т,ВГ
Сеансы ДИД существенного влияния на распластывание тромбоцитов не оказывали, отмечается тенденция к снижению адгезии тромбоцитов и ФВ.
На плазменное звено гемостаза сеансы ДИД влияли положительно, понижая свертывающую активность крови (по данным тромбоэластографии не менялся индекс "И", удлинялись индексы "I", "в", "Т", увеличивался индекс "ФАК").
Таблица 4.
Дпламиха ПК (мл) головы, лспшх, печени, конечностей под влиянием сеансов ДИД.
Показатели Исходное Иммерсия ДИД После ДИД
состояние
сразу через 60 мин
ПК М 0,112 +0,057 -0,048 +0,027 +0,017
головы ±т 0,001 0,020 0,011 0,011 0,013
п 27 36 72 33 68
Р <0,01 <0,01 <0,05 >0,05
ПК М 2,7 +0,6 -1,3 + 1,9 -0,7 .
верхней ±т 0,3 0,3 0,6 0,7 0,6
дали п 30 36 70 32 69
легких Р <0,05 <0,05 <0,05 >0,05
ПК М 4,5 +3,1 -з,з +2,7 +1,2
нижней ±т 0,4 0,7 0,9 0,9 0,5
доли п 31 36 71 35 48
легких Р <0,01 <0,05 <0,01 <0,05
ПК М 1.9 -0,9 +1,9 -1,0 -о,з
печени ±т 0,1 0,3 0,4 0,4 0,2
п 25 33 58 23 38
Р <0,01 <0,01 <0,05 >0,05
ПК М 0,3 +0,15 -0,13 +0,14 ■+0,10
пред- ±т 0,1 0,04 0,03 0,05 0,09
плечий п 26 26 56 27 33
Р <0,01 <0,01 <0,01 >0,05
ПК М 0,6 -0,14 +0,07 -0,05 +0,02
голеней ±т 0,1 0,05 ■ 0,03 0,04 0,02
п 23 32 51 19 68
Р <0,01 <0,05 >0,05 >0,05
Примечание: знак "+" - увеличение по сравнению с исходным состоянием, знак " - уменьшение показателя.
Положительное влияние сеансов ДИД на гемостаз можно объяснить улучше- нием показателей гемодинамики: нормализуется кровоток в малом хруге кровообращения, улу.шастся печеночный кровоток, нормализуется диурез, следовательно уменьшается чравматизация клеток (эритроцитов, тромбоцитов), увеличивается поступление в кровь антикоагулянтов из печени и, в конечном итоге, нормализуются показатели гемостаза.
Таким образом, сеансы ДИД у здоровых лиц и у больных с ПАТ вызывали однонаправленные изменения, а именно устраняли признаки птеркоагуляции: увеличивали активность противосвертывающей системы крови и понижали активность свертывающей системы, устраняя опасность тромбообразованкя.
По данным конъюктивальной биоиикроскопии, проведение сеансов ДИД препятствует ухудшению микроциркуляции.
■ Применение ДИД при моделировании птервшемни малого круга кровообращения приводит к нивелировке изменений ФВД, возникающих под воздействием, приближая показатели к фоновым данным. Отмечено, что сеансы ДИД приводят к восстановлению парциального напряжения кислорода крови, сниженного во время иммерсии (компенсация дыхательного ацидоза), и способствуют увеличению насыщения кислородом тканей организма.
Таким образом, в клинико-экспериментальных исследованиях определяется четкая реакция организма человека, как здорового, так и с поражением сердечнососудистой системы в виде ПАГ, которая выражается особенно отчетливо в первые 3 суток адаптации к суховоздушному погружению гиперволемией малого круга крово- обращения, шперкоагуляцнонным синдромом, развитием компенсированного дыхательного ацидоза, оказывает неблагоприятное слияние на микроциркуляцию, ФВД.
Примените ДИД способствует коррекции патофизиологических сдвигов, возникающих в ИМ, в частности отчетливо происходит разхрузка малого круга кровообращения, устраняются признаки гаперкоагуляции, не ухудшается состояние мнкрососудистого русла и ФВД, устраняются изменения в К.1ЦС.
Никаких побочных реакций от применения ДИД в режиме +10 см водного столба не отмечено ни и о,;"ом случае.
Действие ДИД физиологично, так как во время сеанса "лишняя" кровь, "отжатая" из малого круга кромюбращения, аккумулируется в естественном депо хроаи - в печеии.
II. Исследования в клинических условиях.
Вышеперечисленное дало основание применить метод ДИД в клинических условиях в комплексной терапии отека легких у бальных с сердечно-сосудистыми заболеваниями.
В кардиологической практике формируют опасные ситуации в плане развития сотка легких следующие нозологические формы: острый инфаркт миокарда, выраженные митральный и аортальный стенозы, гипертонические кризы. Поэтому были исследованы больные с названной патологией.
В лечебной и контрольной группах с момента выявления у бального угрозы отека легких проводилось комплексное лечение, включающее нейролептики, в части случаев наркотические анальгетики, периферические вазодилататоры, быстродействующие диуретические препараты, охсигенотерапию, по показаниям - антиаритмическую терапию, в отдельных случаях, сердечные гликозиды, и положительные инотротше средства при низких АД.
Единственным различием было то, что в контрольной группе (без ДИД) внутривенно и ингаляционно применяли пеногасители, а в исследуемой группе - нет.
Метод ДИД реализуется с помощью серийно выпускаемого аппарата "НИМБ-
1. Клиническая эффективность метода дыхания под избьпгочпым давлением при лечении отека легких у больных острым ипфарктои миокарда.
Из 52 бальных ОИМ, которым применялся метод ДИД, было 46 больных с ОСНШ и 6 больных с кардиогенным шоком и отеком легких.
Динамика показателей ЦГД у больных ОИМ при применении ДИД в комплексной терапии отека легких представлена в таблице 5.
Полученные результаты исследований указывают на то, что в I группе с применением ДИД происходит более быстрая нормализация показателей: уменьшается среднее давление в правом предсердии, снижается СДЛА и ДДЛА, уменьшается КДЦЛЖ.
У больных контрольной группы на фоне традиционной терапии показатели работы правого желудочка нормализуются к 60 минутам, а КДДЛЖ сохраняется повышенным и через 1 час от начала лечения.
Таблица 5.
Двяамика показателей ДГД у больных ОИМ при лечении отека легких традиционной терапией (II группа, а-10) и при примеиешш ДИД (I грушш, п-15).
Показатели Группа Исходно 5 шш 30 мин 60 мин Р,
АДс мм рт.ст. I II . Р.М 134±2 128±7,5 132±4,1 128±б,9 115±3,2 105±3,1 <0,05 113±4,7 106±6,2 <0,05 <0,05 <0,05 <0,05
СДЛА мм рт.ст. I II *» 41,1±1,8 38±3,3 40±2,1 38±3,4 20±2,9 31±4,1 18±3,1 24±29 <0,05 <0,01 <0,05 <0,01
ДДЛА мм {)т.ст. I ■ II 29±3 31±2,2 28±2,1 31±2,7 16±3,7 24±3,17 <0,001 14±3,1 18±2,9 <0,01 <0,001 <0,01 <0,001 <0,01
ЧСС уд/мин. I II Р.;, 102±3,2 103±2,78 98±3,18 107±3,9 88±2,7 101±2,1 84±2,1 95±4,1 <0,05 <0,05 <0,05
СИ л/мин/м1 I II P«. 2,77±0,18 3,02±0,1 2,85±0,17 3,02±0,12 2,79±0,11 3,21±0,23 2,8±0,19 3,12±0,11
fan срдаип. мм рт.ст. I II б,85±1,1 7,12±1,4 6,97±1,2 7,13±1,3 5,2±1,1 6,3±1,5 4,1±0,28 4,9±1,02 <0,05 <0,05 <0,05 <0,05
КДДЛЖ мм рт.ст. I II 19,32±1,7 18,28±1,б7 19,08±1,3 18,33±1,5 17,01±0,9 20,2±0,8 П,9±1,2 16,4± 1,22 <0,01 <0,01 <0,01 <0,01 <0,05
Длительность периода изгнания с I II 0,2010,01 0,19±0,01 0,20±0,01 0,19*0,01 0,19±0,02 0,21±0,03 0,22±0,03 0,20±0,01 <0,01 <0,01 <0,05
dp/dt. ЛЖ мм рт.ст. I II р„ 1034±55 1097±64 1037±39 1097±64 1057±41 1071±52 1062±39 1079±44 <0,05 <0,05 <0,05
dp/dtyP. сек"1 1 II Р и, 22,02±1,3 24,GI±1,7 22,02±1,3 24,01±1,7 23,011:0,9 23,09±0,7 23,17±0,8 23,38±1,2 <0,05
0I1CC днн/с/см"" I II 1968±143 1864±172 2001±129 1864±168 1774±131 1800±141 1628±123 1730±112 <0,05 <0,05 <0,05 <0,05
Динамика основных кгапсичесхих проявлений у больных ОИМ и отеком легких была следующей. В группе больных, которым проводилось комплексное лечение отека легких с применением ДИД, быстрее уменьшалась одышка, так у 40 (87%) больных уже через 10 минут нормализовалась частота дыхания. На этот же момент в контрольной группе одышка уменьшилась к 25 минутам только у 19,4%. Среднее время скорости купирования одышки в I группе составило 8±0,3 мин., во II -34,3±0,5 мин. Различия достоверны (р<0,01).
Среднее время от начала лечения до выраженного уменьшения цианоза составило соответственно 13,3±0,8 м:ш. (I гр.) и 36,8±1,0 мин. (II тр.) (р<0,01).
Для группы с применением ДИД время, в течете которого купировался цианоз, составляло от 5 до 30 минут, а в группе без ДИД - от 20 до 60 минут.
Важным клиническим признаком разрешения альвеолярного отека легких является исчезновение влажных крипов.
При использовании з комплексной терапии ДИД исчезали влажные хрипы в верхних отделах легких уже в среднем через 11,9±0б8 мен., в нижних отделах в среднем через!б,0±0,8 икнут у 75% больных. У больных контрольной группы среднее время составило соответственно: 31,3±0,9 мин. и 38,4±0,3 мин., причем у 4 больных еще сохранились хрипы после 60 минут наблюдения, и они не включались в расчет. Различия высокодостозерны.
Факт появления диуреза является важным показателем в разрешении отека легких. Так, в группе больных с применением ДИД среднее время начала диуреза ссстгзияо 24,5±0,8 мин., в контрольной группе 37±0,8 мин. Различия высокодостоверны.
У 6 бсльныя ОИМ, осложненным НК1У применение ДИД дало временный положительный эффект. Тяжелая недостаточность кровообращения продолжала прогрессировать, а итоге все бальные погибли.
Таким образом, предложенный метод лечения альвеолярного отека легких у бслышк ОИМ, осложненным НКШ, приводи в течение первых 5-10 минут его применения во всех случает к быстрому и эффективному купированию альвеолярной стадии стека легких и улучшению клинического состояния больных.
2. Клиническая "эффеягнгаэет* метода дыхания под нзбыто-шым давлением у больных с мнтралыным <пгезозэм в отеком легких.
Было обследовано 28 бальных митральным стенозом с альвеолярным отеком легких, 10 из которых з комплексную терапию включали сеансы ДИД, 10 больных составили контрольную группу.
На фон® сеансов ДИД у больных основной группы отмечалась выраженная ". динамика показателей работы правого желудочка: уменьшалось ЦВД, скисалось давление в легочной артерии, так СДЛА уменьшалось с 6С±8,4б мм рт.ст. до 4ß±4,S мм рт.ст., ДЦЛА - с 32±5,3 мм рт.ст. до 18±3,1 мы рт.ст., ДЛАср - с 45,3±7,47 мм рт.ст до 29±3,7 мм рт.ст. Характер изменений достоверный.
Значительно уменьшалось давление в левом предсердии: с 27,8±2,93 мм рт.ст. до 17,5±2,9 мм рт.ст. Остальные изиекеши; показателей ЦГД нссклп недостоверный характер.
При анализе клинических проявлений отмечалось их быстрое разрешение у больных, которым в комплексную терапию отека легких включали ДИД.
Tai:, среднее spejm от начала лечения до выраженного уменьшения цианоза составляло еоответстЕешю 14,3±0,б ми:. (I группа) к 39,2±0,9 минут (II группа) " (р<0,01).
В результате применения ДИД одышка уменьшилась к 20 минуте. В контрольной группе к 40 минуте одышка уменьшилась у 75% больных.
Исчезновение влахшых хрипов в основной группе отмечено в среднем через 15±0,4 мин. - в верхних отделах, и через 18,0±0,4 мин. - в нюкнкх отделах, что было существенно меньше, чем в группе с общепринятой терапией (35±1,0 мни. и 43±4,3 , мин. соответственно). Изменения носили достоверный характер. У 4 больных в контрольной группе сохранялись влажные хрипы после 60 минут.
При анализе УД, как проявлении острой дыхательной кедостаточности, установлено, что ДИД способствует снижению этого показателя уже через 5 минут (с 34±0,6 до 24,2±0,7) (р<0,001). К 10 мкнугс УД уменьшалась до уроаня 20±0,3 в ми-нугу. В контрольной группе еще через 40 минут сохранялось учащенное дыхание и составляло 23±2,2 в минуту.
Среднее время пояаления диуреза в исследуемой группе составило 25,2±0,8 Mim. и 43±0,6 мин. в контрольной группе.
Таким образом, применение ДИД в комплексной терапии отека легких у больных с митральным стенозом способствует более быстрому разрешению гипер- волемни малого круга кроиообращения и купирует клинические проявления за 10-20 минут.
Таблица 6.
Двпяинза псказатгхей ЦГД у 5еяьшх аортальгъм стелозом и отеком легких при прямегети традиционной терапии и ДИД (п=19).
Показатели Исходные значения После лечения Р
ЧСС, уд/шш 100±2,8 82±4,3 <0,05
МОС, л/мин 3",4±0,28 «2*4,2
АД ср, мм рт.ст. 93,1±3,21 88±3,7 <0,05
с. 115,2±3,4 108±4.2 <0,05
Д. 75,6±2,1 76±2,38
СДЛЖ, мм рт.ст. 250±12,2 180±9,21 <ао!
КДДЛЖ, мм рт.ст. 2б,1±2,1б 21±3,23 <сц«и
029,3±39,1 1059±21,17
(1р/£Й/Р0 13,29±0,76 20±2,1
И-ОАК. 0,091±0,007 0.084±0,С&2
1,-ОАК 0,0525±0,001 0,0513±0,Ш
ДЗМК-ОАК (ФИС) 0,5861±0,00-. 0,568010,601
ОАК-ЗАК (ФИ) 0,3314±0,02 0,3011±0,0117
ОАК-И, 0,2911±0,07 0,2688±(Н0И
ФИР 0,0721±0,004 0,06624^0^0113*
УО 64,2±3,3 $),1±4,1
ФИ 49,72±3,89 55,19±3,1
Длк ер, мм рт.ст. 24.27il.71 " 17,1±2,12 <0,01
ДНА с, мм рт.ст. ■47,3±5,12 34±2,81 <0,01
Д. 28.12i2.98 18±4,12 <0,01
ср. 31,3±3,08 26±2,13 <0,01
ДПрЖе, мм рт.ст. 47,4±5,2 38±1,62 <0,01
с 10,01 ± 1,21 8,71±0,98 <0,05
ДсрПП, мм рт.ст. 7,33±0,95 65±0.49 <0,05
3. Кланичгскля эффективность метода дыхания исд избыточным давлением у больных аортальным стенозом в отеком лггсхж.
Был обследован 41 бальной аортальным стенозоми отехом легких, 19 из которых в комплексную терапию включали сеансы ДИД; 22 больных с общепринятой терапией составили Контрольную группу.
В исследуемой группе при купировании отека легких с применением ДИД отмечались выраженные изменения в сторону уменьшения таких показателей как СДЛЖ, КДЦЯЖ, КСОЯЖ и КДОЛЖ, СДЛА, ДДДА и ДЯАср., а также Ср. давление в правом предсердии (ЦВД). Эти изменения носили достоверный характер (табл.6).
Что касается клинических проявлений, то сеансы ДИД способствовали более быстрому уменьшению цианоза (среднее время в I группе составило 14,5±0,8 мин., во. II трушю - 35;2±1,2), быстрее уменьшалась одышка (ср. время в I группе составило 10,3±0,2 мин., во II группе - 32,3±0,6 мин.). Исчезновение ыихшых хрипов отмечалось скорее в основной группе (12,2±0,7 мин. - верхние доли, 17,2±1,2 мкн. -нижние доли), чем в контрольной (соответственно - 27±2,1 и 40±0,8). Отмечалось более раннее появление диуреза: 25,5±2,8 (11руппа) и 35,5±2,2 (II группа).
Таким образом, ДИД способствует более быстрому разрешению отека легких при включении его в комплексную терапию у бальных аортальным стенозом.
4. Клиническая эффективность метода ДИД у больших с пкзгртоничесхимя кризами, осложненными отекав летках и еердэтаон хстнай.
Было исследовано 22 бальных, у которых острая лгвожелудочховая недостг- точность сопровождалась подъемом АД до индивидуально высоких цифр. У 12 больных на фоне общепринятой терапии гипотензивными средствами, нейролептиками, вазодилататорами, диуретиками применяли метод ДИД.
Изучение показателей гемодинамики показало, чгсо ОЛН протекает при любых параметрах СИ (от 2 до 5,6 л/мин/м1), но при высоких цифрах АД (до 260/Ы. . рт.сг.) и ОПСС (до 4000 дин/с/см""), при этом отек легких у больных с малым СИ протекал при более низких цифрах АД. Резко возрастал ИРЛЖ (до 9,1±0,41 кгм/мин/ы*, при норме - 5,1 ххм/мин/м1).
Комтексная терапия с применением ДИД способствовала более быстрой нормализации гемодннамических показателей и эффективному разрешению клинических проявлений ОЛН.
Огыечастся тот факт, что при более быстром снижении АД на превых этапах у борных с традиционной терапией более замедлена реакция разрешения ОЛН по срапиению с больными (I группа) с применением ДИД.
При анализ? клинических прсяагатй ДИД способствует знач1ггеяыюму уменьшения сдышхи ка 5-3 0-й минуте у 50% бальных, полностью одьппка исчезла через 25 минут. Исчезновение влажных хрипов по всей поверхности легких отмечалось черех 20-30 мнут (в контрольной группе влажные хрипы в задне-нижних отделах сохранялись до 60 минут). Начало диуреза в основной группе отмечено от 15 до 40 минут, в ¡«¡игральной - к?.0-<£рминутам соответственно.
В I группе среднее время диуреза состазило 25,5±2,8 мин., во II гр}тше -35,5±2,2 мин. Различия в показателях достоверны.
Таким образом, результаты проведенных исследовшшй показывают, что включение в комплексную терапию кардиогенного отека легких метода дыхания под избыточным давлением +10 см водного столба способствует более быстрому его разрешению.
1. Суховоздушнсе погружение э иммерсионную среду может служить моделью галгргогкмии малого круга кровообращения, особенно в первые трое суток его пркмгизгшя.
2. В условиях "сухой" иммерсии происходи перераспределение крови с увеличением ее объгмг в сосудистых регионах головы и легких. Наиболее выраженные измякгепя гемеджтамихи происходят в первые трое сутох иммерсии.
3. В иммерсии развивается гиперкоагуляциошшй синдром: повышается адгезия тьюмбощпов, уровень фактора Виллсбрзнда, увеличивается агрегация тромбоцитов; ухудшаются показателя трсмбоэластограммы; увеличивается фибриноген, возрастает гег.«зтс:<р1гг, понижается уровень простациклина, повышается концентрация трсмбоксана, что соответствует реальней клинической ситуации отека легких у бояышх с сердечно-сосудистой патологией.
4. В условиях гиперволсмин малого круга кровообращения ухудшается мяк- рециркуляция за счет нарастания внутрисосудистой агрегации эритроцитов с замедлением сосудистого кровотока, нарушением проницаемости сосудистой стенки в виде появления перпмскуяяршм геморрагий.
5. В условиях "сухой" иммерсии снижается вентиляционная функция легких, сопровождающаяся артериальной гипоксенией, гиперкапнией и дыхательным ацидозом.
6. Дыхание под избыточным дзаташем +10 см водного столба у больных с пограничной артериальной гипертензией приводит к уменьшению кровенаполнения сосудистых зон головы и легких с одновременным увеличением крозопапатнешы
сосудов органов брюшной полости, в частности, печени, с восстановлением нор- , мального соотношения объемов крови верхней и нижней половин тела.
7. Применение ДИД в модельных исследованиях в течение первых трех суток способствует компенсации дыхательного ацидоза, коррекции нарушенной функции внешнего дыхания, предупреждает ухудшения микроциркуляции по данным конь- юнктивальной биомикроскопии. Устраняются признаки гиперкоагуляции в плазменном, тромбоцитарном и сосудистом звеньях гемостаза.
S. Дыхание под избыточным давлением +10 см водного столба является высокоэффективным, быстродействующим и доступным для общей клинической практики методом купирования кардиогенного отека легких: основные клинические проявления отека легких начинают уменьшаться с 5 минут применения ДИД и полностью купируются к 20 минуте, что создает необходимый резерв времени для проведения комплексной терапии.
9. Метод ДИД реализуется с помощью аппаратов "НИМБ-1" и "Выдох", созданных на основе экспериментальных и клинических данных, полученных в рамках настоящего исследования.
1. Метод "сухой" иммерсии позволяет моделировать состояние гиперволемии малого круга кровообращения для изучения патогенетических механизмов и разработки эффективных способов их коррекции.
2. Гиперволемия малого круга кровообращения, смоделированная методом "сухой" иммерсии, сопровождается изменениями КЩС, плазменного, сосудистого и тромбоцитарного гемостаза, микроциркуляции, функции внешнего дыхания, характерными для гиперволемии малого крута, развивающейся при острой левожелу- дочковой недостаточности у больных ОИМ, гипертонических кризах, осложненных отеками легких, пороках сердца.
3. Величина минутного объема сердца в условиях "сухой" иммерсии может определяться с помощью интегральной реографии с использованием коэффициента, соглас)ющего показатели МОС, полученного методами интегральной реографии и тгрмооилюции.
4. Для коррекции нарушений гемодинамики, развивающихся в условиях иммерсии. и ыие централиlaumi кровотока, сдвигоо КЩС, пшеркоагуляцнонного синдром:! угрозой развития тромбообразования, нарушения функции внешнего
дыхания, ухудшения микроциркуляции может с высокой эффективностью испсль- " зоваться метод дыхания под избыточным давлением +10 см водного столба.
5. Для купирования кардиогенного отека легких у больных в состоянии, угрожающем нарастающей асфиксией белковой пеной и фатальной артериальной гипоксемией, можно с высокой эффективностью применять в комплексной общепринятой терапии дыхание под избыточным давлением +10 см водного столба воздух или кислородно-воздушную смесь, в соотношении 1:1 - метод ДИД. Этот метод не требует сложной дыхательной аппаратуры, анестезиологической службы, может применяться в практической кардиологии, как в стационаре, так и в машине скорой помощи с помощью компактного аппарата "НИМБ-1", выпускаемого отечественной промышленностью и аппарата "Выдох", разработанного на основе результатов настоящего исследования.
Применение ДИД позволяет купировать альвеолярную стадию отека легких у больных ОИМ, пороками сердца, гипертонической болезнью за 10-20 минут без применения пеногасигелей. При этом создается оптимальный резерв времени для проведения комплексной терапии острой сердечной недостаточности.
Метод ДИД высокоэффективен профилактики угрожающего кардиогенного отека легких.
Выявленным противопоказанием для применения ДИД является выраженное нарушение сократительной функции правого желудочка.
1. Влияние нитроглицерина, мользидошша и шгтропруссида натрия на центральную гемодинамику и данные электрокардиографического и эхокардиографического исследования у больных острым инфарктом миокарда, /соавт.: Евдокимов В.В., Долотова В.В. и др.// Материалы III Всесоюзного съезда кардиологов, Москва^
1979, с.400-402.
2. Некоторые новые аспекты медикаменторной реабилитации больных острым инфарктом миокарда, /соавт.: Орлов В.Н., Радзевич А.Э. и др.//Тр. научно-практической конференции "Реабилитация при ИВС и пороках сердца", Горький, 1980, с.65-67.
3. Влияние водно-иммерсионной гиподинамии на некоторые показатели гемостаза у лиц с ПАГ. /соавт.: Орлов В.Г., Юнусов МА к др./Др. научно-практической конференции "Актуальные проблемы космической биологии и медицины", М.,
4. Application of ultiple precordial zeads to the evalnation of theeffectiveness of Drugs used to treat Acute miocardial infarction, /соавт.: Орлов B.H., Радзевич А.Э., Либов НА. и др. //Тр. международного симпозиума по элеюгрокардиологии, Будапешт,
1981, с.293-295.
5. Некоторые вопросы потогенеза и оптимизации терапии при инфаркте миокарда, /соавт.: Орлов В.Н., Уранов В.Н., Радзевич А.Э. и др.//Гр. XVIII съезда терапевтов, Ленинград, 1981, с.442-444.
6. Евдокимова А.Г., Кириченко ЛЛ., Смирнов В.В., Козлова В.Г. /Влияние термо- нейтральной "сухой" иммерсии на тромбоцктарный гемостаз, микроциркуляцию, лшшдный обмен и вязкость крови //В кн.: Влияние факторов внешней среды на организм человека: сборник научных трудов ММСИ, 1984, с.56-60.
7. Изучение влияния режимов сниженной гравитации ка организм условно здоровых мужчин в возрасте 45-55 лет, имеющих функциональные отклонения со стороны сердечно-сосудистой системы в виде нейроциркудяторной дистопии по гипертоническому типу и поиски метода адекватной коррекции этих состояний в условиях иммерсии. Изучение лечебного эффекта режима "сухой" иммерсии /соавт.: Орлов В.Н., Радзевич А.Э., Фомин И.О. и др.//Итоговын отчет, М., 1983, № депонир. 0-1429 в библнот. ИМБП, с.316.
8. Юнусов М.А., Евдокимова А.Г., Внноходова Т.В., Иванов С.Г. /Влияние "сухой" иммерсии на показатели гемодинамики и функциональное состояние эритрона у
бальных с артериальной гипертензией.//Влияние факторов внешней среды на организм человека: сборник научных трудов ММСИ, М., 1984, с.113-116. Состояние микроциркуляции и клеточного гемостаза у мужчин с ПАТ в условиях термонейтральной "сухой" иммерсии, /соавт.: Кириченко ЛЛ., Смирнов В.В.//Космическая биология и авиакосмическая мёдицина, 1985, №5 с.35-33.). Влияние нитропруссида натрия, пропранолола и маннитола на размеры инфаркта миокарда, /соавт.: Орлов В.Н., Радзевич А.Э., Шилова НА и др.//Кардиология, 1985, №4 с. 17-20.
".. Показатели гемостаза у лиц с НЦД, находящихся в условиях "сухой" иммерсии, /соавт.: Кириченко Л.Л., Масенко В.П., Раскуражен А.Б.//Космическая биология и авиакосмическая медицина, 1988, №1 с. 10-13. 1. Состояние центральной и периферической гемодинамики в 7-суточном режиме "сухой" иммерсии у лиц с НЦД по гипертоническому типу, /соавт.: Радзевич
A.Э., Соловьева A.B., Виноходова Т.В. и др.//Космическая биология и авиакосмическая медицина, 1989, №10 с.62-64.
Уточнение критериев отбора и поиск оптимальных средств физической профилактики гемодинамических, ортостатических и вестибулярных последствий сниженной гравитации применительно к спецконтингенту старших возрастных групп с НЦД по гипертоническому типу, /соавт.: Орлов В.Н., Радзевич А.Э., Кириченко ЛЛ., Несветов В.Н. и др.//Итоговый отчет N214-88060, инв. №336249/2984, депонир. во ВНИИТИ, М., 1988, с.293.
Способ оценки адаптации организма при моделировании состояний невесомости в условиях иммерсии. //A.c. №1352690, ДСП (соавт. с Орловым В.Н., Шульженко Е.Б., Урановым В.Н. и др.), 1988.
Способ профилактики патологических реакций при сниженной гравитации. //A.c. №1531269 ДСП (соавт. с Орловым В.Н., Радзевичем А.Э., Шульженко Е.Б.), 1989. Евдокимова А.Г., Юнусов М.А, Виноходова Т.В., О возможности применения "сухой" иммерсии в лечении артериальной гипертензии./Дез. доклада научно-практической конференции "Гипертоническая болезнь и сосудистые заболевания мозга", Пермь, 1990, с. 118-120.
Способ определения объемно-функциональных способностей левого желудочка сердца.//А.с. №1692553 (соавт. с Орловым В.Н., Дегтяревым ВА, Несветовым
B.Н. и др.), 1991.
Способ профилактики циркуляторных нарушений при сниженной гравита- ЦИИ.//А.С. №1724182 ДСП (соавт. с Радзевичем А.Э..Фомичевым В.Н., Урановым В.Н. и др.), 1991.
19. Сравнительная оценка влияния физических средств профилактики на гомеостаз у" лиц с НЦД по пшертош1ческому типу, //(соавг. Радзевичем А.Э., Кириченко Л Л., Несветовым В.Н. и др.)/Итоговый отчет х/д темы №89115, шт. №08/250, депонир. в ИМБП, М„ 1989.
20. Клинические испытания изделия "Выдох" у лиц с НЦД по гипертоническому-типу в режиме сниженной гравитации, //(соавт. с Радзевичем А.Э., Кириченко ЛЛ., Несветовым В.Н., Ольхиным ВА и др.)/ Итоговый отчет х/д темы №90133, в библ. ИМБП, № депонир. 08/250, 1990.
21. Гиперволемия малого круга кровообращения и способ ее компенсации методом дыхания под избыточным давлением, /соавт,: Радзевич А.Э., Кириченко Л.Л., Ольхин В.А., Евдокимов В.В. и др.//Сб. трудов научно-практической конференции МИД, М., 1993 с. 11-12.
22. Влияние "сухой" иммерсии и дыхания под избыточным давлением на состояние организма у здоровых лиц и больных ПАГ. /соавт.: Радзевич А.Э., Кириченко Л.Л., Ольхин ВА, Евдокимов В.В. и др.//Сб. научных трудов, М., 1993.
;-Т|!р. "£ (. Е-ла.
Гстпкрипг МЭСИ Б. Савв. пер. 5 Л