O.Ya. Babak, teraapiainstituut. L.T. Ukraina väike meditsiiniteaduste akadeemia
Äge gastrointestinaalne verejooks (AGH) võib olla mitmete haiguste tüsistus, erinevate autorite hinnangul on nende esinemissagedus 50-150 juhtu 100 tuhande elaniku kohta aastas. Näiteks USA-s põhjustavad FGCCd igal aastal rohkem kui 300 000 haiglaravi. Meestel esineb AHCC kaks korda sagedamini kui naistel. Sõltuvalt FGCC kliiniliste ilmingute raskusastmest on ilmne või latentne, võttes arvesse erinevusi diagnostilises ja terapeutilises taktikas, on tavaks eristada verejooksu seedetrakti (GIT) ülemisest ja alumisest osast. Teisest küljest verejooks ülemised divisjonid Seedetrakt jaguneb mitte-söögitoru veenilaienditeks ja verejooksudeks söögitoru veenilaienditest. Seedetrakti alumise osa verejooksu allikas on Treitzi sideme suhtes distaalne ja hõlmab enamasti verejooksu käärsoolest. Kui verejooksu allikas asub Treitzi sideme ja ileotsekaalklapi vahel, nimetatakse seda peensooleks.
Seedetrakti ülaosa verejooks moodustab ligikaudu 90% kõigist seedetrakti verejooksu juhtudest. Sest Viimastel aastatel nende verejooksude kõrge suremus on püsivalt säilinud - 8-10% tasemel.
Verejooks alumisest seedetraktist on harvem ja moodustab ligikaudu 10-20% kõigist seedetrakti verejooksudest, esineb mõnevõrra sagedamini meestel ja on valdavalt eakate inimeste patoloogia. Ameerika Ühendriikides registreeritakse haiglaravi vajavat verejooksu alumisest seedetraktist sagedusega 20 juhtu 100 000 elaniku kohta aastas. Erinevate allikate kohaselt peatub selle lokaliseerimise verejooks 36-85% juhtudest iseenesest.
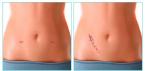
Operatsiooni oodatav kasu seisneb selles, et kaotate olulise osa oma ülekaalust ilma seda pikemas perspektiivis tagasi võtmata ning vähendate või isegi kaotate sellega kaasnevaid haigusi, nagu kõrge vererõhk, diabeet, uneapnoe või liigesevalu.
Selle protseduuriga oodatakse keskmiselt 40–60% liigset kaalukaotust. Seega on kaalulangus keskmiselt 20–30 kg.
- Mis on tööaeg?
- Mis on haiglaravi kestus?
Verejooks seedetrakti ülemisest osast
Seedetrakti verejooksu põhjused
Seedetrakti ülaosa verejooksu kõige levinumad põhjused on mao ja kaksteistsõrmiksoole (kaksteistsõrmiksoole) erosioonilised ja haavandilised kahjustused 35-53% juhtudest; mao limaskesta kahjustus mittesteroidsete põletikuvastaste ravimite (MSPVA-de) võtmise ajal, eriti üle 60-aastastel patsientidel (tabel 1); 3-4% juhtudest on verejooksu põhjuseks mao- ja kaksteistsõrmiksoole kasvajad, nii hea- kui pahaloomulised. Ligikaudu 3% seedetrakti ülaosa AHK-ga patsientidest on Mallory-Weissi sündroomi ilming - mao südameosa limaskesta kitsad lineaarsed rebendid, mis tekivad koos tugeva oksendamisega.
Haruldased verejooksu põhjused seedetrakti ülaosast on mao ja soolte veresoonte angiodüsplaasia (Weber-Osler-Rendu tõbi), aordi aneurüsmi rebend (tavaliselt kaksteistsõrmiksoole luumenis), tuberkuloos ja mao süüfilis, hüpertroofiline polüadenomatoosne gastriit (Menetrieri tõbi), võõrkehad maos, pankrease kasvajad (virsungorraagia), kahjustused sapijuhad või maksa vaskulaarsete moodustiste rebend (hemobilia), vere hüübimishäired (trombotsütopeenilised seisundid ägeda leukeemia korral, fulminantne maksapuudulikkus).
Kõige tavalisem põhjus on pädevate organite, st söögitoru, mao või kaksteistsõrmiksoole haigus. Sellise patsiendi hoolduse aluseks ei ole mitte ainult haiglaravi koos elutähtsate näitajate intensiivse jälgimisega, vaid peamiselt multidistsiplinaarse meeskonna olemasolu, mis peaks olema diagnostilises ja terapeutilises protsessis üks tervik. Endoskoopia mängib võtmerolli, mis mitte ainult ei määra insuldi allikat, vaid saab enamikul juhtudel läbi viia samaaegselt. tõhus ravi.
Seedekanali verejooksu kliinilised ilmingud
Seedetrakti ülaosa verejooksu peamised kliinilised tunnused (otsesed sümptomid) on oksendamine verega (hematemees) ja/või must, tõrvajas väljaheide (melena).
Hematemesi täheldatakse tavaliselt märkimisväärse verekaotusega (üle 500 ml) ja reeglina kaasneb sellega alati melena. Söögitoru arterite verejooksu iseloomustab oksendamine muutumatu vere seguga. Maoverejooksu korral näeb oksendamine välja nagu "kohvipaks", mis on tingitud hematiinkloriidi moodustumisest hemoglobiini ja vesinikkloriidhappe koosmõjul. Raske hüpokloorhüdriaga (näiteks maovähiga), samuti juhtudel, kui mao verejooks rohke, sisaldab oksendamine muutumatul kujul verd.
Melena kaasneb sageli verega oksendamisega, kuid seda võib täheldada ka ilma selleta, see on tüüpiline kaksteistsõrmiksoole verejooksule, kuid esineb sageli kõrgema asukohaga verejooksu allikate korral, eriti kui see toimub piisavalt aeglaselt. Enamasti tuvastatakse melena mitte varem kui 8 tundi pärast verejooksu algust ja selle tekkeks võib juba piisata 50-80 ml verekaotusest. Millal mitte rikkalik verejooks, samuti soolesisu läbipääsu aeglustamisel omandavad väljaheited musta värvi, kuid jäävad vormituks.
Väljaheite tume värv (pseudomeleen) on tüüpiline raua, vismuti, aktiveeritud süsinik, teatud toitude söömisel (keedetud peet, mustikad, mustad sõstrad jne). Sisu kiirendatud läbimisel soolestikku, vähem kui 8 tundi ja verekaotusega üle 100 ml, võib seedetrakti ülaosa verejooks väljenduda punase vere vabanemises väljaheites (hematoheesia), mida peetakse iseloomulikumaks. verejooks alumisest seedetraktist. Umbes 5% haavanditega patsientidest on haavandi verejooksu ainsaks kliiniliseks sümptomiks hematoheesia.
TO üldised sümptomid, või kaudsed verejooksu tunnused on üldine nõrkus, pearinglus, tinnitus, silmade tumenemine, õhupuudus, südamepekslemine. Mõnel juhul võivad kaudsed seedetrakti verejooksu sümptomid eelneda melena ja hematemesi ilmnemisele, harvemini - domineerivad kliiniline pilt. Kui punakaspunase vere vabanemine väljaheites on tingitud seedetrakti alumisest verejooksust, ilmnevad kaudsed sümptomid pärast hematoheesiat ega eelne selle ilmnemisele.
AHCC raskusastet selle arengu esimestel tundidel hinnatakse vererõhu languse astme, tahhükardia raskusastme (asendimuutused) ja tsirkuleeriva vere mahu defitsiidi (BCC) järgi. Posturaalset hüpotensiooni ja tahhükardiat iseloomustab vähenenud süstoolne rõhk 10-20 mm Hg juures. Art. vahetusel horisontaalne asend vertikaalseks ja südame löögisageduse tõus 20 lööki/min või rohkem. BCC defitsiidi hindamiseks kasutatakse šokiindeksi näitajaid, mis arvutatakse Algoveri meetodil, mis defineeritakse pulsisageduse jagatis süstoolse rõhu väärtusega. Indeksiga 0,5 on BCC puudujääk 15%, 1,0 - 30%, 2,0 - 70%. ACHK-l on kolm raskusastet (tabel 2).
Enam kui 80% juhtudest peatub seedetrakti ülaosa verejooks iseenesest, mistõttu vajavad patsiendid ainult sümptomaatilist ravi. Enamikul patsientidest peatub verejooks enne haiglasse lubamist mõni tund pärast haiglaravi, kuna spontaanne hemorraagia tekib tavaliselt esimese 12 tunni jooksul.
On oluline, et sellised teenused oleksid tsentraliseeritud ja institutsionaalsed siduva direktiiviga, et parandada nende patsientide ravi kvaliteeti üksikutes tervishoiuasutustes. Seedetrakti verejooks on endiselt tõsine meditsiiniline probleem. Äge verejooks on gastroenteroloogias väga dramaatiline, eluohtlik seisund. Seevastu krooniline verejooks on peamiselt diferentsiaaldiagnostika ja see ei ole selle väite teema.
Eelkõige on seedetrakti ülaosa verejooks pidev kõrge haigestumus, meditsiiniline draama ja mõnikord isegi uusimate diagnostiliste ja raviprotseduuride korral juhitamatu. See on endiselt koormatud kõrge letaalsusega. Mehed kannatavad sagedamini, üle 60-aastaste vanuserühmas on rohkem kui kaks kolmandikku patsientidest.
Seedetrakti verejooksu diagnoosimine
Seedetrakti ülaosa verejooksu diagnoosimisel on väga oluline põhjalik haiguslugu (varem peptilise haavandi esinemine, mittesteroidsete põletikuvastaste ravimite või antikoagulantide võtmine, alkoholi kuritarvitamine, telangiektaasia nahal ja limaskestadel jne).
AGCC kahtlusega patsientide uurimisel on vaja dünaamiliselt jälgida laboratoorseid parameetreid (hemoglobiin, protrombiin, fibrinogeen, hematokrit, erütrotsüütide ja trombotsüütide arv, veritsusaeg jne), kindlasti määrata veregrupp ja Rh-faktor ning teostada ka terviklikku instrumentaalne uurimine verejooksu allika kindlakstegemiseks.
Seedetrakti ülaosa AHCC-ga patsientidel tehakse peamiselt esophagogastroduodenoscopy, mis peaks olema võimalikult kiireloomuline, kuna patsiendi prognoos sõltub sageli verejooksu allika tuvastamise õigeaegsusest. Nasogastraalsondi esialgne sisestamine kinnitab vere olemasolu maosisus. Tuleb meeles pidada, et ligikaudu 10% veritseva kaksteistsõrmiksoole haavandiga patsientidest ei tuvastata ninasonditoru sisestamisel ja maosisu eemaldamisel verd.
Endoskoopiline uuring võimaldab 70% juhtudest määrata seedetrakti ülaosa verejooksu allika. Sõltuvalt patsientide endoskoopilisest pildist peptiline haavand määrata aktiivne ja peetav seedetrakti verejooks (vt lõik "Sõnastik"). Aktiivne verejooks võib endoskoopiliselt väljenduda arteriaalse jugaverejooksuna (Forrest Ia tüüp), aeglase vere vabanemisega verejooksuna (Forrest Ib tüüp), verejooksuna aeglase vere vabanemisega kõrvalasuvast trombist. Tekkinud verejooksu iseloomustab endoskoopiliselt trombi või pindmiselt paiknevate verehüüvete tuvastamine haavandi põhjas koos nähtava mitteverejooksu alaga. veresoon(tüüp Forrest II). Mõnel juhul avastatakse endoskoopilisel uurimisel erosioon- ja haavandilised kahjustused ilma verejooksu tunnusteta (Forrest III tüüp).
Kui verejooksu allikat ei ole võimalik endoskoopia käigus tuvastada, kasutatakse angiograafiat ja stsintigraafiat, mis võimaldavad kontrollida angiodüsplaasia olemasolu.
Diagnostilised meetmed ja intensiivravi AJCC-ga patsientidel tuleb läbi viia paralleelselt.
Vaadeldud tulemuse põhjal saab prognoosida korduva verejooksu ja suremuse ohtu. Vastupidi, korduva verejooksu sagedus pärast endoskoopilist ravi vähenes veidi ja suremus vähenes selle komplektis vaid 1%. kõrgendatud keskmine vanus, raskem kaasuv haigus ja peaaegu muutumatu primaarse hemostaasi verejooksu kordumise määr on kõige olulisemad tegurid, mis põhjustavad peaaegu muutumatut suremust. Melanoom nõuab ägedat verekaotust vähemalt 100 ml.
Seedetrakti verejooksu ravi
GI ravi üldpõhimõtted on järgmised:
patsiendi erakorraline hospitaliseerimine kirurgiaosakonda;
maksimaalselt kiire taastumine BCC, kasutades lavastust intravenoosne kateeter ja järgnevad infusioonravi, erütrotsüütide massi ülekanne, mida täiendatakse vere hüübimishäirete esinemisel värske külmutatud plasma ja trombotsüütide massi ülekandega;
hemostaatiline ravi.
Seedetrakti verejooksuga patsientide ravimise algoritm on näidatud joonisel. Vereülekannet tehakse hüpovoleemilise šoki sümptomitega, samuti hemoglobiinisisaldusega alla 100 g / l (10 g%). Vajalik ülekantud veredooside arv (n), igaüks 500 ml, arvutatakse järgmise valemiga: n = 10 - X (kus X on hemoglobiini kogus grammides). Šoki sümptomite esinemisel lisatakse 4 annust verd ja kui verejooks jätkub pärast esialgset peatumist, lisatakse veel 2 annust. Aktiivse haavandilise verejooksu (juga või aeglane verejooks) nähtude avastamine endoskoopilisel uurimisel on näidustus verejooksu peatamiseks endoskoopiliste meetodite kasutamiseks, mis sellistel juhtudel vähendavad tõhusalt korduva verejooksu riski, suremust ja erakorraliste kirurgiliste sekkumiste sagedust. .
Farmakoloogiline hemostaas hõlmab antisekretoorsete ravimite intravenoosset manustamist, kuna need stabiliseerivad fibrinogeneesi, soodustavad trombide moodustumist, vähendavad tsentraalset verevoolu ja verevoolu haavandisse. Nende hulka kuuluvad: H 2 -histamiini retseptorite (H 2 -BG) blokaatorid - ranitidiin, famotidiin; prootonpumba inhibiitorid (PPI-d) - omeprasool, pantoprasool, esomeprasool; somatostatiini analoogid - sandostatiin, stülomiin.
Ranitidiini manustatakse intravenoosselt 50 mg iga 6-8 tunni järel; omeprasool - in / in tilguti 40 mg / päevas; famotidiin - 20 mg IV soolalahuses; Pantoprasool - 40 mg IV, samal ajal manustatakse intravenoosselt aminokaproonhapet 100 ml 5%, vikasooli 2 ml 1%. Sandostatiini intravenoosne pidev infusioon (25 mikrogrammi tunnis) viiakse läbi 5 päeva jooksul.
Endoskoopilise hemostaasi meetodid hõlmavad järgmist:
kontakttermokoagulatsioon (krüo- ja elektro-);
mittekontaktne koagulatsioon (argoon, laser);
süstid (epinefriin, sklerosandid);
mehaaniline hemostaas (lõikamine).
Kirurgilise sekkumise näidustused määratakse tavaliselt individuaalselt, operatsiooni ajastamise osas pole rangeid reegleid. Kõige keerulisem ülesanne on teha otsus lõpetada konservatiivne ravi. IN kirurgiline sekkumine Tavaliselt vajavad järgmised patsientide kategooriad:
eakad patsiendid, kellel on püsiv või korduv verejooks, kuna nad ei talu verekaotust ja vereülekannet. Reeglina viiakse konservatiivne ravi läbi mitte kauem kui 24 tundi;
üle 60-aastased peptilise haavandiga patsiendid kaksteistsõrmiksoole haigus sattus kliinikusse tugeva verejooksuga;
patsiendid, kellel on maohaavandi tõttu tugev verejooks (operatsioon on sageli vajalik, kuid mitte alati).
Erakorraline operatsioon on vajalik järgmistel juhtudel:
perforeeritud haavand koos verejooksuga;
Pärast 1500 ml vere kiiret ülekannet ei normaliseerunud ega stabiliseerunud vererõhk ja pulss;
Vererõhk ja pulss on stabiliseerunud, kuid nende normaalsel tasemel hoidmiseks on vaja üle 1500 ml verd üle kanda vähem kui 24 tunni jooksul;
verejooks kestab kauem kui 24 tundi, verejooksu allikat on võimalik kirurgiliselt kõrvaldada, kuna vaid vähesed patsiendid taluvad 24-48 tundi kestvat veritsust;
verejooks peatus, kuid pärast haiglaravi jätkus konservatiivse ravi taustal;
pole piisavalt ühilduvat verd;
korduv verejooks on vältimatu (näiteks aortoduodenaalse fistuliga).
Mõnede ravimata ameeriklaste puhul ei pruugi ägeda verejooksuga kaasneda ükski ülalloetletud sümptom, seega ei tohiks kunagi ära jätta rektaalset uuringut. Mõnikord domineerivad kliinilises pildis hemodünaamilise ebastabiilsuse sümptomid, millega kaasneb minestus, ülalkirjeldatud sümptomid.
Samuti on kasulik jagada etioloogilisest aspektist veenilaienditeks ja mittevakroskoopiliseks hemorraagiaks, mis on eriti oluline edasises ravis. Peaaegu pooled mao-kaksteistsõrmiksoole haavandite juhtudest, ka sagedased verejooksud söögitorust, harva mao veenilaiendid, tavaliselt väga kiire progresseerumisega. Me ei tohiks unustada hemorraagilise gastropaatia difuusset verejooksu.
Seedetrakti verejooksu ennetamine
Helicobacter pyloriga seotud haavandite korral on vaja läbi viia anicheliobacter pylori (AHBT) likvideerimisravi, kuna pärast bakterite hävitamist ei ületa haavandite kordumise sagedus täiskasvanutel 5-10% aastas, korduv verejooks - 0,5%. Stressihaavandite verejooksu vältimiseks määratakse sekretsioonivastased ravimid (H 2 -BG - famotidiin või PPI) on kohustuslik ägedate ja raskete somaatiliste seisundite korral, intensiivravi ajal ja pärast operatsioone. MSPVA-de kasutamisega seotud verejooksu vältimiseks tuleb meeles pidada, et mittespetsiifiliste mittesteroidsete põletikuvastaste ravimite pikaajaline kasutamine peaks toimuma sekretsioonivastaste ravimite või antatsiidide varjus.
Muud röntgeni- või radioisotoopide meetodid on piiratud väärtusega ja neid kasutatakse ainult pärast endoskoopia ebaõnnestumist. Endoskoopilise lähenemise vaieldamatu eelis on võimalus ühe seansi jooksul läbi viia nii diagnostilist kui ka terapeutilist ravi.
Toitumine ja mao veenilaiendid põhjustavad ägedat verejooksu 10% juhtudest. Rebenemise oht suureneb koos veenilaiendite suuruse, nende esiletõstmise, portohepaatilise gradiendi tõusuga üle 12 mm ja maksahaiguse raskusastmega. See on alati dramaatiline sündmus, mis avaldub hematemisatsiooni alguses ja veelgi suurema letaalsusega. Söögitoru muutused tekivad üksi või nendega kaasnevad veenilaiendid kõht. Veenilaiendid tekivad eriti portaalhüpertensiooni taustal, millega kaasneb peamiselt kaugelearenenud maksahaigus, mistõttu hemostaas soodustab protrombiini ja teiste prokoagulantvalkude vähenenud sünteesist tingitud hemostaasi, samuti trombotsütopeeniat.
Verejooks söögitoru veenilaienditest
Söögitoru veenilaiendite verejooks esineb 30% juhtudest maksatsirroosiga patsientidel ja mõnel juhul võib see olla põhihaiguse esimene ilming. Esimese aasta jooksul pärast verejooksu esineb ägenemisi 70% patsientidest, suremus söögitoru veenilaiendite igas verejooksu episoodis on 25-40%. Verejooks on sagedamini tugev, tavaliselt väljendub tume kirsivärvi verine oksendamine ja võib kiiresti viia hüpovoleemilise šoki ja surmani. Mõnel juhul jätkub verejooks korduvate episoodide kujul koos väikese verekaotusega mitu päeva või isegi nädalat. Selline verejooks aitab kaasa maksafunktsiooni halvenemisele, astsiidi suurenemisele, hepaatilise entsefalopaatia sümptomite ägenemisele, mille tulemuseks on maksakooma, ja hepatorenaalse blokaadi teket.
Söögitoru veenilaiendite verejooksu saab kõige paremini kontrollida endoskoopilise skleroteraapia või veritsevate veenide endoskoopilise ligeerimisega. Skleroseeriva ravi käigus tekivad ligikaudu 20% juhtudest erinevad tüsistused, nagu haavandid, striktuurid, söögitoru motoorsed häired ja mediastiniit. Söögitoru veritsevate veenilaiendite endoskoopiline ligeerimine on üsna tõhus, tüsistuste esinemissagedus selle rakendamisel on palju väiksem.
Intravenoosne vasopressiin näitab head hemostaatilist toimet söögitoru veenilaiendite verejooksu korral, kuid puuduvad tõendid selle kohta, et selle kasutamine pikendaks patsientide eeldatavat eluiga. Nitroglütseriini samaaegne intravenoosne manustamine vähendab vasopressiini kahjulikku mõju südame-veresoonkonna süsteem. Mõned uuringud näitavad, et ka somatostatiini intravenoosne manustamine tõhus meetod peatada verejooks söögitoru veenilaienditest, millel on palju vähem hemodünaamilisi kõrvalmõjusid. Vasopressiini manustatakse intravenoosselt 20 RÜ 100 ml 5% glükoosilahuse kohta, pärast mida lülituvad nad üle ravimi aeglasele infusioonile 4–24 tunni jooksul kiirusega 20 RÜ tunnis, kuni verejooks täielikult peatub. Kui vasopressiini või somatostatiini manustamine ei peata verejooksu, tuleb verejooksu söögitoru veenilaiendite korral rakendada Sangstaken-Blackmore või Minnessota-Lintoni sonde kasutades balloontamponaadi.
Ebaefektiivse skleroteraapia korral (verejooks ei peatu või taastub pärast skleroseerivate ainete kahekordset süstimist) rakendatakse porto-caval šunti. On soovitav, et patsiendil oleks normaalne või äärmuslikel juhtudel vähe kõrgendatud tase bilirubiin, lähedal normaalne tase seerumi albumiin, entsefalopaatia ja astsiidi tunnuseid ei esinenud.
Enamik Mallory-Weissi sündroomiga patsiente teatavad alustamisest suur hulk kontsentreeritud alkohol. Korduv oksendamine või köhimine suurendab intraabdominaalset rõhku, mis võib põhjustada limaskesta ja alamkihi lõhenemist gastroösofageaalse ristmiku piirkonnas koos pragude ja sellele järgneva verejooksuga, mis enamikul juhtudel peatub spontaanselt. Alkohoolikute mõõduka verejooksu põhjuseks on prolapsist tingitud gastropaatia. See on täpselt määratletud subepiteliaalse hemorraagia piirkond koos tsentraalse erosiooniga, mis asub gastroösofageaalsest ristmikul distaalselt.
Soolestiku verejooks
Soolestiku verejooksu põhjused
Peen- ja jämesoole verejooksu põhjused võivad olla põletikulised soolehaigused (haavandiline koliit, Crohni tõbi), peensoole (lümfoomid) ja jämesoole kasvajad (kolorektaalvähk, adenoomid), isheemiline koliit, soole divertikuloos, hemorroidid ja lõhed anus, limaskestade kavernoossed hemangioomid ja telangiektaasiad peensoolde(Randu-Weber-Osleri tõbi), aordi-soolestiku fistulid, divertikulaar niudesool või Meckeli divertikulaar (noortel).
Põhjuseks on mao limaskesta prolaps pideva oksendamise ajal söögitorusse. Need on enamasti väikesed lamedad haavandid või haavandid, mis paiknevad sambaepiteeliga söögitoru osas, mida vähemalt mõnes osas iseloomustab soole metaplaasia. Maohaavandiga patsientidel on see sagedamini kui melaniini esimene hematemeesverejooksu ilming, kaksteistsõrmiksoole haavandi puhul on see vastupidi, hematemisatsioon on harvem.
Verejooks on peptilise haavandi esimene ilming ligikaudu igal neljandal patsiendil, tavaliselt olenevalt haavandi suurusest ja sügavusest. Verejooksu raskusaste oleneb erodeeritud veresoone suurusest ning kapillaar-, venoossest või arteriaalsest verejooksust. Vere suunamine haavandi alumisest osast on kapillaarset päritolu, aeglaselt ja pidevalt voolav veri näitab venoosset verejooksu ja pulseerivaid väljendunud verepritsmeid arteriaalse päritoluga luumenisse.
Soolestiku verejooksu kliinilised ilmingud
Erinevalt söögitoru ja mao verejooksust on sooleverejooksu kliinilised ilmingud mõõdukamad ja sageli ei kaasne sellega üldisi sümptomeid. Mõnikord teatavad patsiendid vahelduvast sooleverejooksust ainult hoolika küsitlemisega. Massiivne sooleverejooks on haruldane.
Järgmise patsiendi prognoosi jaoks on Forresti sõnul primaarse peptilise haavandi klassifikatsioonil praktilised tagajärjed. Kõrgel väikese mao kõverusel või kaksteistsõrmiksoole sibula tagumisel seinal paiknevatel haavanditel on pärast endoskoopilist ravi tõenäolisem verejooks, mistõttu on sellel patsientide rühmal ka halvem prognoos ja oluliselt kõrgem suremus.
Nii mao-kaksteistsõrmiksoole haavandi haiguse etiopatogenees kui ka haavandilistest kahjustustest tingitud verejooksu etiopatogenees mängivad olulist rolli mitmes teguris. Pole kahtlust, et mõlemad need tegurid on seotud gastroduodenaalse haavandi haiguse etiopatogeneesiga, kuid nende vastastikune koostoime ei ole veel lahendatud. Neid on üsna palju, nad võivad olla nii maos kui ka kaksteistsõrmiksooles. Neid seostatakse sageli õnnetusjuhtumi või suurema operatsiooniga. Need on valutud ja verejooks on nende esimene ilming.
Soolestiku verejooksu diagnoosimine
Kõige sagedamini ilmneb sooleverejooksuga muutumatu veri (hematoheesia). On teada, et mida kergem veri pärasoolest vabaneb, seda distaalsemalt paikneb verejooksu allikas. Tõepoolest, sarlakpunane veri on valdavalt iseloomulik verejooksule, mis tekib sigmoidi ja/või pärasoole mõjul, samas kui tumepunane veri ("burgundia veini" värvus) näitab verejooksu allika paiknemist proksimaalsemas käärsooles. Perianaalse piirkonna kahjustusega (hemorroidid, lõhed) seotud verejooksu korral ei segune eraldunud veri (jälgede kujul tualettpaberil, WC-poti seintele langevate tilkade kujul) tavaliselt väljaheitega, mis säilitab oma pruuni värvi. värvi. Kui verejooksu allikas asub rektosigmoidse käärsoole proksimaalselt, on veri enam-vähem ühtlaselt segunenud väljaheitega, nii et tavaliselt ei ole võimalik tuvastada selle tavalist pruuni värvi. Sooleverejooksu episoodile eelnev kõhuvalu viitab ägedale nakkuslikule või kroonilisele haigusele. põletikulised haigused sooled, peen- või jämesoole ägedad isheemilised kahjustused. Ootamatu teravad valud kõhuõõnes, millega kaasneb sooleverejooks, võib põhjuseks olla aordi aneurüsmi rebend kaksteistsõrmiksoole luumenisse. Valu pärasooles defekatsiooni ajal või pärast seda süveneb tavaliselt hemorroidide või pärakulõhega. Valutut massilist sooleverejooksu täheldatakse soole divertikuloosi, telangiektaasia, Meckeli divertikuli haavandumise korral.
on suure diagnostilise väärtusega kliinilised sümptomid seotud sooleverejooksuga. Tavalised on äge palavik, kõhuvalu, tenesmus ja kõhulahtisus nakkushaigused jämesool. Sooletuberkuloosi kliinilises pildis esineb sageli pikaajaline palavik, higistamine, kehakaalu langus, kõhulahtisus. Palavik, artriit, aftoosne stomatiit, nodoosne erüteem, primaarne skleroseeriv kolangiit, silmakahjustused (iriit, iridotsükliit) on iseloomulikud kroonilistele põletikulistele soolehaigustele. Kiiritusproktiidi korral on sümptomid (kiire väljaheide, tenesmus) sageli kombineeritud kiiritusenteriidi kliiniliste ilmingutega (rohke vesine väljaheide, steatorröa, malabsorptsiooni sündroomi nähud).
Massiivse sooleverejooksuga röntgenuuring (irrigograafia) ei ole näidustatud selle vähese infosisalduse ja suurte raskuste tõttu, mida see tekitab edasiseks uurimiseks. Praegu on verejooksu diagnoosimisel peamine roll kolonoskoopial, enne mida on mõistlik teha sigmoidoskoopia, et välistada võimalik verejooksu allikas pärakukanalis (hemorroidid, pärakulõhe). Tuleb meeles pidada, et potentsiaalse verejooksu allika avastamine ei välista peamise patoloogilise fookuse olemasolu proksimaalses soolestikus.
Küsimus verejooksuga patsiendi ettevalmistamise vajaduse kohta ajab arstid sageli segadusse, kuna kardetakse selle suurenemist või taastumist. Kui aktiivne veritsus jätkub, on aeg kallis ja kohe tuleb läbi viia uuring. Kui verejooks peatub, peate esmalt puhastama soolestikku. Ettevalmistuseta läbivaatus on keerulisem, seotud patoloogia "kaotamise" ohuga (kuigi veri ise on hea lahtistav toime ja mõnel juhul on soolestik uurimiseks üsna kättesaadav). Klistiir on seotud vere retrograadse tagasivooluga proksimaalsesse soolde, mis võib diagnoosimise keeruliseks teha ja on veritsevale patsiendile äärmiselt raske (piisava puhastamise jaoks on vaja 4-5 klistiiri). Sellega seoses on eelistatav suu puhastamine osmootse toimega lahtistitega, näiteks kombineeritud ravim makrogool (4 liitrit 3-4 tunni jooksul). Viimasel ajal on laialdaselt arutatud kapsli endoskoopia rolli peensoole verejooksu diagnoosimisel.
Limaskesta põletiku leevendamisel leiti arvukalt väikeseid pindmisi kahjustusi, mis häirivad ainult mao limaskesta ja kaksteistsõrmiksoole sibulat, kuid ei tungi lihaskiht on iseloomulikud hemorraagilisele gastropaatiale ja bulbopaatiale. See on alati pindmine limaskesta kahjustus, mis ei häiri veritsevate laikude ja petehhiate ning vanemate erosioonidega lihaskihti.
Angiodüsplaasia mao või kaksteistsõrmiksoole limaskestas on tavaline eakatel patsientidel neerupuudulikkus või süsteemne haigus, on raske ägeda verejooksu põhjus ligikaudu 5% kõigist juhtudest. Põhimõtteliselt on see diagnostiline ja terapeutiline probleem.
Sooleverejooksu ravi põhimõtted
Kui sooleverejooksu allikat ei ole võimalik endoskoopiliste meetoditega kindlaks teha, kasutatakse selektiivset angiograafiat ja stsintigraafiat, mis võimaldavad tuvastada peensoole limaskesta angiodüsplaasiat ja telangiektaasiat. Ligikaudu 80% ägeda sooleverejooksu juhtudest peatub spontaanselt. Endoskoopilise uurimise ajal (verejooksu polüüpide, angiodüsplaasiaga) võib kasutada elektrokoagulatsiooni või laserkoagulatsiooni. Jätkuva sooleverejooksu korral kaalutakse operatsiooni (segmentaalne resektsioon või hemikolektoomia).
Samal ajal on diagnostilise endoskoopia ja angiograafia meetodite kaasaegne areng oluliselt hõlbustanud seedetrakti verejooksuga patsientide ravi. Terapeutiline endoskoopia (verejooksu allika koagulatsioon) ja terapeutiline angiograafia (vasokonstriktorite selektiivne infusioon, verejooksu veresoone emboliseerimine) võimaldavad üha enam vältida erakorralist kirurgilist sekkumist.
Seega on seedetrakti verejooksu probleem olnud ja jääb aktuaalseks. Vaatamata diagnostiliste ja ravivõimaluste laienemisele on verejooksude risk ja nende eluohtlikkus endiselt üsna kõrge. Samas lihtsustab täpne teave verejooksu allika kohta patsiendi juhtimist, hõlbustab ravitaktika valikut ja vähendab arstide töökoormust.
Praegu saab enamikul juhtudel AJCH-d ravida konservatiivselt või minimaalselt invasiivsete meetoditega – kasutades farmakoloogilist ja endoskoopilist hemostaasi. Tõhus hemostaas ja verejooksu vältimine on enamikul juhtudel võimalik vesinikkloriidhappe tootmise farmakoloogilise blokeerimisega, kasutades parenteraalseid somatostatiini analooge, PPI-sid, H2-blokaatoreid histamiini retseptorid(famotidiin). AHCC ja nende retsidiivide õigeaegne ja korrektne ennetamine, antisekretoorsete ravimite kasutamine "kattena" pikaajaliseks kasutamiseks mitteselektiivsed mittesteroidsed põletikuvastased ravimid, stressihaavandite ennetamine sisearsti ja arsti poolt üldpraktika võib aidata verejooksu sagedust oluliselt vähendada.
Nad võivad veritseda nii kartsinoomide kui ka lümfoomidega ning leiomüosarkoomiga patsientidel esineb sageli märkimisväärne verejooks. Erandiks on polüübid, nii hüperplastilised kui ka adenomatoossed. IN diferentsiaaldiagnostika samuti on võimalik vältida naaberorganites lokaliseeritud haigusi, multisüsteemseid haigusi, vere- ja veresoonkonnahaigusi.
Terminit hemobilia kasutatakse sapiteede verejooksu kohta. Enamasti seostatakse seda maksakahjustusega või maksaarteri ja selle harude aneurüsmi rebendiga, harvaesinevaks hemobilia põhjuseks on kasvaja või abstsess maksa parenhüümis. Tähelepanu tuleb pöörata ka maksa ja sapiteede iatrogeense kahjustuse võimalusele seoses biopsiaga või sapi äravoolu kasutuselevõtuga. Verejooks kõhunäärme väljapääsust on väga haruldane.
Kirjandus
1. Ivaškin V.T., Lapina T.L. Seedesüsteemi haiguste ratsionaalne farmakoteraapia: juhend praktiseerivatele arstidele. M., Kirjandus, 2003, 1046s.
2. Fedorov E.D., Mihhalev A.I., Orlov S.Yu., Timofejev M.E., Tšernjakevitš P.L., Plakhov R.V. Ägeda gastroduodenaalse verejooksu endoskoopiline diagnoosimine ja peatamine ning nende kordumise ohu ennustamine. Vene gastroenteroloogia, hepatoloogia, koloproktoloogia ajakiri. 2002, nr 1, lk. 9-18.
3. Bohnacker S., Sriram P.V.J., Soehendra N. Endoskoopilise ravi roll verejooksu veenilaiendite ravis. Bailliere's Clin Gastroenterol. 2000; 3:477-94.
4. Corky D.A., Cello J.P., Adkisson W., Ko W.F., Kerlikowske K. Oktreotiid ägeda söögitoru veenilaiendite verejooksu korral: metaanalüüs. gastroenteroloogia. 2001 märts; l 20 (4): 946-54.
5. Donahue P. E. ja Nyhus L. M. Massive Upper Gastrointestinal Hemorrhage in Surgery of the Sophagus, Stomach and Peensoole (5. väljaanne). Boston: Little, Brown, 1999.
6. Goetzsche P. C. Somatostatiini analoogid ägedate verejooksude söögitoru veenilaiendite korral. In: The Cochrane Library, Issue 2, 2003; Oxfordi värskendustarkvara.
7. Harris A., Stebbing J. Seedetrakti hädaolukordade käsiraamat. London Life Science Communications, 2002.
8. Laine L. ja Peterson W. L. Verejooks peptiline haavand. N. Ingl. J. Med. 331:717, 1999.
9. Lin H. J. et al. Endoskoopiline süstimine peptilise haavandi hemorraagia peatamiseks: tulevase, randomiseeritud, võrdleva uuringu lõpptulemused. seedetrakt. Endosc. 39:15, 1998.
10. Mueller X. et al. Tegurid, mis soodustavad edasist hemorraagiat ja suremust pärast peptilise haavandi verejooksu. J. Am. Coll. Surg. 179:457, 1999.
11. Sugawa C. ja Joseph A. L. Veritsevate kaksteistsõrmiksoole ja maohaavandite endoskoopiline sekkumine. Surg. Clin. North Am. 72:317, 1999.
12. Rolhauser C., Fleischer D.E. Haavandi verejooksu endoskoopilise ravi praegune seis. Baillier's Clin Gastroenterol. 2000, 3, 391-41.
Ägeda verejooksu iatrogeenne etioloogia on kõige tavalisem endoskoopilise polüektoomia ja papilotserntetrotoomia kontekstis. Kuigi endoskoopiline polüektoomia on korralikult märgistatud ja teostatud, on see ohutu, kuid see on kindlasti koormatud vähemate tüsistustega kui kirurgiline polüpektoomia, tuleb arvestada, et järgnev verejooks esineb kuni 5% polüpektoomia puhul. Ohtlik – eriti hiline verejooks, mis tekib 7 päeva jooksul pärast treeningut. Kõige riskantsemad on eakad patsiendid, kellel on suured polüübid ja koagulopaatia, nii esmane kui indutseeritud.
See teave on mõeldud tervishoiu- ja farmaatsiatöötajatele. Patsiendid ei tohiks seda teavet kasutada meditsiinilise nõuande või soovitusena.
Verejooks seedetrakti ülaosast
prof. A. A. Sheptulin
Seedetrakti ülaosa (GIT) verejooks moodustab ligikaudu 80–70% kõigist seedetrakti verejooksu juhtudest. Verejooksu kliinilise tähtsuse määravad ka kõrged suremusnäitajad, mis on viimastel aastatel püsinud stabiilselt 5-10% tasemel.
Tõsine veritsus pärast papillomagnetoomiat on veelgi harvem, kuid sageli on patsient otseselt eluohtlik ning pärast endoskoopilist hemostaasi on sageli vajalik operatsioon, sealhulgas sapijuhade drenaaž plastist stendi sisestamise teel. Väga harv verejooksu põhjus võib olla aordi-tsentraalne fistul.
Haiglaravi faas algab oluliste elutähtsate näitajate stabiliseerimisega, millele järgneb enamikul juhtudel endoskoopiline uuring veritsevate kahjustustega, millele järgneb intensiivne teraapia veritsevale patsiendile, mida täiendatakse tõhusa farmakoloogilise raviga.
Etioloogia
Seedetrakti ülaosa verejooksu peamised põhjused ja nende suhteline esinemissagedus on toodud tabelis 1.
Enamik ühine põhjus verejooksud seedetrakti ülaosast mao ja kaksteistsõrmiksoole erosiivsed ja haavandilised kahjustused. Nende verejooksude riskitegurid on patsientide vanus (üle 65 aasta), samuti mittesteroidsete põletikuvastaste ravimite kasutamine. Näiteks andmete vastuvõtmine ravimid kombinatsioonis anamneesis peptilise haavandiga suurendab seedetrakti ülaosa verejooksu riski võrreldes üldpopulatsiooniga 17 korda.
Esimene samm on hemodünaamilise stabiilsuse, elutähtsate näitajate ja venoosse juurdepääsu hindamine. Vahetult pärast võtmist on vaja kindlaks teha verejooksu raskusaste ja verekaotuse suurus. Ortostaatiline süstoolse langus vererõhk 20 mm Hg juures. Ja posturaalse pulsatsiooni sageduse tõus 20 lööki minutis näitab umbes 20% veremahu kaotust. Kui patsiendil ilmnevad šokist tingitud vereringe ebastabiilsuse nähud, tuleb koheselt lisada ringlevat vedelikku ja vajadusel manustada vasoaktiivseid aineid.
Eraldi rühm veritseb söögitoru ja mao veenilaiendid. Reeglina täheldatakse neid maksatsirroosiga patsientidel, kuid need võivad esineda ka muude haiguste korral, millega kaasneb portaalhüpertensiooni sündroom (eriti portaal- või põrnaveenide tromboos). Nende areng on hõlbustatud kõrgsurve portaalveeni süsteemis, veenilaiendite märkimisväärsed suurused, nende erosioon (koos samaaegse refluksösofagiidiga), väljendunud vähenemine funktsionaalne aktiivsus maks, jätkuv alkoholi kuritarvitamine.
Seedetrakti ülaosa verejooksu harvad põhjused võivad olla mao ja soolte veresoonte angiodüsplaasia (Weber-Osler Randu haigus) aordi aneurüsmi rebend (tavaliselt kaksteistsõrmiksoole luumenis) tuberkuloos Ja mao süüfilis, hüpertroofiline polüadenomatoosne gastriit (Menetrieri haigus) mao võõrkehad, pankrease kasvajad (virsungorraagia), sapiteede vigastus või maksa vaskulaarsete moodustiste rebend (hemobiilia), vere hüübimishäired (näiteks fulminantse maksapuudulikkuse, ägeda leukeemiaga trombotsütopeeniliste seisundite korral) jne.
Peamine kliinilised tunnused verejooks seedetrakti ülaosast (otsesed sümptomid) on oksendamine verega (hematemees) ja must tõrvajas väljaheide (melena) (tabel 2).
Vere oksendamist täheldatakse tavaliselt märkimisväärse verekaotusega (üle 500 ml) ja reeglina kaasneb sellega alati melena. Söögitoru arteriaalset verejooksu iseloomustab oksendamine muutumatu vere seguga. Söögitoru veenilaiendite verejooks on sageli rikkalik ja väljendub oksendamises tumeda kirsivärvi verega. Maoverejooksu korral näeb hemoglobiini ja vesinikkloriidhappe koostoime ja hematiinkloriidi moodustumise tagajärjel oksendamine välja nagu kohvipaks. Tõsi, raske hüpokloorhüdria korral, samuti juhtudel, kui maoverejooks on tugev, säilitab okse muutumatu vere segu.
Melena kaasneb sageli verega oksendamisega, kuid seda võib täheldada ka ilma selleta. Melena on iseloomulik kaksteistsõrmiksoole verejooksule, kuid seda leitakse sageli kõrgema asukohaga verejooksuallikatega, eriti kui see toimub piisavalt aeglaselt. Enamasti tuvastatakse melena mitte varem kui 8 tundi pärast verejooksu algust ja selle tekkeks võib piisata juba 5080 ml verekaotusest. Väiksema verejooksu, aga ka soole sisu läbimise aeglustumise korral muutub väljaheide mustaks, kuid jääb vormituks.
Väljaheite tumeda värvuse ilmnemisel tuleb meeles pidada pseudomeleena tekkevõimalust, mida täheldatakse raua, vismuti, aktiivsöe preparaatide võtmisel, samuti mustikate ja mustade sõstarde söömisel.
Sisu kiirendatud (vähem kui 8 tunni) läbimisel soolestikku ja verekaotusega üle 100 ml võib seedetrakti ülaosa verejooks ilmneda punakaspunase vere vabanemises väljaheitega. (hematoheesia), mida peetakse iseloomulikumaks seedetrakti alumise osa verejooksule. Umbes 5% peptilise haavandiga patsientidest võib hematoheesia olla ainsaks peptilise haavandi verejooksu kliiniliseks sümptomiks.
TO üldised sümptomid Seedetrakti ülaosa verejooksu (kaudsed nähud) hulka kuuluvad üldine nõrkus, pearinglus, müra tunnetus kõrvades ja tumenemine silmades, õhupuudus, südamepekslemine. Mõnel juhul võivad kaudsed seedetrakti verejooksu sümptomid eelneda melena esinemisele ja verega oksendamisele või tulla kliinilises pildis esile. Kui punakaspunase vere vabanemine väljaheitega on tingitud verejooksust seedetrakti alumisest osast, siis kaudsed sümptomid (südamepekslemine, pearinglus, üldine nõrkus jne) tekivad pärast hematoheesiat ja ei eelne selle ilmnemisele.
Raskusastme skoor
Seedetrakti verejooksu raskusastet selle arengu esimestel tundidel saab hinnata vererõhu languse aste, tahhükardia raskusaste, ringleva vere mahu puudulikkus (BCC). Tuleb meeles pidada, et hemodilutsioonist tingitud hemoglobiinisisalduse langust hakatakse tuvastama alles paar tundi pärast verejooksu algust. BCC puudujäägi hindamisel aitab määratlus šoki indeks(SHI) Algoveri meetodi järgi (defineeritud kui pulsisageduse jagamise jagatis süstoolse rõhu väärtusega) (tabel 3).
Sõltuvalt verekaotuse mahust ja BCC puudulikkuse suurusest eristatakse seedetrakti ägeda verejooksu 3 raskusastet (tabel 4).
Diagnoos ja diferentsiaaldiagnostika
Seedetrakti ülaosa verejooksu diagnoosimisel ja põhjuse väljaselgitamisel aitab põhjalik haiguslugu, näiteks peptilise haavandi tuvastamine minevikus, mittesteroidsete ravimite võtmine. ravimid või antikoagulandid, alkoholi kuritarvitamine (Mallory-Weissi sündroomiga), maksatsirroosile (astsiit, palmaarne erüteem, hepato- ja splenomegaalia, günekomastia) või muude haiguste (Weber-Osler Randu sündroomi korral telangiektaasia nahal ja limaskestadel) tunnuste tuvastamine ).
Seedetrakti verejooksu kahtlusega patsientide uurimisel viiakse läbi laboratoorsete parameetrite (hemoglobiini tase, hematokrit, erütrotsüütide ja trombotsüütide arv, protrombiini tase, fibrinogeen, veritsusaeg jne) dünaamilist jälgimist, on vaja kindlaks teha veretüüp Ja rh tegur, läbi viia komplekssed instrumentaalsed uuringud, mille eesmärk on tuvastada verejooksu allikas.
Kui patsiendil on vere ja melena oksendamine, tuleb kõigepealt teha esophagogastroduodenoskoopia, mis peaks olema võimalikult kiire, kuna patsiendi prognoos sõltub sageli verejooksu allika tuvastamise õigeaegsusest. Nasogastraalsondi esialgne sisestamine kinnitab vere olemasolu maosisus. Tuleb meeles pidada, et vere puudumine maoloputuses ei välista seedetrakti verejooksu võimalust (näiteks kui verejooksu allikas paikneb kaksteistsõrmiksoole distaalsetes osades).
Endoskoopiline uuring võimaldab 70% juhtudest kontrollida seedetrakti ülaosa verejooksu allikat. Sõltuvalt endoskoopilisest pildist peptilise haavandiga patsientidel, aktiivne Ja jätkuv seedetrakti verejooks (Tabel 5). Aktiivne veritsus võib omakorda avalduda endoskoopiliselt arteriaalse jugaverejooksuna (nn Forrest Ia tüüp), aeglase vere vabanemisega verejooksuna (Forrest Ib tüüp), verejooksuna koos aeglase vere vabanemisega kõrvalasuvast trombist. Tekkinud verejooksu iseloomustab endoskoopiliselt trombi või pindmiselt paiknevate verehüüvete tuvastamine haavandi põhjas koos mitteveritseva veresoone nähtava alaga (Forrest II tüüp). Mõnel juhul (tüüp Forrest III) avastati endoskoopilisel uurimisel erosioon- ja haavandiline kahjustus ilma verejooksu tunnusteta (joonis 15).
Endoskoopilised muutused võimaldavad hinnata verejooksu varajase kordumise riski (tabel 6).
Kui verejooksu allikat ei ole endoskoopia käigus võimalik tuvastada, angiograafia Ja stsintigraafia, võime tuvastada näiteks angiodüsplaasia esinemist.
Seedetrakti ülaosast ägeda verejooksuga patsientide ravi üldpõhimõtted soovitavad patsiendi viivitamatut hospitaliseerimist kirurgiaosakonda, BCC võimalikult kiiret taastumist intravenoosse kateetri paigaldamisega ja sellele järgnevat massiivset infusioonravi, hemostaatilise ravi, värskete ravimite kasutamist. külmutatud plasma ja trombotsüütide mass vere hüübimishäirete esinemisel.
Üldised põhimõtted
patsientide konservatiivne ravi
koos verejooksuga seedetrakti ülaosast
l Erakorraline haiglaravi
l BCC taastamine
l Hemostaatiline ravi
l Vereülekanded
Vereannuste arvutamine (igaüks 500 ml)
valemi järgi: n = 10-x,
kus x on algne sisu
hemoglobiin grammides
l Ravimid
H2 blokaatorid
prootonpumba inhibiitorid
traneksaamhape
sekretiin
somatostatiin
Vereülekannet tehakse šoki tekkimisel, samuti kui hemoglobiini tase langeb alla 100 g / l. Kui on šokipilt, lisatakse veel 4 annust verd ja kui verejooks taastub pärast selle esialgset peatumist, lisatakse veel 2 annust.
Kasutusefektiivsus H2 blokaatorid Ja prootonpump Seedetrakti verejooksu ravis hinnatakse praegu ebajärjekindlalt. Kuid arvestades nende ravimite võimet tõsta maosisese pH taset, võib nende kasutamist haavandilise verejooksu korral pidada õigustatuks. Ranitidiini manustatakse tilguti või joaga 50 mg (famotidiini annuses 20 mg) iga 68 tunni järel, omeprasooli intravenoosselt annuses 40 mg ööpäevas.
Seedetrakti ülaosa verejooksu ravis on võimalik kasutada ka traneksaamhape(intravenoosselt annuses 1015 mg 1 kg kehamassi kohta) antifibrinolüütilise toimega ravim, mis pärsib plasminogeeni seondumist ja aktiveerib plasmiini muundumist fibriiniks.
Erosiivse ja haavandilise verejooksu (nt Forrest Ib) ravimisel annab hea efekti sekretiin või somatostatiin. Secretini manustatakse intravenoosselt isotoonilises naatriumkloriidi lahuses või 5% fruktoosilahuses annuses 800 RÜ (ehk 12 RÜ 1 kg kehakaalu kohta) päevas ja see aitab 8095% juhtudest verejooksu peatada. Somatostatiini manustatakse pideva infusioonina annuses 250 mcg/h. Sekretiini ja somatostatiini kasutamise kestus peab olema vähemalt 48 tundi.
Aktiivse haavandilise verejooksu (juga või aeglane verejooks) nähtude avastamine endoskoopilisel uurimisel on näidustus kasutamiseks Endoskoopilised meetodid verejooksu peatamiseks, mis sellistel juhtudel vähendab tõhusalt uuesti verejooksu riski, suremust ja erakorraliste kirurgiliste sekkumiste sagedust.
Kõige sagedamini kasutatavad on erinevad termoreaktiivsed meetodid endoskoopiline hemorraagia kontroll, mis põhineb asjaolul, et kõrge temperatuuri toime põhjustab koevalkude koagulatsiooni, veresoone valendiku kokkusurumist ja verevoolu vähenemist. Sellised meetodid hõlmavad laserravi, multipolaarset elektrokoagulatsiooni, termokoagulatsiooni. Hemostaatilisel eesmärgil süstitakse erinevate haavandite piirkonda skleroseeriv Ja vasokonstriktorid (adrenaliini, polidokanooli, etanooli jne lahused). Praegu peetakse veritsevate haavandite endoskoopilise ravi valikmeetodiks elektrokoagulatsiooni, termokoagulatsiooni, süste-skleroteraapiat, samuti termokoagulatsiooni ja süste-skleroteraapia kombineeritud kasutamist.
Juhtudel, kui endoskoopilised meetodid haavandi verejooksu peatamiseks on ebaefektiivsed (verejooks jätkub või hemodünaamiliste parameetrite ja hemoglobiinitaseme stabiliseerimiseks on vaja rohkem kui 6 doosi verd päevas), kasutavad nad kirurgiline ravi. Tavaliselt kasutatakse kaksteistsõrmiksoole haavandite korral selektiivne proksimaalne vagotoomia (SPV) veritseva veresoone õmblemisega, maohaavanditega Billrothi maovähendusoperatsioon või haavandi ekstsisioon kombinatsioonis SPV-ga. alternatiivne traditsioonilised viisid kirurgiline ravi on laparoskoopiline kirurgia, millega kaasneb madalam suremus ja lühemad taastusravi perioodid operatsioonijärgsel perioodil.
Suure operatsiooniriski korral saab kasutada angiograafilised ravimeetodid, kaasa arvatud vasopressiini infusioon Ja emboliseerimine. Vasopressiini intraarteriaalne infusioon põhjustab vasokonstriktsiooni ja peatab haavandi verejooksu 50% juhtudest. Emboliseerivad materjalid (nt imenduv želatiinkäsn) süstitakse kateetri kaudu veritsevasse arterisse.
Verejooksuga patsientide ravi
söögitoru veenilaienditest
Hepaatilise entsefalopaatia sümptomite ilmnemise või süvenemise vältimiseks piirata valgusisaldust dieedis kuni 40 g päevas, määrake laktuloos sees (1020 ml päevas) ja klistiiri kujul (2 korda päevas), neomütsiin (1,0 g 4 korda päevas sees).
Kasutatakse verejooksu peatamiseks vasokonstriktorid (vasopressiin, terlipressiin, somatostatiin, oktreotiid). Vasopressiini manustatakse esmalt intravenoosselt (20 minuti jooksul) annuses 20 RÜ 100 ml 5% glükoosilahuse kohta, seejärel lülituvad nad üle ravimi aeglasele infusioonile, manustades seda 424 tunni jooksul kiirusega 20 RÜ 1 kohta. tund, kuni verejooks täielikult peatub. Vasopressiini kombinatsioon glütserüültrinitraadiga võib vähendada vasopressiini süsteemsete kõrvaltoimete raskust. Triglütsüülvasopressiini manustatakse algul boolussüstina annuses 2 mg ja seejärel intravenoosselt 1 mg iga 6 tunni järel.
Söögitoru veenilaiendite väikese verejooksu ja stabiilsete hemodünaamiliste parameetrite korral on soovitatav läbi viia endoskoopiline skleroteraapia. Sklerosantide (polidokanool või etoksüsklerool) paravasaalne või intravasaalne manustamine aitab verejooksu peatada enam kui 70% patsientidest.
Massiivse verejooksu korral, kui skleroseeriv ravi on halva nähtavuse tõttu võimatu, kasutavad nad seda õhupalli tamponaad söögitoru veenilaiendid, kasutades Sengstaken-Blakemore sondi või (koos veenilaiendite lokaliseerimisega mao põhjas) Linton Nachlassi sondi. Sond paigaldatakse perioodiks, mis ei ületa 1224 tundi. Hea toime saavutatakse enamikul patsientidel, kuid mõnel patsiendil võib pärast sondi eemaldamist verejooks taastuda.
Suutmatus peatada verejooksu söögitoru veenilaienditest, selle kiire kordumine pärast esialgset hemostaasi, samuti vajadus kasutada suurtes annustes konserveeritud verd (üle 6 annuse 24 tunni jooksul) on näidustused kirurgiline ravi. Childe'i järgi A- ja B-klassi maksatsirroosi korral kasutatakse sagedamini möödaviiguoperatsiooni, C-klassi tsirroosi korral söögitoru transsektsiooni.
Suremus veenilaiendite verejooksudesse sõltub suuresti maksa funktsionaalsest seisundist ja ulatub Childe C-klassi tsirroosi korral 50%-ni.
Ärahoidmine
Seedetrakti ülaosa verejooksu ennetamine hõlmab selliste haiguste õigeaegset avastamist ja ravi, mis võivad olla seedetrakti verejooksuga komplitseeritud. Jah, käes haavandivastane ravi vähendab peptilise haavandi kordumise tõenäosust ja vähendab vastavalt haavandi verejooksu sagedust.
Mao limaskestale negatiivset mõju avaldavate ravimite (eriti mittesteroidsed põletikuvastased ravimid, antikoagulandid) määramisel tuleb rangelt arvesse võtta näidustusi. Misoprostooli profülaktiline kasutamine H2 blokaatorid või prootonpumba inhibiitorid vähendab ravimitest põhjustatud mao- ja kaksteistsõrmiksoole limaskesta kahjustuste tekkeriski. Stressihaavandite ohu korral (näiteks ulatuslike põletuste, neurokirurgiliste operatsioonide korral) on soovitatav kasutada antatsiidid .
Söögitoru veenilaiendite verejooksu vältimine on vähendatud kuni õigeaegne bypass operatsioon (eriti transjugulaarne intrahepaatiline portosüsteemne šunteerimine) või skleroteraapia, verejooksu riski vähendamine. Ennetava eesmärgiga on näidatud ka väikeste annuste b-blokaatorite või nitraatide kasutamine, mis vähendavad rõhku portaalisüsteemis.
Kirjandus
1. Ivaškin V.T. Mittesteroidsete põletikuvastaste ravimite kasutamisest põhjustatud gastropaatia patogenees. Ros. ajakiri gastroenterool. hepatool. 1994; 1:1114.
2. Kitsenko E.A. Taktika ja ravimteraapia portaalhüpertensiooniga patsiendid. Ros. ajakiri gastroenerool. hepatool. 1997; 5:1418.
3. Jensen DM. Uued arengud raskekujulise seedetrakti ülaosa verejooksu diagnoosimises ja ravis Aktuaalsed teemad gastroenteroloogias ja hepatoloogias (Ed. G.N.J. Tytgat, M. van Blankenstein). Stuttgart-New York, 1990; 422.
4. Levine JS, Klor H.-U., Oehler G. Gastroenteroloogiline diferentsiaaldiagnostika. Stuttgart New York, 1995.
5. Swain CP. Seedetrakti ülaosa hemorraagia Hiljutised edusammud gastroenteroloogias (Ed. R.E. Pounder). Edinbugh London Madrid Melbourne New York Tokyo, 1992; 9:13550.
6Wagner P.K. gastroduodenaalne verejooks. Sümptomid ja tunnused, diagnoos, ravi. Hoechsti meditsiini värskendus. Frankfurt Maini ääres, 1988.
7 Walt R.P. Seedetrakti ülaosa verejooks Hiljutised edusammud gastroenteroloogias (Ed.R.E. Pounder). Edinburgh London Melbourne New York, 1990; 8:10116.
Kontrollülesanded
(õigeid vastuseid võib olla rohkem kui üks)
1. Millised järgmistest teguritest aitavad kaasa mao erosiivsetest ja haavandilistest kahjustustest tingitud verejooksu tekkele?
A. Kõrge vesinikkloriidhappe sekretsioon.
B. Eakas vanus haige.
B. Mittesteroidsete põletikuvastaste ravimite võtmine.
D. Kaasuva refluksösofagiidi esinemine.
D. Duodenogastrilise sapi refluksi esinemine.
Õiged vastused: B, V. Seedetrakti verejooksu tekkerisk suureneb eakatel oluliselt, eriti mittesteroidsete põletikuvastaste ravimite võtmisel.
2. Millised järgmistest teguritest soodustavad verejooksu tekkimist söögitoru veenilaienditest?
A. Portaalhüpertensiooni kõrge aste.
B. Veenilaiendite märkimisväärne suurus.
B. Kaasuva refluksösofagiidi esinemine.
D. B- või C-hepatiidi viiruse replikatsiooni markerite olemasolu.
D. Kaasuva maksa gastropaatia esinemine.
Õiged vastused: A B C. Verejooksu tekkimist söögitoru veenilaienditest soodustab kõrge portaalhüpertensioon, suured suurused veenilaiendid, nende erosioon (koos samaaegse refluksösofagiidiga), maksa funktsionaalse aktiivsuse järsk langus, jätkuv alkoholi kuritarvitamine.
3. Millised tegurid määravad oksendamise värvuse seedetrakti verejooksu korral?
A. Verejooksu allika lokaliseerimisest.
B. Verejooksu kiirusest.
B. Teatud ravimite võtmisest.
G. Seedetrakti motoorika seisundist.
D. Vesinikkloriidhappe sekretsiooni tasemest.
Õige vastus: A, B, D. Oksendamise värvuse seedetrakti verejooksu ajal määrab verejooksu allika asukoht (söögitoru, magu), selle arengu kiirus, vesinikkloriidhappe sekretsiooni tase (rohke verejooksu, samuti raske hüpokloorhüdria, hemoglobiini korral vesinikkloriidhappega seondumist ja hematiinvesinikkloriidi moodustumist, mis annab oksendamismassile kohvipaksu värvi, ei teki).
4. Millistel juhtudel on haavandilise verejooksu korral soovitav teha endoskoopilist hemostaasi?
A. Aktiivse verejooksuga haavandist.
B. Aktiivse aeglase verejooksuga haavandist.
B. Kui haavandi põhjas leitakse nähtav veresoon.
G. Kui haavandi põhjas leitakse tromb.
D. Kõigil ülaltoodud juhtudel.
Õige vastus: A B C. Aktiivse (juga või aeglase) haavandiverejooksu tunnuste tuvastamine endoskoopia ajal, samuti nähtav veresoon haavandi põhjas, näitab kõrge riskiga verejooksu kordumine ja on näidustus endoskoopilise hemostaasi tekkeks. Haavandi põhjas oleva trombi esinemise korral on korduva verejooksu oht väike, mistõttu endoskoopilist hemostaasi sellises olukorras ei tehta.
statRiis. 3. Tromb haavandi põhjas (tüüp Forrest II).
Riis. 4. Veresoone nähtav osa haavandis (II tüüpi Forrest).
Riis. 5. Maohaavand ilma värske verejooksu tunnusteta (Forrest III tüüp).