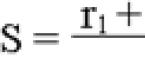МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
Лекарственные формы для ОФС.1.4.1.0007.15
парентерального применения Взамен ст. ГФ XI «Инъекционные лекарственные формы»
Требования настоящей общей фармакопейной статьи не распространяются на иммунобиологические лекарственные препараты, препараты крови человека и радиофармацевтические препараты, предназначенные для парентерального применения.
Растворы для инъекций гомеопатические должны дополнительно выдерживать требования ОФС «Растворы для инъекций гомеопатические».
Лекарственные формы для парентерального применения представляют собой стерильные лекарственные формы, предназначенные для введения в организм человека путем инъекций, инфузий или имплантации (с нарушением целостности кожных покровов или слизистых оболочек, минуя желудочно-кишечный тракт).
К лекарственным формам для парентерального применения относятся:
- инъекционные и инфузионные лекарственные формы (раствор для инъекций, эмульсия для инъекций, суспензия для инъекций, раствор для инфузий, эмульсия для инфузий);
- концентраты для приготовления инъекционных и инфузионных лекарственных форм;
- твердые лекарственные формы, предназначенные для приготовления инъекционных и инфузионных лекарственных форм (порошок; лиофилизат, в том числе «лиофилизированный порошок»);
- лекарственные формы для имплантации (имплантат, таблетка для имплантации и т.д.).
Раствор для инъекций (в том числе «гель для инъекций») –водный или неводный раствор лекарственного вещества/веществ в соответствующем растворителе, предназначенный для инъекционного введения.
Эмульсия для инъекций – эмульсия типа «масло в воде» или «вода в масле», предназначенная для инъекционного введения.
Суспензия для инъекций – суспензия, предназначенная для инъекционного введения.
В зависимости от способа введения инъекционные лекарственные формы подразделяются на подкожные, внутримышечные, внутривенные, внутрисуставные, внутриcердечные, внутриполостные, субконъюктивальные и др.
Раствор для инфузий – водный раствор для внутрисосудистого введения объёмом 100 мл и более.
Эмульсия для инфузий – эмульсия для внутрисосудистого введения типа «масло в воде» объёмом 100 мл и более.
Концентрат для приготовления инъекционных или инфузионных лекарственных форм – жидкая лекарственная форма, из которой путем разведения соответствующим растворителем получают инъекционную или инфузионную лекарственную форму.
Порошок для приготовления инъекционных или инфузионных лекарственных форм – твёрдая дозированная лекарственная форма с добавлением или без вспомогательных веществ, обладающая свойством сыпучести, предназначенная для приготовления раствора или суспензии для парентерального применения.
Лиофилизат (в т.ч. «лиофилизированный порошок») для приготовления инъекционных или инфузионных лекарственных форм – твёрдая дозированная лекарственная форма, полученная методом лиофилизации, предназначенная для приготовления раствора или суспензии для парентерального применения.
Лекарственные формы для имплантации – лекарственные формы, предназначенные для имплантации и высвобождающие лекарственное вещество (вещества) в течение определенного (длительного) периода времени.
ОСОБЕННОСТИ ТЕХНОЛОГИИ
Лекарственные формы для парентерального применения подвергают стерилизации в соответствии с требованиями и указаниями фармакопейных статей.
Растворители
Вода, используемая при производстве лекарственных форм для парентерального применения, должна соответствовать требованиям ФС «Вода для инъекций».
В качестве водных растворителей, кроме воды для инъекций, можно использовать изотонический раствор натрия хлорида, раствор Рингера, раствор глюкозы 5 % и др., неводных – жирные растительные масла или другие органические растворители.
Если не указано иначе в фармакопейной статье, растительные масла, предназначенные для приготовления лекарственных форм для парентерального применения, должны соответствовать следующим требованиям: быть прозрачными при температуре 10 °С, без запаха или почти без запаха и не иметь запаха прогорклости. Кислотное число должно быть не более 0,56, число омыления должно быть от 185 до 200, йодное число от 79 до 141. Могут использоваться также жидкие синтетические моно- и диглицериды жирных кислот, которые должны быть прозрачны при охлаждении до 10 °С и иметь йодное число не превышающее 140.
В составе комплексных растворителей могут быть использованы спирт этиловый, глицерин, пропиленгликоль, макрогол 400, бензилбензоат, бензиловый спирт и другие.
Растворители, используемые для получения лекарственных форм для парентерального применения, должны отвечать требованиям фармакопейных статей по показателям «Бактериальные эндотоксины» или «Пирогенность».
Вспомогательные вещества
В состав лекарственных форм для парентерального применения могут быть добавлены антимикробные консерванты, стабилизаторы, эмульгаторы, солюбилизаторы и другие вспомогательные вещества, указанные в фармакопейных статьях.
В качестве вспомогательных веществ, повышающих стабильность действующих веществ, используют аскорбиновую, хлористоводородную, винную, лимонную, уксусную кислоты, натрия карбонат и гидрокарбонат, натрия гидроксид, калия или натрия сульфит, натрия гидросульфит или метабисульфит, натрия тиосульфат, динатрия эдетат, натрия цитрат, натрия фосфат одно- или двузамещенные, антимикробные консерванты — метилпарагидроксибензоат и пропилпарагидроксибензоат, хлорбутанол, крезол, фенол и другие.
Количество используемых вспомогательных веществ, если нет других указаний в фармакопейной статье, не должно превышать следующих концентраций: для веществ, содержащих ртуть и катионные поверхностно-активные вещества – 0,01 %; для веществ, подобных хлорбутанолу, крезолу и фенолу – 0,5 %; для сернистого ангидрида или эквивалентных количеств сульфита, бисульфита и метабисульфита калия или натрия – 0,2 %.
В многодозовые лекарственные формы для парентерального применения консерванты добавляют независимо от способа стерилизации, за исключением тех случаев, когда само лекарственное вещество обладает антимикробной активностью.
Лекарственные формы для парентерального применения при разовой дозе, превышающей 15 мл, за исключением специальных случаев, а также лекарственные формы для внутриполостных, внутрисердечных, внутриглазных инъекций или инъекций, имеющих доступ к спинномозговой жидкости, не должны содержать антимикробных консервантов.
Инфузионные лекарственные формы обычно должны быть изотоничны по отношению к крови человека и не должны содержать антимикробных консервантов.
испытания
Все лекарственные формы для парентерального применения должны выдерживать испытание на стерильность в соответствии с требованиями .
Лекарственные формы для парентерального применения, а также фармацевтические субстанции, используемые для их приготовления, подвергают испытанию на бактериальные эндотоксины или пирогены. Испытание проводят в соответствии с требованиями или .
Для лекарственных форм для парентерального применения, приготовленных из сырья природного происхождения, для инъекционных и инфузионных лекарственных форм в упаковках из полимерных материалов и в других случаях, если это указано в фармакопейной статье, проводят испытание на аномальную токсичность в соответствии с требованиями .
Лекарственные формы для парентерального применения, предназначенные для внутрисосудистого введения и полученные из фармацевтических субстанций, которые могут обладать депрессорным действием (субстанции микробиологического или животного происхождения), подвергаются испытаниям на гистамин и/или депрессорное действие в соответствии с и «Испытание на депрессорные вещества».
В жидких лекарственных формах для парентерального применения контролируют показатель «рН» в соответствии с требованиями .
В лекарственных формах для парентерального применения, содержащих антимикробные консерванты и антиоксиданты, необходимо проводить определение их подлинности и количественное определение с обязательным указанием верхнего и нижнего пределов содержания.
Лекарственные формы для парентерального применения должны выдерживать испытания по показателю «Механические включения», контролируемые в соответствии с требованиями ОФС «Видимые механические включения» и .
ИНЪЕКЦИОННЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ
Растворы для инъекций (в том числе «гели для инъекций» ) дополнительно проверяют по показателям: «Прозрачность», «Цветность».
Растворы для инъекций должны быть прозрачными (). Цветность растворов для инъекций определяют путем сравнения с эталонами в соответствии с или в соответствии с указаниями фармакопейных статей.
Вязкие растворы для инъекций и растворы ВМС (в том числе «гели для инъекций») дополнительно контролируют по показателю «Вязкость».
Масляные растворы для инъекций дополнительно контролируют по показателю «Плотность».
Эмульсии для инъекций не должны обнаруживать признаков фазового расслоения, должны представлять собой эмульсии типа «масло в воде» и соответствовать требованиям . Кроме того, эмульсии для внутрисосудистого введения дополнительно контролируют по показателю «Размер частиц». Если не указано иначе в фармакопейной статье, размер частиц не должен превышать 5 мкм.
Суспензии для инъекций должны отвечать требованиям .
Суспензии для инъекций дополнительно контролируют по показателям «Размер частиц», «Проходимость через иглу», «Седиментационная устойчивость».
ИНФУЗИОННЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ
Инфузионные лекарственные формы должны отвечать требованиям, предъявляемым к растворам или эмульсиям для инъекций.
На этикетках инфузионных лекарственных препаратов приводят значение теоретической осмолярности. В случае, если теоретическая осмолярность не может быть рассчитана, указывают среднее значение осмоляльности в соответствии с .
Если не указано иначе в фармакопейной статье, для инфузионных лекарственных форм проводят испытание на наличие бактериальных эндотоксинов в соответствии с требованиями .
Концентраты для приготовления инъекционных или инфузионных лекарственных форм
Концентраты перед применением разводят до указанного объема соответствующим стерильным растворителем. После разведения полученный раствор должен соответствовать требованиям, предъявляемым к инъекционным или инфузионным лекарственным формам.
Испытания по показателям «Прозрачность», «Цветность» и «рН» для концентратов проводят на разведенном растворе в том растворителе и в той концентрации, которые указаны в инструкции по применению, если нет других указаний в фармакопейной статье.
ПОРОШКИ и лиофилизаты для ПРИГОТОВЛЕНИЯ инъекционных и ли ИНФУЗИонных лекарственных форм
Для приготовления инъекционных или инфузионных лекарственных форм содержимое упаковки с лекарственным препаратом растворяют или диспергируют в подходящем стерильном растворителе непосредственно перед введением. Полученные растворы или суспензии должны соответствовать всем требованиям, предъявляемым к растворам для инъекций или суспензиям для инъекций.
Испытания по показателям «Прозрачность», «Цветность», «рН» и «Механические включения» проводят с использованием раствора, полученного при растворении лекарственной формы в том растворителе и в той концентрации, которые указаны в инструкции по применению, если нет других указаний в фармакопейной статье.
При использовании в производстве порошков или лиофилизатов органических растворителей необходимо контролировать их остаточное содержание в соответствии с .
Порошки и лиофилизаты для приготовления инъекционных или инфузионных лекарственных форм должны отвечать требованиям .
Имплантаты
Имплантаты контролируют на соответствие требованиям и . Кроме того, необходимо определять размер имплантатов и проводить испытание на высвобождение действующего вещества (веществ).
При наличии испытания на однородность дозирования испытание на однородность массы является не обязательным.
Упаковка
В соответствии с требованиями . Лекарственные формы для парентерального применения выпускают во флаконах, ампулах, шприцах, картриджах или полимерной упаковке. Упаковки должны быть изготовлены из достаточно прозрачных материалов, позволяющих проводить визуальный контроль содержимого, за исключением упаковки для имплантатов и других случаев, описанных в фармакопейных статьях.
Марка стекла и укупорочных средств должны быть указаны в фармакопейной статье. Материалы, которые используются при производстве упаковок и укупорочных средств, не должны обладать токсическим действием.
Упаковка и укупорочные средства должны обеспечивать герметичность лекарственных форм для парентерального применения, быть химически и физически индифферентными по отношению к лекарственному средству, сохранять его терапевтическую активность, качество и чистоту в процессе приготовления, хранения, транспортирования, реализации и использования.
Пластиковые материалы или эластомеры, используемые при производстве укупорочных средств, должны быть достаточно плотными и эластичными, чтобы при прохождении иглы сохранялась целостность пробки и обеспечивалась герметичность упаковки после удаления иглы.
Лекарственные формы для парентерального применения могут выпускаться в однодозовых упаковках (ампулы, картриджи или заполненные шприцы) или в многодозовых, содержащих несколько доз действующего вещества.
Объем лекарственной формы для парентерального применения в однодозовой упаковке должен быть достаточным для однократного введения, но не должен превышать 1 л. Лекарственные формы для парентерального применения, предназначенные для орошения, гемофильтрации, диализа или парентерального питания, освобождаются от указанного ограничения по объему.
Лекарственные формы для парентерального применения, предназначенные для внутриполостных, внутрисердечных, внутриглазных инъекций или инъекций, имеющих доступ к спинномозговой жидкости, должны выпускаться только в однодозовых упаковках.
Имплантаты и таблетки для имплантации упаковывают в индивидуальные стерильные упаковки.
Маркировка
В соответствии с требованиями . На упаковке лекарственных форм для парентерального применения указывают название действующих веществ и их количества, перечень названий всех вспомогательных веществ, для инфузионных растворов – дополнительно количества вспомогательных веществ. При использовании антимикробных консервантов для всех лекарственных форм для парентерального применения указывают концентрацию каждого антимикробного консерванта.
Для инфузионных растворов указывают осмолярность, при указании в фармакопейной статье — дополнительно ионный состав в ммоль/л.
Если к порошку, порошку лиофилизированному или лиофилизату, предназначенному для приготовления инъекционных или инфузионных лекарственных форм прилагается упаковка с растворителем, на этикетке упаковки должен быть указан состав растворителя.
На упаковке концентратов для приготовления инъекционных или инфузионных лекарственных форм дополнительно должно быть указано, что раствор разводят перед использованием в соответствии с инструкцией по применению.
ХРАНЕНИЕ
В соответствии с требованиями и . В стерильной упаковке, обеспечивающей стабильность лекарственной формы для парентерального применения в течение указанного срока годности, в защищенном от света месте при температуре от 8 до 15 °С, если нет других указаний в фармакопейной статье.
В соответствии с указаниями ГФХ, в качестве растворителей для приготовления инъекционных растворов применяют воду для инъекций, персиковое и миндальное масла. Вода для инъекций должна отвечать требованиям статьи № 74 ГФХ. Персиковое и миндальное масла должны быть стерильными, а их кислотное число не превышать 2,5.
Инъекционные растворы должны быть прозрачными. Проверку производят при просмотре в свете рефлекторной лампы и обязательном встряхивании сосуда с раствором. Испытание растворов для инъекций на отсутствие механических загрязнений осуществляют согласно специальной инструкции, утвержденной Министерством здравоохранения СССР.
Инъекционные растворы готовят массо-объемным способом: лекарственное вещество берут по массе (весу), растворитель - до требуемого объема.
Количественное определение лекарственных веществ в растворах производят согласно указаниям в соответствующих статьях. Допустимое отклонение содержания лекарственного вещества в растворе не должно превышать ±5% от указанного на этикетке, если в соответствующей статье нет другого указания.
Исходные лекарственные препараты должны удовлетворять требования ГФХ. Кальция хлорид, кофеин-бензоат натрия, гексаметилентетрамин, натрия цитрат, а также магния сульфат, глюкоза, кальция глюконат и некоторые другие должны употребляться в виде сорта «для инъекций», обладающего повышенной степенью чистоты.
Во избежание загрязнения пылью, а вместе с ней и микрофлорой препараты, употребляемые для приготовления инъекционных растворов и асептических лекарств", хранят в отдельном шкафу в небольших банках, закрытых притертыми стеклянными пробками, защищенными от пыли стеклянными колпачками. При наполнении этих сосудов новыми порциями препаратов банка, пробка, колпачок должны каждый раз подвергать тщательному мытью и стерилизации.
В связи с весьма ответственным способом применения и большой опасностью ошибок, которые могут быть допущены во время работы, приготовление инъекционных растворов нуждается в строгой регламентации и неукоснительном соблюдении технологии.
Не допускается одновременное приготовление нескольких инъекционных лекарств, содержащих различные ингредиенты или одинаковые ингредиенты, но в различных концентрациях, а также одновременное приготовление инъекционного и какого-либо другого лекарства.
На рабочем месте при изготовлении инъекционных лекарств не должно находиться никаких штангласов с лекарственными препаратами, не имеющими отношения к приготовляемому лекарству.
В аптечных условиях особое значение приобретает чистота посуды для приготовления инъекционных лекарств. Для мойки посуды применяют разведенный в воде в виде взвеси 1:20 порошок горчицы, а также свежеприготовленный раствор перекиси водорода 0,5-1% с добавлением 0,5-1% моющих средств («Новость», «Прогресс», «Сульфанол» и другие синтетические моющие средства) или смесь 0,8-1% раствора моющего средства «Сульфанол» и тринатрийфосфата в соотношении 1:9.
Посуду вначале замачивают в моющем растворе, нагретом до 50-60 °С, в течение 20-30 мин, а сильно загрязненную - до 2 ч и более, после чего тщательно моют и ополаскивают сначала несколько (4-5) раз водопроводной водой, а затем 2-3 раза дистиллированной водой. После этого посуду стерилизиуют в соответствии с указаниями ГФХ (статья «Стерилизация»).
Ядовитые вещества, необходимые для приготовления инъекционных лекарств, взвешиваются рецептаром-контролером в присутствии ассистента и немедленно используются последним для приготовления лекарства. Получая ядовитое вещество, ассистент обязан убедиться в соответствии наименования штан-гласа назначению в рецепте, а также в правильности набора гирь и взвешивания.
На все без исключения инъекционные лекарства, приготовленные ассистентом, последний обязан немедленно составить контрольный паспорт (талон) с точным указанием названий взятых ингредиентов лекарства, их количеств и личной подписью.
Все инъекционные лекарства до стерилизации должны подвергаться химическому контролю на подлинность, а при наличии химика-аналитика в аптеке - и количественному анализу. Растворы новокаина, атропина сульфата, кальция хлорида, глюкозы и изотонический раствор натрия хлорида при любых обстоятельствах в обязательном порядке подлежат качественному (идентификация) и количественному анализу.
Во всех случаях инъекционные лекарства должны приготавливаться в условиях максимально ограниченного загрязнения лекарства микрофлорой (асептические условия). Соблюдение этого условия обязательно для всех инъекционных лекарств, в том числе проходящих заключительную стерилизацию.
Правильная организация работы по приготовлению инъекционных лекарств предполагает заблаговременное обеспечение ассистентов достаточным набором простерилизованной посуды, вспомогательных материалов, растворителей, мазевых основ и т. п.
№ 131. Rp.: Sol. Calcii chloridi 10% 50,0 Sterilisetur! DS. Внутривенная инъекция
Для приготовления инъекционного раствора необходима простерилизованная посуда: отпускная склянка с пробкой, мерная колба, воронка с фильтром, часовое стекло или кусок стерильного пергамента в качестве крыши для воронки. Для приготовления раствора кальция хлорида для инъекций необходима также стерилизованная градуированная пипетка с грушей для отмеривания концентрированного раствора кальция хлорида (50%). Перед приготовлением раствора многократно промывают стерильной водой фильтр; фильтрованной водой промывают и ополаскивают отпускную склянку и пробку.
Отмеривают (или отвешивают) необходимое количество лекарственного вещества, смывают его в мерную колбу, добавляют небольшое количество стерильной воды, доводя затем объем раствора до метки. Приготовленный раствор фильтруют в отпускную склянку. Сосуд с раствором и воронку во время фильтрования закрывают часовым стеклом или стерильным пергаментом. Осматривают раствор на отсутствие механических примесей.
После укупорки склянки с инъекционным раствором плотно обвязывают пробку влажным пергаментом, надписывают на обвязке состав и концентрацию раствора, ставят личную подпись и стерилизуют раствор при 120 °С в течение 20 мин.
№ 132. Rp.: Sol. Glucosi 25% 200,0 Sterilisetur! DS.
Для стабилизации указанного раствора используют заранее приготовленный раствор стабилизатора Вейбеля (см. с. 300), которого добавляют к инъекционному раствору в количестве 5% независимо от концентрации глюкозы. Стабилизированный раствор глюкозы стерилизуют текущим паром в течение 60 мин.
При изготовлении инъекционных растворов глюкозы следует учитывать, что последняя содержит 1 молекулу кристаллизационной воды, поэтому глюкозы следует взять соответственно больше, используя следующее уравнение ГФХ:
где а - прописанное в рецепте количество препарата; б - содержание влаги в глюкозе, имеющейся в аптеке; х - требуемое количество глюкозы, имеющейся в аптеке.
Если анализ на влажность показывает содержание влаги в порошке глюкозы, равное 9,6%, то препарата следует взять:
![]()
а на 200 мл раствора - 55 г.
№ 133. Rp.: Sol. Cofieini-natrii benzoatis 10% 50,0 Sterilisetur! DS. По 1 мл под кожу 2 раза в день
В рецепте № 133 приведен пример раствора вещества, являющегося солью сильного основания и слабой кислоты. По указанию ГФХ (статья № 174), руководствуясь прописью для ампу-лированного раствора кофеин-бензоата натрия, используют в качестве стабилизатора 0,1 н. раствор едкого натра из расчета 4 мл на 1 л раствора. В данном случае добавляют 0,2 мл раствора едкого натра (рН 6,8-8,0). Раствор стерилизуют текучим паром в течение 30 мин.
№ 134. Rp.: 01. Camphorati 20% 100,0 Sterilisetur! DS. По 2 мл под кожу
Рецепт № 134 - пример инъекционного раствора, в котором в качестве растворителя использовано масло. Камфору растворяют в большей части теплого (40-45 °С) стерилизованного персикового (абрикосового или миндального) масла. Полученный раствор фильтруют через сухой фильтр в сухую мерную колбу и доводят маслом до метки, промывая им фильтр. Далее содержимое переводят в стерильную склянку с притертой пробкой.
Стерилизацию раствора камфоры в масле осуществляют текучим паром в течение 1 ч.
Физиологические растворы. Физиологическими называются растворы, которые по составу растворённых веществ способны поддерживать жизнедеятельность клеток, переживающих органов и тканей, не вызывая существенных сдвигов физиологического равновесия в биологических системах. По своим физико-химическим свойствам физиологические растворы и примыкающие к ним кровезамещающие жидкости весьма близки к плазме человеческой крови. Физиологические растворы обязательно должны быть изотоничными, содержать хлориды калия, натрия, кальция и магния в соотношениях и количествах, характерных для кровяной сыворотки. Очень важна их способность сохранять постоянство концентрации водородных ионов на уровне, близком к рН крови (~7,4), что достигается введением в их состав буферов.
Большинство физиологических растворов и кровезамещающих жидкостей для обеспечения лучшего питания клеток и создания необходимого окислительно-восстановительного потенциала обычно содержат глюкозу, а также некоторые высокомолекулярные соединения.
Наиболее распространенными физиологическими растворами являются жидкость Петрова, раствор Тироде, раствор Рингера - Локка и ряд других. Иногда физиологическим условно называют 0,85% раствор натрия хлорида, применяющийся в виде вливаний под кожу, в вену, в клизмах при кровопотерях, интоксикациях, при шоке и т. д., а также для растворения ряда медикаментов при инъекционном введении.
Изготовление инъекционных растворов в аптеках регламентируется рядом НД: ГФ, приказами МЗ РФ № 309, 214, 308, Методическими указаниями по изготовлению стерильных растворов в аптеках, угвержденных МЗ РФ от 24.08.94 г.
Лекарственные формы для инъекций могут изготовлять только те аптеки, которые имеют асептический блок и возможности для создания асептики.
Не разрешается готовить инъекционные лекарственные формы, если нет методик количественного анализа, данных о совместимости ингредиентов, режиме стерилизации и технологии.
Стадии технологического процесса
Подготовительная.
Изготовление раствора.
Фильтрование.
Фасовка раствора.
Стерилизация.
Стандартизация.
Оформление к отпуску.
На подготовительной стадии проводятся работы по созданию условий асептики: подготовка помещения, персонала, оборудования, вспомогательных материалов, тары и упаковочных средств.
НИИ Фармации разработаны методические указания (МУ) № 99/144 «Обработка посуды и укупорочных средств, используемых в технологии стерильных растворов, изготовленных в аптеках» (М., 1999 г.). Эти МУ являются дополнением к действующей Инструкции по санитарному режиму аптек (пр. МЗ РФ № 309 от 21.10.97).
К посуде относятся бутылки стеклянные для крови, трансфузионных и инфузионных препаратов и флаконы из дрота для лекарственных веществ. К укупорочным средствам относятся резиновые и полиэтиленовые пробки, алюминиевые колпачки.
На подготовительной стадии осуществляется также подготовка лекарственных веществ, растворителей и стабилизаторов. Для получения воды очищенной используют аквадистилляторы.
Проводятся также расчеты. В отличие от других лекарственных форм для всех инъекционных растворов регламентированы состав, способы обеспечения стабильности и стерильности. Эти сведения имеются в приказе МЗ РФ № 214 от 16.09.97, а также в Методических указаниях по изготовлению стерильных растворов в аптеках, утвержденных МЗ РФ от 24.08.94.
Изготовление растворов для инъекций. На этой стадии проводят отвешивание порошкообразных веществ, отмеривание жидкостей и химический анализ раствора.
В соответствии с приказом МЗ РФ № 308 от 21.10.97. «Об утверждении инструкции по изготовлению в аптеках жидких лекарственных форм» инъекционные растворы готовят массо-объемным методом в мерной посуде или объем растворителя определяют расчетным путем. При необходимости добавляют стабилизатор. После изготовления проводят идентификацию, определяют количественное содержание лекарственного вещества, рН, изотошфуюшие и стабилизирующие вещества. При удовлетворительном результате анализа раствор фильтруют.
Стадия фильтрования и розлива. Для фильтрования растворов используют разрешенные к применению фильтрующие материалы.
Фильтрование больших объемов растворов проводят на фильтровальных установках стационарного или карусельного типа.
Примеры установок
Аппарат стационарного типа с 4 воздушными камерами (см. учебник. т.1, стр.397). Фильтрование происходит через стеклянные фильтры с обмоткой из фильтрующего материала, помещенные в 3-5 литровые бутыли с фильтруемым раствором. Профильтрованный раствор собирают во флаконы, которые установлены на подъемных столиках.
Фильтр « Грибок » - простейшая установка для фильтрованш небольших объемов инъекционных растворов. Работает под вакуумом.
Состоит из бачка с фильтруемым раствором, воронки, сборника профильтрованного раствора, ресивера и вакуумного насоса.
Воронка закрывается слоями фильтрующего материала из ваты марли и опускается в бак с фильтруемым раствором. При создании вакуума системе раствор фильтруется и поступает в приемник. Ресивер предназначен для предотвращения переброса жидкости в вакуумную линию.
Фасовка. Для фасовки инъекционных растворов используют стерильные флаконы из нейтрального стекла НС-1,НС-2. Для укупорки флаконов
применяют пробки из специальных сортов резины: силиконовые (ИР-21), из нейтрального каучука (25П), бутилового каучука (ИР-119, 52-369).
После фасовки проводят первичный контроль каждого флакона на отсутствие механических включений визуальным методом. Если обнаруживаются механические включения, раствор перефильтровывают.
После контроля на чистоту флаконы, укупоренные резиновыми пробками, обкатывают металлическими колпачками. Для этого используют приспособление для обжима крышек и колпачков (ПОК) и более совершенный полуавтомат ЗП-1 для закатки колпачков.
После укупорки флаконы маркируют с помощью жетона или штамповкой на колпачке названия раствора и его концентрации.
Стерилизация. Для стерилизации водных растворов используют чаще всего термический метод, а именно стерилизацию насыщенным паром под давлением. Стерилизацию проводят в паровых стерилизаторах вертикальных (марки ВК-15, ВК-3) и горизонтальных (ГК-100, ГП-280, ГП-400, ГПД-280 и др.). ВК - вертикальный круговой; ГП - горизонтальный прямоугольный односторонний; ГПД - горизонтальный прямоугольный двусторонний.) Устройство парового стерилизатора и принцип работы (см. учебник).
В отдельных случаях растворы стерилизуют текучим паром при температуре 100°С, когда этот метод является единственно возможным для данного раствора. Текучий пар убивает только вегетативные формы микроорганизмов.
Растворы термолабильных веществ (апоморфина гидрохлорида, викасола, барбитала натрия) стерилизуют фильтрованием.
Для этого используют глубинные или, предпочтительно, мембранные фильтры.
Мембранные фильтры вставляют в фильтродержатели. Держатели бывают двух типов: пластинчатые и патронные. В пластинчатых держателях фильтр имеет форму круглой или прямоугольной пластины, в патронных -форму трубки. Перед фильтрованием стерилизуют фильтр в держателе и емкость для сбора фильтрата паром под давлением или воздушным методом. Метод фильтрования перспективен для аптечных условий.
Стерилизация растворов должна производиться не позднее 3-х часов после изготовления раствора, под контролем провизора. Повторная стерилизация не допускается.
После стерилизации проводят вторичный контроль на отсутствие механических включений, качество укупорки флаконов и полный химический контроль, т.е. проверяют рН, подлинность и количественное содержание действующих веществ. Стабилизаторы после стерилизации проверяют только в случаях, предусмотренных НД. Для контроля после стерилизации отбирается один флакон от каждой серии.
Стадия стандартизации. Стандартизация проводится после стерилизации по показателям: отсутствие механических включений,
прозрачность, цветность, значение рН, подлинность и количественное содержание действующих веществ. Инъекционные лекарственные формы и вода для инъекций периодически проверяются органами Госсанэпиднадзора на стерильность и апирогенность.
Растворы для инъекций считаются забракованными, если они не соответствуют нормам хотя бы по одному из показателей, а именно: физико-химические свойства, содержание видимых механических включений, стерильность, апирогенность, а также при нарушении герметичности укупорки и недостаточном объеме заполнения флакона.
Оформление к отпуску. На флакон наклеивают этикетку белого цвета с синей полосой с обязательным указанием наименования раствора, его концентрации, даты изготовления, условий и срока хранения. Сроки хранения инъекционных лекарственных форм регламентированы приказом МЗ РФ № 214 от 16.07.97.
Направления совершенствования технологии растворов для инъекций, изготавливаемых в аптечных условиях
Механизация технологического процесса, т.е. использование современных материалов и средств малой механизации (дистилляторов, сборников воды для инъекций, мешалок, аппаратов для фильтрования, стерилизаторов и др.).
Расширение ассортимента стабилизаторов.
Внедрение физико-химических методов контроля качества растворов.
Создание современных средств упаковки и укупорки.
8. Изготовление растворов для инъекций в промышленных условиях Особенности заводского производства:
Большой объем;
Высокая степень механизации и автоматизации;
Возможность изготовления дозированных лекарственных форм;
Возможность получения лекарственных препаратов с большим сроком годности.
Производство инъекционных лекарственных форм стало возможным при появлении трех условий: изобретении шприца, организации асептических условий работы и использования ампулы как вместилища определенной дозы стерильного раствора. Первоначально ампулированные препараты выпускались в аптеках в малом количестве. Затем их выпуск был перенесен в условия крупных фармацевтических производств. В Перми ампулированные препараты выпускает НПО «Биомед». Наряду с ампулами препараты для инъекции заводского производства выпускаются во флаконах, в прозрачных упаковках из полимерных материатов и шприц-тюбиках разового применения. Однако ампулы являются самой распространенной упаковкой для инъекционных растворов.
Ампулы
Ампулы представляют собой стеклянные сосуды различной формы и вместимости, состоящие из расширенной части - корпуса и капилляра. Наиболее распространенными являются ампулы вместимостью от 1 до 10 мл. Наиболее удобны ампулы с пережимом, который препятствует попаданию раствора в капилляр при запайке и облегчает вскрытие ампулы перед инъекцией.
В РФ выпускают ампулы разных типов:
ампулы вакуумного наполнения (обозначаются В или ВП-вакуумные с пережимом);
ампулы шприцевого наполнения (обозначаются Ш или ШП-шприцевого наполнения с пережимом).
Наряду с этими обозначениями указывают вместимость ампул, марку стекла и номер стандарта.
Ампульное стекло
Стекло для ампул используют разных марок:
НС-3 - нейтральное стекло для изготовления ампул и флаконов для растворов веществ, подвергающихся гидролизу, окислению и др. реакциям (например, солей алкалоидов);
НС-1 - нейтральное стекло для ампулирования растворов более устойчивых лекарственных веществ (например, натрия хлорида);
СНС-1 - нейтральное светозащитное стекло для ампулирования растворов светочувствительных веществ;
АБ-1 - щелочное стекло для ампул и флаконов для масляных растворов лекарственных веществ (например, раствора камфоры).
Медицинское стекло - это твердый раствор, полученный в результате охлаждения расплава смеси силикатов, оксидов металлов и солей. Оксиды металлов и солей используются как добавки к силикатам для придания стеклу необходимых свойств (температуры плавления, химической и термической устойчивости и др.) Наибольшую температуру плавления имеет кварцевое стекло (до 1800°С), которое состоит на 95-98% из оксида кремния. Это стекло термически и химически устойчивое, но очень тугоплавкое. Чтобы понизить температуру плавления в состав такого стекла добавляют оксиды натрия и калия. Однако эти оксиды снижают химическую стойкость стекла. Повышают химическую стойкость введением оксидов бора и алюминия. Добавление оксидов магния увеличивает термическую устойчивость. Чтобы повысить механическую прочность и уменьшить хрупкость стекла, регулируют содержание оксидов бора, алюминия и магния.
Таким образом, изменяя состав компонентов и их концентрацию, можно получить стекло с заданными свойствами.
К стеклу для ампул предъявляются следующие требования:
Прозрачность - для контроля за отсутствием механических включений в
растворе;
бесцветность - для обнаружения изменения цвета раствора в процессе стерилизации и хранения;
легкоплавкость - для запайки ампул с раствором при относительно невысокой температуре;
термическая устойчивость - чтобы ампулы выдерживали тепловую стерилизацию и перепад температур;
химическая устойчивость - чтобы не разрушались лекарственные вещества и другие компоненты раствора в ампуле;
механическая прочность - чтобы ампулы выдерживали механические нагрузки в процессе производства, транспортировки и хранения;
достаточная хрупкость - для легкого вскрытия капилляра ампулы.
Стадии технологического процесса производства растворов для инъекций в ампулах
Процесс изготовления сложен и условно делится на два потока: основной и параллельный основному. Стадии и операции основного потока производства:
первая стадия: изготовление ампул
операции:
калибровка стеклодрота;
мойка и сушка стеклодрота;
изготовление ампул;
вторая стадия: подготовка ампул к наполнению
операции:
сушка и стерилизация;
оценка качества ампул;
резка капилляров ампул;
третья стадия: стадия ампулирование
операции:
наполнение ампул раствором;
запайка ампул;
стерилизация;
контроль качества после стерилизации;
маркировка,
упаковка готовой продукции;
регенерация забракованных ампул.
Стадии и операции параллельного потока производства:
первая стадия: подготовка растворителей
операции: подготовка растворителей (например, для масляных
растворов); получение воды для инъекций;
вторая стадия: подготовка раствора к наполнению операции: изготовление раствора;
фильтрование раствора;
контроль качества (до стерилизации).
Для обеспечения высокого качества готовой продукции создаются специальные условия выполнения стадий и операций технологического процесса. Особое внимание при этом уделяется технологической гигиене. Требования к технологической гигиене и пути их реализации изложены в ОСТ 42-510-98 «Правила организации производства и контроля качества лекарственных средств» (GMP).
Стадии и операции основного потока:
Калибровка дрота
Дрот - это стеклянные трубки определенной длины (1,5 метра). Выпускается на стекольных заводах из медицинского стекла. К дроту предъявляются жесткие требования: отсутствие механических включений, пузырьков воздуха и других дефектов, одинаковый диаметр по всей длине, определенная толщина стенок, отмываемость загрязнений и др. Дрот калибруют, т.е. сортируют по наружному диаметру от 8 до 27мм. Это очень важно, чтобы ампулы одной серии имели одинаковую вместимость. Поэтому стеклянные трубки калибруют на специальной установке по наружному диаметру в двух сечениях на определенном расстоянии от середины трубки.
Мойка и сушка дрота
После калибровки дрот поступает на мойку. В основном, дрот приходится отмывать от стеклянной пыли, которая образуется при его изготовлении. От основной массы загрязнений легче отмыть именно дрот, а не готовые ампулы. Дрот моют либо в установках камерного типа, в которых одновременно и сушат трубки, либо в горизонтальных ваннах с помощью ультразвука.
Положительные стороны камерного способа мойки:
высокая производительность;
возможность автоматизации процесса;
совмещение операций мойки и сушки. Недостатки:
большой расход воды;
Невысокая эффективность мойки за счет небольшой скорости потока воды.
Увеличение эффективности мойки достигается за счет барботажа, создания турбулентных потоков и струйной подачи воды.
Более эффективным по сравнению с камерным является ультразвуковой способ.
В жидкости при прохождении ультразвука (УЗ) образуются чередующиеся зоны сжатия и разряжения. В момент разряжения возникают разрывы, которые называются кавитационными полостями. При сжатии полости захлопываются, в них возникает давление, около нескольких тысяч атмосфер. Поскольку частицы загрязнений являются зародышами кавитационных полостей, то при их сжатии загрязнения отрываются от поверхности трубок и удаляются.
Контактно - ультразвуковой способ более эффективен по сравнению с УЗ
Способом, т.к. к специфическому действию УЗ добавляются еще механическая вибрация. В установках контактно-УЗ способа мойки трубки контактируют с вибрирующей поверхностью магнитно-стрикционных излучателей, расположенных на дне ванны с водой. При этом колебания поверхности излучателей передаются стеклянным трубкам, что способствует отделению загрязнений от их внутренних поверхностей.
Качество мойки дрота проверяют визуально. Отмытый и высушенный дрот передается на изготовление ампул.
Изготовление ампул
Ампулы изготовляют на роторных стеклоформующих автоматах.
Стеклянная трубка обрабатывается за время одного поворота ротора на одном участке по длине. При этом одновременно обрабатываются от 8 до 24 и более трубок в зависимости от конструкции автомата. В автомате ИО-8, например, на роторе вращаются 16 пар верхних и нижних патронов. Имеются накопительные барабаны, куда загружаются стеклянные трубки. Дрот из накопительного барабана подается к патронам и зажимается «кулачками» верхнего и нижнего патронов. Они синхронно вращаются с помощью шпинделей вокруг своей оси и движутся по копирам. За один поворот ротора трубки проходят 6 позиций:
Из накопительного барабана трубки подаются внутрь верхнего патрона. С помощью ограничительного упора регулируется их длина. Верхний патрон сжимает трубку «кулачком» и она остается на постоянной высоте во всех 6-ти позициях.
К вращающейся трубке подходят горелки с широким пламенем, происходит нагрев до размягчения. В это время нижний патрон, двигаясь по ломаному копиру, поднимается вверх и зажимает нижний конец трубки.
Нижний патрон, двигаясь по копиру, опускается вниз и вытягивает размягченный дрот в капилляр будущей ампулы.
К верхней части капилляра подходит горелка с острым пламенем и отрезает капилляр.
Одновременно с отрезкой капилляра происходит запаивание донышка следующей ампулы.
«Кулачок» нижнего патрона разжимает ампулу, она опускается на наклонный лоток, а трубка с запаянным донышком подходит к 1-ой позиции, и цикл работы автомата повторяется.
У такого способа изготовления ампул есть два основных недостатка:
Образование внутренних напряжений в стекле. В местах наибольших внутренних напряжений могут возникнуть трещины при тепловой стерилизации, поэтому остаточные напряжения убирают путем отжига.
Получение «вакуумных» ампул. Ампулы на 5-ой позиции запаиваются в момент, когда внутри них находится горячий воздух. При охлаждении образуется вакуум. Он нежелателен, так как при вскрытии капилляра такой ампулы стеклянная пыль засасывается внутрь и впоследствии трудно удаляется.
Пути устранения вакуума в ампулах:
Использование приставок к ампулоформующему автомату для резки капилляров ампул. Приставка располагается рядом с «лотком» в позиции 6. Горячая ампула после попадания в лоток тотчас же попадает в приставку к автомату и вскрывается.
Нагревание корпуса ампулы в момент отрезки капилляра. Находящийся в ампуле воздух при нагревании расширяется. Он вырывается из ампулы в месте отпайки, где стекло расплавлено, и образует там отверстие. За счет отверстия ампулы получаются безвакуумными.
Отламывание капилляра ампулы. Это происходит в тот момент, когда в позиции 6 нижний патрон освобождает зажим и под действием тяжести ампулы в месте отпайки вытягивается очень тонкий капилляр. При падении ампулы капилляр отламывается, герметичность внутри ампулы нарушается, и она становится безвакуумной.
Резка капилляров ампул
Как отдельная операция присутствует, если автомат формует безвакуумные ампулы. Резка капилляров необходима, чтобы ампулы получались одинаковой высоты (для точности дозирования), и концы капилляров ампул были ровные и гладкие (для удобства запайки).
Ленточный полуавтомат для резки капилляров ампул имеет ленточный транспортер, по которому ампулы подходят к вращающемуся дисковому ножу. На подходе к ножу ампула начинает вращаться за счет трения о резиновую ленту. Нож делает на ампуле круговой надрез, и капилляр по месту надреза отламывается пружинами. После вскрытия капилляр оплавляется горелкой, и ампулы поступают в бункер для набора в лотки и затем на отжиг.
Отжиг ампул
Остаточные напряжения в ампулах возникают из-за того, что в процессе изготовления ампулы выдерживают значительные перепады температур. Например, стенки ампул нагреваются до температуры 250 °С, а дно и капилляры, которые находятся непосредственно в зоне пламени горелки, до 800 °С. Готовая ампула подается в зону резкого охлаждения до комнатной температуры (25 °С). Таким образом, перепад температур составляет несколько сотен градусов. Кроме того, наружные слои, особенно крупноемких ампул, охлаждаются быстрее внутренних слоев, сокращаясь в объеме, а внутренние, еще не успевшие охладиться, препятствуют этому сокращению. В результате, между наружными и внутренними слоями создаются и сохраняются остаточные напряжения, которые могут служить причинами трещин в ампулах.
Отжиг представляет собой специальную термическую обработку стекла, состоящую из трех стадий:
Нагревание до температуры, близкой к размягчению стекла (например, для стекла НС-1 - 560-580 °С).
Выдержка при этой температуре до исчезновения напряжений (например, для стекла НС-1-7-10 минут).
Охлаждение - двухступенчатое:
сначала медленное до определенной заданной температуры;
затем более быстрое до комнатной температуры.
Отжиг производится в туннельных печах с беспламенными газовыми горелками с инфракрасными излучателями. Печь состоит из корпуса, трех камер (нагрева, выдержки и охлаждения), стола загрузки и стола выгрузки, цепного конвейера и газовых горелок. Ампулы помещают в лотки и подают на стол загрузки. Далее с помощью конвейера они продвигаются через туннель и охлажденными выходят к столу выгрузки.
Весь режим отжига строго регламентирован для каждого сорта стекла и контролируется приборами. Качество отжига проверяют поляризационно-оптическим методом. Используют прибор-полярископ, на экране которого места в стекле, которые имеют внутренние напряжения, окрашиваются в оранжево-желтый цвет. По интенсивности окрашивания можно судить о величине напряжений.
После отжига ампулы набираются в кассеты и поступают на мойку.
Мойка ампул
Мойка ампул - очень ответственная операция, которая наряду с фильтрованием обеспечивает чистоту раствора в ампулах.
Механические загрязнения, которые удаляются в процессе мойки, состоят, в основном (до 80%), из частиц стекла и стеклянной пыли. В процессе мойки удаляются только те частицы, которые удерживаются механически, за счет сил адгезии и адсорбции. Частицы, которые вплавились в стекло или образовали с ним спайки, не удаляются.
Мойка делится на наружную и внутреннюю.
Наружная мойка - это душирование ампул горячей профильтрованной или водопроводной обессоленной водой.
Аппарат для наружной мойки ампул состоит из корпуса, в котором находится промежуточная емкость для моющей жидкости, рабочая емкость, душирующее устройство и система клапанов. Кассета с ампулами во время мойки находится в рабочей емкости, где под давлением струи воды вращается, что способствует лучшему промыванию наружной поверхности ампул.
Внутренняя мойка осуществляется несколькими способами: вакуумным, ультразвуковым, шприцевым и др.
Вакуумный способ имеет разные варианты:
вакуумный;
турбовакуумный;
пароконденсационный;
разные сочетания с другими способами, например, с ультразвуковым.
Вакуумный способ основан на заполнении ампул водой путем создания разности давлений внутри ампулы и снаружи с последующим ее удалением с помощью вакуума. Ампулы в кассете помещают в аппарат капиллярами вниз Капилляры погружают в воду. Создают вакуум в аппарате. Затем подают в аппарат профильтрованный воздух. За счет перепада давления вода входит внутрь ампул и промывает их внутреннюю поверхность. При последующем: создании вакуума вода удаляется из ампул. Так повторяется несколько раз. Этот способ неэффективен, так как невысока производительность мойки. Имеет место низкое качество мойки, поскольку вакуум создается и гасится недостаточно резко и не образуются турбулентные потоки воды.
Турбовакуумный способ гораздо эффективнее по сравнению с вакуумным за счет резкого мгновенного перепада давления и за счет ступенчатого вакуумирования. Мойка осуществляется в турбовакууммоечном аппарате с программой управления по заданным параметрам (величине давления и уровню воды).
Производительность мойки этим способом высокая, но имеет место большой расход воды и наблюдается большой брак мойки. Количество непромытых ампул составляет до 20% от общего количества ампул. Это следствие общего недостатка вакуумного способа мойки - слабого вихревого турбулентного движения воды на входе и особенно на выходе из ампул. Поэтому даже 15-20 кратная вакуумная мойка не обеспечивает полного удаления основного вида загрязнений - стеклянной пыли. Для отрыва частиц стеклянной пыли от стенок ампул необходимо достичь скорости движения воды до 100 м/с. В аппаратах данной конструкции это невозможно. В связи с этим процесс мойки совершенствовался в следующих направлениях:
Мойка ампул
Пароконденсационный способ мойки ампул разработан проф. Ф.А. Коневым в 1972г., который предложил наполнять ампулы не водой, а паром. Схематически три основные позиции пароконденсационного способа
мойки можно изобразить так:
I позиция: вытеснение воздуха из ампул паром при небольшом разряжении в аппарате.
II позиция: подача воды в ампулу. Капилляр опущен в воду. Корпус ампулы охлаждается, а пар конденсируется. За счет конденсации пара в ампуле создается вакуум, и она заполняется горячей)водой (t =80-90 °С).
III позиция: удаление воды из ампул. Горючая вода при создании вакуума в ампуле закипает, и образующийся пар вместе с кипящей водой с большой скоростью выбрасывается из ампулы. В ампуле остается пар, и цикл мойки повторяется. При выходе воды из ампулы иногда создается интенсивное турбулентное движение, это значительно повышает качество мойки.
В промышленных условиях этим способом ампулы моют в аппарате АП- 30 в автоматическом режиме по заданной программе.
Особенностью процесса пароконденсаштонной мойки ампул является вскипание моющей жидкости в ампуле за счет создающегося разрежения и последующее интенсивное вытеснение моющей жидкости образовавшимся внутри ампулы паром.
Достоинства способа:
Высокое качество мойки;
- стерилизация ампул паром;
Горячие ампулы не нуждаются в сушке перед наполнением растворами;
Не требуется использование в производстве вакуумных насосов, которые являются весьма энергоемкими и дорогими.
Термический способ предложен харьковскими учеными Тихомировой В.Я. и Коневым Ф.А. в 1970 г.
Ампулы после промывки вакуумным способом заполняют горячей дистиллированной водой и капиллярами вниз помещают в зону нагрева до t = 300-400 °С. Вода бурно вскипает и удаляется из ампул.
Положительная сторона: быстрота мойки (время одного цикла 5 мин).
Недостатки: относительно низкая скорость удаления воды из ампул и сложность аппаратурного оформления.
Ультразвуковой (УЗ) способ мойки основан на явлении акустической кавитации в жидкости. Акустическая кавитация - это образование разрывов в жидкости, пульсирующих полостей. Она возникает под действием переменных давлений, создаваемых с помощью излучателей УЗ. Пульсирующие кавитационные полости отслаивают частицы или пленки загрязнений с поверхности стекла.
Кроме того, под действием УЗ поля поле разрушаются ампулы, имеющие микротрещины и внутренние дефекты, что позволяет отбраковывать их. Положительным моментом является также бактерицидное действие УЗ. Ультразвуковой способ мойки обычно сочетают с турбовакуумным. Источником ультразвука являются магнитострикционные излучатели. Они крепятся на крышке или дне турбовакууммоечного аппарата. Все операции выполняются автоматически.
Качество мойки значительно выше по сравнению с турбовакуумным способом.
Еще более совершенным является виброультразвуковой способ мойки в турбовакуумном аппарате, где ультразвук сочетается еще с механической вибрацией.
Шприцевой способ мойки. Сущность шприцевого способа мойки заключается в том, что в ампулу, ориентированную капилляром вниз, вводят полую иглу, через которую под давлением подают воду. Турбулентная струя воды из иглы (шприца) омывает внутреннюю поверхность ампулы и удаляется через зазор между шприцем и отверстием капилляра. Очевидно, что интенсивность мойки зависит от скорости поступления и вытекания жидкости из ампулы. Однако, шприцевая игла, введенная в капилляр, уменьшает его сечение и затрудняет удаление жидкости из ампулы. Это первый недостаток. Второй - большое количество шприцев усложняет конструкцию машин и ужесточает требования к форме и размерам ампул. Ампулы должны иметь точные размеры и строго калиброваться по диаметру капилляра. Производительность мойки эти способом невысокая.
В плане сравнения качества мойки ампул разными способами можно судить по следующим данным
Контроль качества мойки ампул проводится просмотром ампул, наполненных профильтрованной дистиллированной водой. Сушка и стерилизация ампул
После мойки ампулы быстро, чтобы предотвратить их загрязнение, передают на сушку или стерилизацию в зависимости от технологии ампулирования. Если ампулы предназначены для заполнения масляными растворами или готовятся впрок, их подвергают сушке при t=120-130 C C в течение 15-20 минут.
Если необходима стерилизация, например, в случае ампулирования растворов нестойких веществ, то ампулы стерилизуют в суховоздушном стерилизаторе при t=180 °C в течение 60 минут. Стерилизатор устанавливают в стене между моечным отделением и отделением наполнения ампул растворами (т.е. помещением класса чистоты А). Таким образом, шкаф открывается с двух сторон в разных помещениях. Начиная с этой операции все производственные помещения сообщаются лишь передаточными окнами и располагаются последовательно по ходу производственного потока.
Стерилизация ампул в суховоздушных стерилизаторах имеет недостатки:
разная температура в разных зонах стерилизационной камеры;
большое количество механических загрязнений в воздухе стерилизационной камеры, которые выделяются нагревательными элементами в виде окалины;
попадание нестерильного воздуха при открывании стерилизатора.
Всех этих недостатков лишены стерилизаторы с ламинарным потоком горячего стерильного воздуха. Воздух в таких стерилизаторах предварительно нагревается в калорифере до температуры стерилизации (180-300 °С), фильтруется через стерилизующие фильтры и поступает в стерилизационную камеру в виде ламинарного потока, т.е. движущегося с одинаковой скоростью параллельными слоями. Во всех точках стерилизационной камеры поддерживается одинаковая температура. Подача воздуха с небольшим избыточным давлением и стерильное фильтрование обеспечивают отсутствие всяких частиц в зоне стерилизации.
Оценка качества ампул
Показатели качества:
Наличие остаточных напряжений в стекле. Определяются поляризационно-оптическим методом;
Химическая устойчивость;
Термическая устойчивость;
- для отдельных видов стекла - светозащитные свойства.
Наполнение ампул растворами
После сушки (и, при необходимости, стерилизации) ампулы направляются на следующую стадию - ампулирования. Она включает операции:
> наполнение растворами;
> запайка ампул;
стерилизация растворов;
бракераж;
маркировка;
упаковка.
Наполнение ампул растворами производится в помещениях класса чистоты А.
С учетом потерь на смачиваемость стекла фактический объем наполнения ампул больше номинального объема. Это необходимо, чтобы обеспечить определенную дозу при наполнении шприца. В ГФ XI издания, вып.2 в общей статье «Инъекционные лекарственные формы» имеется таблица, указывающая номинальный объем и объем наполнения ампул.
Наполнение ампул растворами производится тремя способами; вакуумным, пароконденсационным, шприцевым.
Вакуумный способ наполнения. Способ аналогичен соответствующему способу мойки. Он заключается в том, что ампулы в кассетах помещают в герметичный аппарат, в емкость которого заливают раствор для наполнения. Создают вакуум. При этом воздух из ампул отсасывается. После сброса вакуума раствор заполняет ампулы. Аппараты для наполнения ампул раствором вакуумным способом аналогичны по конструкции вакуум-моечным аппаратам. Они работают в автоматическом режиме.
Аппарат состоит из рабочей емкости, соединенной с вакуумной линией, линией подачи раствора и воздушной линией. Имеются устройства, регулирующие уровень раствора в рабочей емкости и глубину разрежения.
Автоматическое управление процессом наполнения носит характер логических решений, т.е. выполнение какой-то операции возможно лишь тогда, когда в определенный момент будут выполнены запрограммированные условия, например необходимая глубина разрежения.
Основной недостаток вакуумного способа наполнения - невысокая точность дозирования. Происходит это потому, что ампулы разной вместимости заполняются неодинаковой дозой раствора. Поэтому для повышения точности дозирования ампулы, находящиеся в одной кассете, предварительно подбирают по диаметру так, чтобы они были одинакового объема.
Второй недостаток - загрязнение капилляров ампул, которые приходится очищать перед запайкой.
К преимуществам вакуумного способа наполнения относится большая производительность (он в два раза более производителен по сравнению со шприцевым способом) и нетребовательность к размерам и форме капилляров заполняемых ампул.
Шприцевой способ наполнения. Сущность его в том, что ампулы, подлежащие наполнению, в вертикальном или наклонном положении подаются к шприцам, и происходит их наполнение заданным объемом раствора. Если дозируется раствор легкоокисляющегося вещества, то наполнение идет по принципу газовой защиты. Сначала в ампулу через иглу подают инертный или углекислый газ, который вытесняет из ампулы воздух. Затем наливают раствор, вновь подают инертный газ, и ампулы тотчас запаивают.
Преимущества шприцевого способа наполнения:
проведение операций наполнения и запайки в одном автомате;
точность дозирования;
капилляры не загрязняются раствором, что особенно важно для вязких жидкостей.
Недостатки:
малая производительность;
более сложное аппаратурное оформление по сравнению с вакуумным способом;
> жесткие требования к размерам и форме капилляров ампул.
Пароконденсационный способ наполнения заключается в том, что после
мойки пароконденсационным способом ампулы, наполненные паром, опускаются капиллярами вниз в ванночки-дозаторы, содержащие точный объем раствора для одной ампулы Корпус ампулы охлаждается, пар внутри конденсируется, образуется вакуум, и раствор заполняет ампулу.
Способ высокопроизводителен, обеспечивает точность дозирования, но пока еще не внедрен в практику.
После наполнения ампул раствором вакуумным способом в капиллярах остается раствор, что мешает запайке. Его можно удалить двумя способами:
отсасыванием под вакуумом, если ампулы расположить капиллярами вверх в аппарате. Остатки раствора с ампул смываются конденсатом пара или струйками воды апирогенной при душировании;
продавливанием раствора внутрь ампулы стерильным воздухом или инертным газом, что применяется наиболее широко.
Запайка ампул
Следующая операция - запайка ампул. Она очень ответственна, так как некачественная запайка влечет за собой брак продукции. Основные способы запайки:
> оплавление кончиков капилляров;
> оттяжка капилляров.
При запайке оплавлением у непрерывно вращающейся ампулы нагревают кончик капилляра, и стекло само заплавляет отверстие капилляра.
Работа автоматов основана на принципе движения ампул в гнездах вращающегося диска или транспортера, который проходит через газовые горелки. Они нагревают и запаивают капилляры ампул.
Недостатки способа:
наплыв стекла на конце капилляров, трещины и разгерметизащм ампул;
необходимость соблюдения требований к размерам ампул;
необходимость промывки капилляров ампул перед запайкой, В конструкции автомата предусматривается распылительная форсунка для душирования апирогенной водой.
Оттяжка капилляров. При этом способе сначала разогревают капилляр непрерывно вращающейся ампулы, а затем отпаиваемую часть капилляра захватывают специальными щипцами и, оттягивая, отпаивают. В то же время отводят пламя горелки в сторону для пережёга стеклянной нити, образующейся в месте отпайки, и для оплавления запаянной части. Запайка с оттяжкой обеспечивает красивый внешний вид ампулы и высокое качество. Однако при запайке ампул с малым диаметром и тонкими стенками капилляр, при воздействии на него средств оттяжки,либо скручивается, либо разрушается. Этих недостатков лишен способ запайки с оттяжкой капилляра под действием струи сжатого воздуха. При этом отсутствует механический контакт с капилляром, имеется возможность пневмотранспортировки отходов, увеличивается производительность и упрощается конструкция запавчного узла. Этим способом можно качественно запаивать ампулы как большого, так и малого диаметра.
Запайка ампул
В отдельных случаях, когда нельзя использовать термические способы запайки, ампулы укупоривают пластмассой. Для запайки ампул со взрывоопасными веществами используют нагрев с помощью электрического сопротивления.
После запайки все ампулы проходят контроль на качество запайки.
Способы контроля:
вакуумирование - отсасывание раствора из некачественно запаянных ампул;
использование растворов красителей. При погружении ампул в раствор метиленового синего бракуются ампулы, содержимое которых окрашивается;
определение величины остаточного давления в ампуле по цвету свечения газовой среды внутри ампулы под действием высокочастотного электрического поля.
Стерилизация ампулированных растворов
После контроля качества запайки ампулы с раствором передаются на стерилизацию. В основном, используется термический способ стерилизации
насыщенным паром под давлением.
Оборудование: паровой стерилизатор типа АП-7. Стерилизация может
осуществляться в двух режимах:
при избыточном давлении 0,11 мПа и t=120 °C;
при избыточном давлении 0,2 мПа и t=132 °C.
Бракераж
После стерилизации следует бракераж ампулированых растворов по следующим показателям: герметичность, механические включения, стерильность, прозрачность, цветность, количественное содержание действующих веществ.
Контроль на герметичность. Горячие ампулы после стерилизации погружают в холодный раствор метиленового синего. При наличии трещин краситель засасывается внутрь, и ампулы отбраковываются. Контроль гораздо чувствительнее, если эту операцию проделать непосредственно в стерилизаторе, в камеру которого после стерилизации заливают раствор метиленового синего и создают избыточное давление пара.
Контроль на механические включения. Под механическими включениями подразумевают посторонние нерастворимые частицы, кроме пузырьков газа. Согласно РД 42-501-98 «Инструкция по контролю на механические включения инъекционных лекарственных средств» контроль может проводиться тремя методами:
визуальным;
счетно-фотометрическим;
микроскопическим.
Визуальный контроль проводится контролером невооруженным глазом на черном и белом фоне. Допускается механизированная подача ампул, флаконов и др. емкостей в зону контроля. На предприятиях осуществляется трехкратный контроль; первичный - внутрицеховой сплошной (100% ампул), вторичный - внутрицеховой выборочный и выборочный-контролером отдела контроля качества.
Визуальный метод контроля субъективен и не дает количественной оценки механических включений.
Счетно-фотометрический метод осуществляется на приборах, которые работают по принципу светоблокировки и позволяют автоматически определять размер частиц и число частиц соответствующего размера. Например, анализаторы механических примесей фотометрические счетные ФС-151, ФС-151.1 или АОЗ-101.
Микроскопический метод заключается в фильтровании анализируемого раствора через мембрану, которую помещают на предметный столик микроскопа и определяют размер частиц и их количество. Этот метод, кроме того, позволяет выявить природу механических включений, что очень важно, т.к. способствует устранению источников загрязнения. Являясь наиболее объективным, этот метод может быть использован как арбитражный.
Следующий вид контроля - это контроль на стерильность. Проводится микробиологическим методом. Сначала устанавливают на специальных тест-микроорганизмах наличие или отсутствие антимикробного действия лекарственного и вспомогательных веществ. При наличии антимикробного действия используют инактиваторы или мембранное фильтрование для отделения антимикробных веществ. После этого растворы высеивают на питательные среды, инкубируют при соответствующих температурах определенное время и контролируют рост или отсутствие роста микроорганизмов.
После стерилизации и бракеража ампулы маркируют и упаковывают. Забракованные ампулы передают на регенерацию.
Маркировка и упаковка ампул
Маркировка - это нанесение надписи на ампулу с указанием названия раствора, его концентрации и объема (Полуавтомат для маркировки ампул).
Упаковка ампул может быть:
в картонные коробки с гофрированными бумажными гнездами;
в картонные коробки с полимерными ячейками - вкладышами для ампул;
ячейки из полимерной пленки (полихлорвинила), которые сверху закрываются фольгой. Фольга и полимер термосклеиваются.
На упаковку наносится серия и срок годности препарата, а также указывается завод-изготовитель, название препарата, его концентрация, объем, количество ампул, дата изготовления. Есть обозначения: «Стерильно», «Для инъекций». Готовая упаковка вырезается по нужному количеству ампул и попадает в накопитель.
Стадия приготовления раствора для ампулирования
Эта стадия стоит особняком, ее называют еще стадией параллельной основному потоку производства или стадией вне основного потока.
Приготовление растворов производится в помещениях класса чистоты В при соблюдении всех правил асептики. Стадия включает следующие операции: растворение, изотонирование, стабилизация, введение консервантов, стандартизация, фильтрование. Некоторые операции, например, изотонирование, стабилизация, введение консервантов,могут отсутствовать.
Растворение производится в реакторах фарфоровых или эмалированных. Реактор имеет паровую рубашку, которая обогревается глухим паром, если растворение необходимо вести при повышенной температуре. Перемешивание проводят с помощью мешалок или барботированием инертным газом (например, углерода диоксидом или азотом).
Растворы готовят массообъемным способом. Все исходные вещества (лекарственные, а также стабилизаторы, консерванты, изотонирующие добавки) должны удовлетворять требованиям НД. К некоторым лекарственным веществам предъявляются повышенные требования к чистоте, и тогда они используются квалификации «для инъекций». Глюкоза и желатин должны быть апирогенными.
Стабилизация растворов. Обоснование стабилизации гидролизующихся и окисляющихся веществ (см. выше).
При изготовлении растворов гидролизующихся веществ используют химическую защиту - добавление стабилизаторов (щелочей или кислот). На стадии ампулирования используют физические способы защиты: подбирают ампулы из химически стойкого стекла или заменяют стекло на полимер.
При изготовлении растворов легкоокисляющихся веществ используют химические и физические способы стабилизации. К физическим способам относится, например, барботирование инертного газа. К способам химическим - добавление антиоксидантов. Стабилизация растворов легкоокисляющихся веществ производится не только на стадии изготовления растворов, но и на стадии ампулирования.
Принципиальная схема ампулирования инъекционных растворов в среде углекислого газа была предложена еще в 60-е годы харьковскими учеными. Изготовление раствора производится в ректоре при перемешивании углекислым газом. После фильтрования раствор собирается в сборнике, который насыщается углекислым газом. Наполнение ампул раствором производится вакуумным способом. Снятие разрежения в аппарате производится не воздухом, а углекислым газом. Раствор из капилляров ампул удаляется также углекислым газом способом продавливают внутрь ампул. Запайку ампул осуществляют тоже в среде инертного газа. Таким образом, в течение ампулирования происходит газовая защита раствора.
Введение консервантов в раствор для ампулирования. Их добавляют в раствор, когда нельзя гарантировать сохранение его стерильности. В ГФ XI издания приведены следующие консерванты для инъекционных растворов: хлорбутанолгидрат, фенол, крезол, нипагин, нипазол и другие.
Консерванты применяют в многодозовых лекарственных средствах для парентерального применения, иногда - в однодозовых в соответствии с требованиями частных ФС. Не разрешается вводить консерванты в лекарственные средства для внутриполостных, внутрисердечных, внутриглазных или других инъекций, имеющих доступ к спинномозговой жидкости, а также при разовой дозе более 15 мл.
Стандартизация растворов. Перед фильтрованием раствор анализируют в соответствии с требованиями общей статьи ГФ XI издания «Инъекционные лекарственные формы» и соответствующей ФС.
Определяют количественное содержание лекарственных веществ, рН, прозрачность, окраску раствора. При получении положительных результатов анализа раствор фильтруют.
Фильтрование растворов.
Фильтрование проводится с двумя целями:
для удаления механических частиц размером от 50 до 5 мкм (тонкая фильтрация);
для удаления частиц размером от 5 до 0,02 мкм, в том числе микроорганизмов (стерилизация растворов термолабильных веществ).
В промышленных условиях для фильтрования растворов используют установки, основными частями которых являются нутч-фильтры или друк-фильтры, или фильтры, работающие под давлением столба жидкости.
Нутч-фильтры применяются для предварительной очистки, например, отделения осадка или адсорбента (фильтр «Грибок»).
Фильтр ХНИХФИ работает под давлением столба жидкости. Сам фильтр состоит из двух цилиндров. Внутренний цилиндр перфорирован. Он укреплен внутри наружного цилиндра или корпуса. На внутренний цилиндр наматываются жгуты из марли сорта "ровница". Они представляют собой фильтрующий материал. Фильтр является частью установки для фильтрования. Установка, кроме двух фильтров, включает две напорные емкости, бак для фильтруемой жидкости, регулятор постоянного уровня, устройство для визуального контроля и сборник.
фильтруемая жидкость из бака подается в напорную емкость. Затем через регулятор уровня под постоянным давлением она подается на фильтр. Второй фильтр в это время может регенерироваться. Фильтруемая жидкость поступает на наружную поверхность фильтра, проходит через слой ровницы во внутренний цилиндр и по его стенкам выходит через патрубок. Далее она поступает через устройство для контроля в сборник.
Друк-фильтры работают под давлением, создаваемым сжатым стерильным воздухом или инертным газом. В таких фильтрах можно фильтровать по принципу газовой защиты. Фильтрующими материалами являются бельтинг, фильтровальная бумага, ткань ФПП-15-3 (из перхлорвинила), капрон. Для стерильного фильтрования используются мембранные фильтры, которые могут работать под вакуумом или под давлением. После контроля на отсутствие механических включений раствор передается на стадию ампулирования.
Для повышения производительности процесса и повышения качества конечного продукта используется комплексная механизация и автоматизация ампульного производства, создаются автоматические линии. Одна из них, например, автоматизирует стадию ампулирования и выполняет следующие операции: наружную и внутреннюю мойку ампул, сушку ампул, заполнение раствором, продавливание раствора из капилляров, наполнение ампул инертным газом, промывку капилляров ампул и запайку. В линию постоянно подается фильтрованный воздух под небольшим давлением, и, таким образом, исключается попадание загрязнений из окружающего воздуха.
Введение
1. Инъекционные формы, их характеристика
1.1 Преимущества и недостатки инъекционного введения
1.2 Требования к инъекционным лекарственным формам
1.3 Классификация инъекционных растворов
2. Технология инъекционных растворов в условиях аптеки
2.1 Приготовление инъекционных растворов без стабилизаторов
2.2 Приготовление инъекционных растворов со стабилизатором
2.3 Приготовление физиологических растворов в аптечных условиях
Заключение
Список литературы
Введение
В современных условиях производственная аптека - рациональное и экономически выгодное звено в организации лечебного процесса. Основная ее задача - наиболее полное, доступное и своевременное удовлетворение потребностей стационарных больных в лекарственных средствах, дезинфекционных растворах, перевязочных материалах и т.д.
Неотъемлемым элементом полноты и доступности лекарственной помощи является наличие в аптеках, помимо готовых лекарственных средств, экстемпоральных лекарственных форм. В основном это лекарственные средства, которые не производятся фармпредприятиями.
На долю инфузионных растворов приходится 65% всех экстемпорально приготовленных форм: растворы глюкозы, натрия хлорида, калия хлорида разной концентрации, аминокапроновая кислота, натрия гидрокарбонат и т.д.
Удельный вес инъекционных растворов в экстемпоральной рецептуре хозрасчетных аптек составляет около 15%, а в аптеках лечебно-профилактических учреждений достигает 40-50% .
Инъекционные растворы – это лекарства, вводимые в организм при помощи шприца с нарушением целостности кожных и слизистых покровов, являются сравнительно новой лекарственной формой.
Идея введения лекарственных веществ через нарушенный кожный покров возникла в 1785 г., когда врач Фуркруа с помощью специальных лезвий (скарификаторов) делал на коже насечки и в полученные ранки втирал лекарственные вещества.
Впервые подкожное впрыскивание лекарств было осуществлено в начале 1851 г. русским врачом Владикавказского военного госпиталя Лазаревым. В 1852 г. Правацем был предложен шприц современной конструкции. Начиная с этого времени, инъекции стали общепризнанной лекарственной формой.
1. Инъекционные формы, их характеристика
1.1 Преимущества и недостатки инъекционного введения
Необходимо отметить следующие преимущества эстемпорального производства инъекционных лекарственных форм по сравнению с использованием готовых лекарственных форм:
Обеспечение быстрого терапевтического эффекта;
Возможность изготовления лекарства для конкретного больного с учетом веса, возраста, роста и т.д. по индивидуальным прописям;
Возможность точно дозировать лекарственное вещество;
Вводимые лекарственные вещества поступают в кровяное русло, минуя такие защитные барьеры организма, как желудочно-кишечный тракт и печень, способные изменять, а иногда и разрушать лекарственные вещества;
Возможность ввести лекарственные вещества больному, находящемуся в бессознательном состоянии;
Краткость времени между приготовлением и использованием лекарственного средства;
Возможность создания больших запасов стерильных растворов, что облегчает и ускоряет их отпуск из аптек;
Отсутствие необходимости коррекции вкуса, запаха, цвета лекарственной формы;
Более низкая стоимость по сравнению с препаратами промышленного производства.
Но инъекционное введение лекарственных средств, помимо преимуществ имеет и отрицательные стороны:
При введении жидкостей через поврежденный покров кожи в кровь легко могут попасть патогенные микроорганизмы;
Вместе с раствором для инъекций в организм может быть введен воздух, вызывающий эмболию сосудов или расстройство сердечной деятельности;
Даже незначительные количества посторонних примесей могут оказать вредное влияние на организм больного;
Психоэмоциональный аспект, связанный с болезненностью инъекционного пути введения;
Инъекции лекарств могут осуществляться только квалифицированными
специалистами.
1.2 Требования к инъекционным лекарственным формам
К лекарственным формам для инъекций предъявляются следующие требования: стерильность, отсутствие механических примесей, стойкость, апирогенность, к отдельным инъекционным растворам - изотоничность, что указывается в соответствующих статьях или рецептах .
Парентеральное применение препаратов предполагает нарушение кожного покрова, что связано с возможным инфицированием патогенными микроорганизмами и введением механических включений.
Стерильность инъекционных растворов, приготовляемых в условиях аптеки, обеспечивается в результате неукоснительного соблюдения правил асептики, а также стерилизации этих растворов. Стерилизацией, или обеспложиванием, называется полное уничтожение в том или ином объекте жизнеспособной микрофлоры.
Асептические условия производства лекарственных препаратов – это комплекс технологических и гигиенических мероприятий обеспечивающих защиту продукта от попадания в него микроорганизмов на всех этапах технологического процесса.
Асептические условия необходимы при изготовлении термолабильных препаратов, а также малоустойчивых систем – эмульсий, взвесей, коллоидных растворов, то есть препаратов, не подвергаемых стерилизации.
Также не меньшую роль играют соблюдение правил асептики при приготовлении лекарственных препаратов выдерживающих термическую стерилизацию, так как этот метод стерилизации не освобождает продукт от погибших микроорганизмов и их токсинов, что может привести к пирогенной реакции при инъекции такого препарата.
Отсутствие механических примесей . Все инъекционные растворы не должны содержать каких-либо механических примесей и должны быть совершенно прозрачными. В инъекционном растворе могут содержаться частицы пыли, волокна материалов, используемых для фильтрования, любые иные твердые частицы, которые могут попасть в раствор из посуды, в которой он готовится. Главная опасность наличия в инъекционном растворе твердых частиц - возможность закупорки сосудов, которая может вызвать смертельный исход в случае, если закупоренными окажутся сосуды, питающие сердце или продолговатый мозг.
Источниками механических загрязнений могут быть некачественная фильтрация, технологическое оборудование, особенно его трущиеся детали, окружающий воздух, персонал, некачественно подготовленные ампулы.
Из этих источников в продукт могут попасть микроорганизмы, частички металла, ржавчины, стекла, древесные резины, угля, золы, крахмала, талька, волокна, асбеста.
Апирогенность . Апирогенностью называется отсутствие в инъекционных растворах продуктов метаболизма микроорганизмов - так называемых пирогенных веществ, или пирогенов. Свое название пирогены (от лат. руг - жар, огонь) получили за способность вызывать повышение температуры при попадании в организм, возможно иногда падение артериального давления, озноб, рвота, понос.
В производстве инъекционных препаратов от пирогенов освобождаются различными физико-химическими методами – путем пропускания раствора через колонки с активированным углем, целлюлозой, мембранные ультрафильтры.
В соответствии с требованиями
ГФХ инъекционные растворы не должны содержать пирогенных веществ. Для обеспечения
этого требования инъекционные растворы готовят на апирогенной воде для инъекций
(или маслах) с использованием медикаментов и других вспомогательных веществ, не
содержащих пирогенов .
1.3 Классификация инъекционных растворов
Лекарственные средства для парентерального применения классифицируются следующим образом:
Инъекционные лекарственные средства;
Внутривенные инфузионные лекарственные средства;
Концентраты для инъекционных или внутривенных инфузионных лекарственных средств;
Порошки для инъекционных или внутривенных инфузионных лекарственных средств;
Имплантаты.
Инъекционные лекарственные средства - это стерильные растворы, эмульсии или суспензии. Растворы для инъекций должны быть прозрачными и практически свободными от частиц. Эмульсии для инъекций не должны обнаруживать признаков расслоения. Суспензия для инъекций при взбалтывании должна быть достаточно стабильной для того, чтобы обеспечить необходимую дозу при введении.
Внутривенные инфузионные лекарственные средства - это стерильные водные растворы или эмульсии с водой в качестве дисперсионной среды; должны быть свободны от пирогенов и обычно изотоничны крови. Предназначаются для применения в больших дозах, поэтому не должны содержать никаких антимикробных консервантов.
Концентраты для инъекционных или внутривенных инфузионных лекарственных средств – это стерильные растворы, предназначенные для инъекций или инфузий. Концентраты разводят до указанного объема и после разведения полученный раствор должен соответствовать требованиям, предъявляемым к инъекционным лекарственным средствам.
Порошки для инъекционных лекарственных средств представляют собой твердые стерильные вещества, помещенные в контейнер. При встряхивании с указанным объемом соответствующей стерильной жидкости они быстро образуют или прозрачный, свободный от частиц раствор, или однородную суспензию. После растворения они должны соответствовать требованиям, предъявляемым к инъекционным лекарственным средствам .
Имплантаты представляют собой
стерильные твердые лекарственные средства, имеющие подходящие для парентеральной
имплантации размеры и форму, и высвобождающие действующие вещества в течение длительного
периода времени. Они должны быть упакованы в индивидуальные стерильные контейнеры.
2. Технология инъекционных растворов в условиях аптеки
В соответствии с указаниями ГФХ, в качестве растворителей для приготовления инъекционных растворов применяют воду для инъекций, персиковое и миндальное масла. Вода для инъекций должна отвечать требованиям статьи № 74 ГФХ. Персиковое и миндальное масла должны быть стерильными, а их кислотное число не превышать 2,5.
Инъекционные растворы должны быть прозрачными. Проверку производят при просмотре в свете рефлекторной лампы и обязательном встряхивании сосуда с раствором.
Инъекционные растворы готовят массо-объемным способом: лекарственное вещество берут по массе (весу), растворитель - до требуемого объема.
Количественное определение лекарственных веществ в растворах производят согласно указаниям в соответствующих статьях. Допустимое отклонение содержания лекарственного вещества в растворе не должно превышать ±5% от указанного на этикетке, если в соответствующей статье нет другого указания.
Исходные лекарственные препараты должны удовлетворять требования ГФХ. Кальция хлорид, кофеин-бензоат натрия, гексаметилентетрамин, натрия цитрат, а также магния сульфат, глюкоза, кальция глюконат и некоторые другие должны употребляться в виде сорта «для инъекций», обладающего повышенной степенью чистоты.
Во избежание загрязнения пылью, а вместе с ней и микрофлорой препараты, употребляемые для приготовления инъекционных растворов и асептических лекарств, хранят в отдельном шкафу в небольших банках, закрытых притертыми стеклянными пробками, защищенными от пыли стеклянными колпачками. При наполнении этих сосудов новыми порциями препаратов банка, пробка, колпачок должны каждый раз подвергать тщательному мытью и стерилизации.
Не допускается одновременное приготовление нескольких инъекционных лекарств, содержащих различные ингредиенты или одинаковые ингредиенты, но в различных концентрациях, а также одновременное приготовление инъекционного и какого-либо другого лекарства.
На рабочем месте при изготовлении инъекционных лекарств не должно находиться никаких штангласов с лекарственными препаратами, не имеющими отношения к приготовляемому лекарству.
В аптечных условиях особое значение приобретает чистота посуды для приготовления инъекционных лекарств. Для мойки посуды применяют разведенный в воде в виде взвеси 1:20 порошок горчицы, а также свежеприготовленный раствор перекиси водорода 0,5-1% с добавлением 0,5-1% моющих средств («Новость», «Прогресс», «Сульфанол» и другие синтетические моющие средства) или смесь 0,8-1% раствора моющего средства «Сульфанол» и тринатрийфосфата в соотношении 1:9.
Посуду вначале замачивают в моющем растворе, нагретом до 50-60 °С, в течение 20-30 мин, а сильно загрязненную - до 2 ч и более, после чего тщательно моют и ополаскивают сначала несколько (4-5) раз водопроводной водой, а затем 2-3 раза дистиллированной водой. После этого посуду стерилизиуют в соответствии с указаниями ГФХ.
Ядовитые вещества, необходимые для приготовления инъекционных лекарств, взвешиваются рецептаром-контролером в присутствии ассистента и немедленно используются последним для приготовления лекарства. Получая ядовитое вещество, ассистент обязан убедиться в соответствии наименования штангласа назначению в рецепте, а также в правильности набора гирь и взвешивания.
На все без исключения инъекционные лекарства, приготовленные ассистентом, последний обязан немедленно составить контрольный паспорт (талон) с точным указанием названий взятых ингредиентов лекарства, их количеств и личной подписью.
Все инъекционные лекарства до стерилизации должны подвергаться химическому контролю на подлинность, а при наличии химика-аналитика в аптеке - и количественному анализу. Растворы новокаина, атропина сульфата, кальция хлорида, глюкозы и изотонический раствор натрия хлорида при любых обстоятельствах в обязательном порядке подлежат качественному (идентификация) и количественному анализу.
Во всех случаях инъекционные лекарства должны приготавливаться в условиях максимально ограниченного загрязнения лекарства микрофлорой (асептические условия). Соблюдение этого условия обязательно для всех инъекционных лекарств, в том числе проходящих заключительную стерилизацию.
Правильная организация работы
по приготовлению инъекционных лекарств предполагает заблаговременное обеспечение
ассистентов достаточным набором простерилизованной посуды, вспомогательных материалов,
растворителей, мазевых основ и т. п.
2.1 Приготовление инъекционных растворов без стабилизаторов
Приготовление инъекционных растворов без стабилизаторов складывается из следующих последовательных операций:
Расчет количества воды и сухих лекарственных веществ;
Отмеривание необходимого количества воды для инъекций и отвешивание лекарственных веществ;
Растворение;
Подготовка флакона и укупорочных средств;
Фильтрование;
Оценка качества инъекционного раствора;
Стерилизация;
Оформление к отпуску;
Оценка качества.
Rp.: Solutionis 25% 30ml
Da. Signa: по 1мл внутримышечно 3 раза в день
Выписан раствор вещества, хорошо растворимого в воде, для парентерального применения.
Расчеты.
Анальгина 7,5
Воды для инъекций
30 – (7,5х0.68) = 34,56мл
0,68 – коэффициент увеличения объема анальгина
Технология.
Создание асептических условий достигается приготовлением инъекционных лекарственных средств из стерильных медикаментов, в стерильной посуде и в специально оборудованном помещении. Однако асептика не может гарантировать полную стерильность растворов, поэтому они в дальнейшем подвергаются стерилизации.
При расчете количества воды для инъекций необходимо учитывать, что концентрация анальгина превышает 3% и поэтому необходимо учитывать коэффициент увеличения объема.
В асептическом блоке в стерильной подставке в 34,65мл свежеперегнанной воды для инъекций растворяют 7,5г анальгина. Приготовленный раствор фильтруют через двойной стерильный бензольный фильтр с комочком длинноволокнистой ваты. Можно для фильтрации использовать стеклянный фильтр №4. раствор фильтруют в стерильный флакон объемом 50мл из нейтрального стекла.
Укупоривают флакон стерильной резиновой пробкой и обкатывают металлическим колпачком. Проверяют раствор на прозрачность, отсутствие механических включений, цветность. Затем раствор стерилизуют в автоклаве при 120°С 8 минут. После стерилизации и охлаждения раствор передают на контроль повторно.
Флакон прозрачного стекла укупорен герметично резиновой пробкой «под обкатку», наклеивают номер рецепта и этикетки: «Для инъекций», «Стерильно», «Хранить в прохладном и защищенном от света месте», «Беречь от детей».
Дата № рецепта
Injectionibus 43,65
Простерилизовано
Приготовил
Проверил
2.2 Приготовление инъекционных растворов со стабилизатором
При изготовлении инъекционных растворов необходимо принимать меры к обеспечению сохранности лекарственных веществ.
Стабильность - это неизменность свойств содержащихся в растворах лекарственных веществ - достигается подбором оптимальных условий стерилизации, использованием консервантов, применением стабилизаторов, соответствующих природе лекарственных веществ. Несмотря на многообразие и сложность процессов разложения лекарственных веществ, наиболее часто имеют место гидролиз и окисление.
Лекарственные вещества, требующие стабилизации их водных растворов, можно разделить на три группы:
1) соли образованные сильными кислотами и слабыми основаниями;
2) соли, образованные сильными основаниями и слабыми кислотами;
3) легкоокисляющиеся вещества.
Стабилизация растворов солей сильных кислот и слабых оснований (соли алкалоидов и азотистых оснований) осуществляется добавлением кислоты. Водные растворы таких солей вследствие гидролиза имеют слабокислую реакцию. При тепловой стерилизации и хранении таких растворов рН повышается ввиду усиления гидролиза, сопровождающегося уменьшением концентрации водородных ионов. Сдвиг рН раствора приводит к гидролизу солей алкалоидов с образованием мало растворимых оснований, которые могут выпадать в осадок.
Прибавление к растворам солей сильных кислот и слабых оснований свободной кислоты подавляет гидролиз и таким образом обеспечивает стабильность инъекционного раствора. Количество кислоты, необходимое для стабилизации растворов солей, зависит от свойств вещества, а также оптимальной границы рН раствора (обычно рН 3,0-4,0). 0,1 н раствор хлористоводородной кислоты используют для стабилизации растворов дибазола, новокаина, спазмолитика, совкаина, атропина сульфата и др .
Rp.: Solutionis Dibazoli 1% 50ml
Da. Signa: по 2 мл 1 раз в день подкожно
Выписана жидкая лекарственная форма для инъекционного применения, представляющая собой истинный раствор, в состав которого входит вещество группы Б.
Расчеты.
Дибазола 0,5
Раствора кислоты
хлористоводородной 0,1 и
Воды для инъекций до 50 мл
Технология
В рецепте пописан раствор для подкожного введения, в состав которого входит вещество, трудно растворимое в воде. Инъекционные растворы дибазола нуждаются в стабилизации 0,1н хлористоводородной кислоты.
В асептических условиях в стерильной мерной колбе емкостью 50мл в части воды для инъекций растворяют 0,5г дибазол, добавляют 0,5 0,1н раствора хлористоводородной кислоты м доводят водой до метки. приготовленный раствор фильтруют в склянку для отпуска емкостью 50мл из нейтрального стекла через двойной стерильный беззольный фильтр с подложенным комочком длинноволокнистой ваты.
Флакон укупоривают и проверяют раствор на отсутствие механических примесей, для чего склянку переворачивают вверх дном и просматривают в проходящем свете на черно-белом фоне. Если при просмотре обнаруживаются механические частицы, операцию фильтрации повторяют. Затем горловину склянки с пробкой обвязывают стерильной и еще влажной пергаментной бумагой с удлиненным концом 3х6см, на котором ассистент должен сделать запись графитным карандашом о входящих ингредиентах и их количестве, и поставить личную подпись.
Склянку мс приготовленным раствором помещают в бикс и стерилизуют при 120°С 8 минут. После охлаждения раствор передают на контроль.
Дата № рецепта
Solutionis acidi
Hidrychloridi 0,1 № 50ml
Объем 50мл
Простерилизовано
Приготовил
Проверил
Стабилизация солей сильных оснований и слабых кис лот осуществлется добавлением щелочи или натрия гидрокарбоната. Растворы солей, образованных сильными основаниями и кислотами, диссоциируют с образованием слабодиссоциирующей кислоты, что влечет к уменьшению свободных ионов водорода, а, как следствие, к увеличению рН раствора. Для подавления гидролиза подобных растворов солей необходимо добавить щелочь. К числу солей, стабилизируемых едким натрием или натрия гидрокарбонатом, относятся: никотиновая кислота, кофеин-бензоат натрия, натрия тиосульфат, натрия нитрит.
Стабилизация растворов легковоспламеняющихся веществ . К легкоокисляющимся лекарственным веществам следует отнести аскорбиновую кислоту, натрия салицилат, сульфацил натрия, стрептоцид растворимый, аминазин и др.
Для стабилизации этой группы препаратов используют антиоксиданты - вещества, обладающие большим окислительно-восстановительным потенциалом, чем стабилизируемые лекарственные вещества. К этой группе стабилизаторов относятся: сульфит и метабисульфит натрия, ронгалит, аскорбиновая кислота и др. Другая группа антиоксидантов способна связывать ионы тяжелых металлов, катализирующих окислительные процессы. К ним относятся этилендиаминтетрауксусная кислота, трилон Б и др.
Растворы ряда веществ не могут приобрести необходимую устойчивость при использовании какой-либо одной формы защиты. В этом случае прибегают к комбинированным формам защиты. Комбинированную защиту используют для растворов сульфацила натрия, адреналина гидрохлорида, глюкозы, аскорбиновой кислоты и некоторых других веществ.
2.3 Приготовление
физиологических растворов в аптечных условиях
Физиологическими называются растворы, которые по составу растворённых веществ способны поддерживать жизнедеятельность клеток, переживающих органов и тканей, не вызывая существенных сдвигов физиологического равновесия в биологических системах. По своим физико-химическим свойствам такие растворы и примыкающие к ним кровезамещающие жидкости весьма близки к плазме человеческой крови. Физиологические растворы обязательно должны быть изотоничными, содержать хлориды калия, натрия, кальция и магния в соотношениях и количествах, характерных для кровяной сыворотки. Очень важна их способность сохранять постоянство концентрации водородных ионов на уровне, близком к рН крови (~7,4), что достигается введением в их состав буферов.
Большинство физиологических растворов и кровезамещающих жидкостей для обеспечения лучшего питания клеток и создания необходимого окислительно-восстановительного потенциала обычно содержат глюкозу, а также некоторые высокомолекулярные соединения.
Наиболее распространенными физиологическими растворами являются жидкость Петрова, раствор Тироде, раствор Рингера - Локка и ряд других. Иногда физиологическим условно называют 0,85% раствор натрия хлорида, применяющийся в виде вливаний под кожу, в вену, в клизмах при кровопотерях, интоксикациях, при шоке и т. д., а также для растворения ряда медикаментов при инъекционном введении.
Rp.: Natrii chloride 8,0
Kalii chloride 0,2
Calcii chloride 0,2
Natrii hydrpcarbonatis 0,2
M. Sterilisetur!
Выписана жидкая лекарственна форма для внутривенного, а также для введения в клизмах при больших потерях жидкости организмом и при интоксикации. Лекарственная форма является истинным раствором, в состав которого не входят вещества списка А и Б.
Расчеты
Натрия хлорида 8,0
Кальция хлорида 0,2
Натри гидрокарбоната 0,2
Глюкозы 1,0
Воды для инъекций 1000мл
Технология
В прописи представлены вещества, которые хорошо растворяются прописанном количестве воды. Раствор Рингера-Локка готовят путем последовательного растворения солей и глюкозы в 1000мл воды (количествр сухих ингредиентов менее 3%). При этом необходимо избегать сильного встряхивания для того, чтобы предотвратить потерю углекислоты при добавлении натрия гидрокарбоната. После растворения веществ раствор фильтруют, разливают во флаконы для кровозаменителей.
Стерилизацию проводят в паровых стерилизаторах при 120°С в течение 12-14 мин. При изготовлении и стерилизации этого раствора допустимо совместное присутствие натрия гидрокарбоната и кальция хлорида, так как суммарное содержание ионов кальция очень незначительно (не превышает 0,005%) и не может вызвать помутнения раствора. Вскрывать флаконы разрешается только по истечении 2часов после стерилизации. Срок годности раствора, приготовленного в аптеке, 1 месяц.
Дата № рецепта
Aquae pro injectionibus 1000ml
Natrii chloride 8,0
Kalii chloride 0,2
Сalcii chloride 0,2
Объем 1000мл
Простерилизовано!
Проиготовил
Проверил
Заключение
В настоящее время проводится большая работа по совершенствованию изготовления инъекционных растворов.
1. Разрабатываются новые способы и аппараты для получения воды для инъекций высокого качества.
2. Изыскиваются возможности обеспечения необходимых асептических условий изготовления, позволяющих выполнить требования стандарта GMR.
3. Расширяется ассортимент моющих, дезинфицирующих и моющедезинфицирующих средств.
4. Совершенствуется технологический процесс, используются современные производственные модули, разрабатываются новые современные приборы и аппараты (мерники-смесители, фильтрующие установки, установки ламинарного потока воздуха, стерилизующие аппараты, приборы для контроля отсутствия механических включений и др.).
5. Совершенствуется качество исходных субстанций, растворителей, расширяется ассортимент стабилизаторов различного назначения.
6. Расширяются возможности внутриаптечной заготовки растворов.
7. Совершенствуются методы оценки качества и безопасности инъекционных растворов.
8. Внедряются новые вспомогательные материалы, упаковочные и укупорочные средства.
Список литературы
1. Белоусов Ю.Б., Леонова М.В. Основы клинической фармакологии и рациональной фармакотерапии. - М.: Бионика, 2002. - 357 с.
2.Беседина И.В., Грибоедова А.В., Корчевская В.К. Совершенствование условий приготовления инъекционных растворов в аптеке с целью обеспечения их апирогенности // Фармация.- 1988.- №2.- с. 71-72.
3. Беседина И.В., Карчевская В.В. Оценка чистоты инъекционных растворов аптечного изготовления в процессе применения // Фармация.- 1988.- №6.- с. 57-58.
4. Губин М.М. Проблемы изготовления инъекционных растворов в производственных аптеках // Фармация. – 2006. - №1.
5. Молдовер Б.Л. Асептически изготовляемые лекарственные формы Санкт-Петербург, 1993.
6. Предварительная и стерилизующая фильтрация инъекционных растворов, парентеральных препаратов большого объёма. http://www.septech.ru/items/70
7. Сбоев Г.А., Краснюк И.И. Проблемы гармонизации аптечной практики c международной системой фармацевтической помощи. // Ремедиум. 30.07.2007 г.
8. Современные аспекты технологии и контроля качества стерильных растворов в аптеках / Под ред. М.А.Алюшина. – М.: Всесоюз. Центр науч.-фармац. информ. ВО Союзфармация, 1991. – 134с.
9. Справочник Видаль. Лекарственные препараты в России. – М.: АстраФарм-Сервис, 1997. – 1166 с.
10. Ушкалова Е.А. Фармакокинетические лекарственные взаимодействия //Новая аптека. - 2001. - № 10. - С.17-23.
Для изготовления инъекционных растворов применяют воду очищенную повышенной чистоты, полученную дистилляцией или методом обратного осмоса (вода для инъекций).
Вода для инъекций (Aqua pro injectionibus) должна отвечать требованиям, предъявляемым к воде очищенной, но, кроме того, должна быть апирогенной и не содержать антимикробных веществ и других добавок. Пирогенные вещества не перегоняются с водяным паром, но могут попасть в конденсат с каплями воды, если дистилляционные аппараты не снабжены устройствами для отделения капель воды от пара.
Сбор воды для инъекций, как и воды очищенной, проводят в стерилизованные (обработанные паром) сборники промышленного производства или стеклянные баллоны, которые должны иметь соответствующую маркировку (бирки с указанием даты получения воды). Разрешается иметь суточный запас воды для инъекций при условии ее стерилизации сразу же после получения, хранения в плотно закрытых сосудах в асептических условиях.
Во избежание контаминации микроорганизмами, полученную пирогенную воду используют для изготовления инъекционных лекарственных форм сразу же после перегонки или в течение 24 ч, сохраняя при температуре от 5 до 10 °С или от 80 до 95 °С в закрытых емкостях, исключающих загрязнение воды инородными частицами и микроорганизмами.
Для инъекционных лекарственных форм, изготовляемых в асептических условиях и не подлежащих последующей стерилизации, воду для инъекций предварительно стерилизуют насыщенным паром.
Производство и хранение апирогенной воды для инъекционных лекарственных форм находятся под систематическим контролем санитарно-эпидемиологической и контрольно-аналитической служб.
Для изготовления инъекционных и асептических лекарственных форм разрешено применять неводные растворители (жирные масла) и смешанные растворители (смеси растительных масел с этилолеатхзм, бензилбензоатом, водно-глицериновые, этаноло-водно-глицериновые). В составе комплексных растворителей применяют пропиленгликоль, ПЭО-400, спирт бензиловый и др.
Неводные растворители обладают разной растворяющей способностью, антигидролизными, бактерицидными свойствами, способны удлинять и усиливать действие лекарственных веществ. Смешанные растворители, как правило, обладают большей растворяющей способностью, чем каждый растворитель по отдельности. Сорастворители нашли применение при изготовлении инъекционных растворов веществ, труднорастворимых в индивидуальных растворителях (гормонов, витаминов, антибиотиков и др.).
Для изготовления инъекционных растворов используют масла персиковое, абрикосовое и миндальное (Olea pinguia) - сложные эфиры глицерина и высших жирных кислот (главным образом, олеиновой). Обладая малой вязкостью, они сравнительно легко проходят через узкий канал иглы шприца.
Масла для инъекций получают методом холодного прессования из хорошо обезвоженных семян. Они не должны содержать белка, мыла (<0,001 %). Обычно масло жирное содержит липазу, которая в присутствии ничтожно малого количества воды вызывают гидролиз сложноэфирной связи триглицерида с образованием свободных жирных кислот. Кислые масла раздражают нервные окончания и вызывают болезненные ощущения, поэтому кислотное число жирных масел не должно быть более 2,5 (< 1,25 % жирных кислот, в пересчете на кислоту олеиновую).
Отрицательные свойства масляных растворов - высокая вязкость, болезненность инъекций, трудное рассасывание масла, возможность образования олеом. Для снижения отрицательных свойств в некоторых случаях в масляные растворы добавляют сорастворители (этилолеат, спирт бензиловый, бензилбензоат и др.). Масла применяют для изготовления растворов камфоры, ретинола ацетата, синэстрола, дезоксикортикостерона ацетата и других, главным образом для внутримышечных инъекций и довольно редко - для подкожных.
Этанол (Spiritus aethylicus) применяют как сорастворитель при изготовлении растворов сердечных гликозидов и как антисептик, находит применение в составе противошоковых жидкостей.
Этанол, применяемый в растворах для инъекций, должен иметь высокую степень чистоты (без примеси альдегидов и сивушных масел). Применяют его в концентрации до 30 %.
Этиловый спирт иногда используют как промежуточный растворитель веществ, не растворимых ни в воде, ни в масле. Для этого вещества растворяют в минимальном объеме спирта, смешивают с оливковым маслом, а затем этанол отгоняют под вакуумом и получают практически молекулярный раствор вещества в масле. Такой технологический прием используют при изготовлении масляных растворов некоторых противоопухолевых веществ.
Спирт бвнзиловый (Spiritus benzylicus) - бесцветная, легкоподвижная, нейтральная жидкость с ароматическим запахом. Растворим в воде в концентрации около 4 %, в 50 % этаноле - в соотношении 1:1. С органическими растворителями смешивается во всех соотношениях. Применяют как сорастворитель в масляных растворах в концентрации от 1 до 10%. Обладает бактериостатическим и кратковременным анестезирующим действиями.
Глицерин (Glycerinum) в концентрации до 30 % применяют в растворах для инъекций. В больших концентрациях обладает раздражающим действием вследствие нарушения осмотических процессов в клетках. Глицерин улучшает растворимость в воде сердечных гликозидов и др. В качестве дегидратирующего средства (при отеках мозга, легких) глицерин вводят внутривенно в виде 10 - 30% растворов в изотоническом растворе натрия хлорида.
Этилолеат (Ethylii oleas). Это сложный эфир ненасыщенных жирных кислот с этанолом. Он представляет собой светло-желтую жидкость, не растворимую в воде. С этанолом и маслами жирными этилолеат смешивается во всех соотношениях. В этилолеате хорошо растворяются жирорастворимые витамины, гормоны. Применяют в составе масляных растворов для повышения растворимости и понижения вязкости растворов.
Бензилбензоат (Benzylii benzoas) - бензиловый эфир бензойной кислоты - бесцветная, маслянистая жидкость, смешивается с этанолом и маслами жирными, повышает растворимость в маслах стероидных гормонов, предотвращает кристаллизацию веществ из масел в процессе хранения.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Дайте определение «тары». Какие материалы используют для изготовления тары?
2. Какие виды укупорочных средств используют в аптечной практике?
3. Как проводится обработка аптечной тары и средств укупорки?
4. Как осуществляют контроль чистоты посуды в аптечной практике?
5. Каков режим стерилизации аптечной тары и средств укупорки?