Sündroomi paroksüsmaalsed tahhükardiad võivad areneda nii lapsepõlves kui ka täiskasvanueas, kuid enamasti ilmnevad esimesed nähud. kaasasündinud anomaalia ilmnevad lastel või noortel meestel.
SVC sündroom lapsel
Paljudel juhtudel avaldub haigus juba lapse esimestel elupäevadel. Vastsündinu haigus algab alati ootamatult ja avaldub paroksüsmaalse tahhükardia rünnakuna, mis võib põhjustada südamepuudulikkust. Lapsepõlves alanud patoloogia ei pruugi pikka aega avalduda, seejärel kordub noorukieas.
Olenemata lapse vanusest, kliiniline pilt rünnak on sama: see algab, rünnak on äkiline, südame löögisagedus ületab 200 lööki minutis, vererõhk langeb, selle maksimumväärtused võivad ulatuda 60/70 mm-ni. rt. Art., miinimum ei ole registreeritud. Laps muutub kahvatuks, täheldatakse periolabiaalse ruumi ja (harva) jäsemete tsüanoosi. Süda lööb valesti, nii puhkeolekus kui ka stressis, laps võib kogeda südamevalu ja minestada. Sündroomi rünnak peatub, nagu see algab, äkki. Vanusega väheneb kodade impulsside kiirus mööda lisaradu ja mõnikord kaovad EKG eelergastuse tunnused täielikult.
Wolff-Parkinson-White'i sündroom rasedatel
Kui patoloogia raseduse ajal ei avaldu, pole täiendavat ravi vaja. Kuid mõnikord võib see sündroom raseduse ajal ilmneda paroksüsmaalse tahhükardiana. Sellisel juhul on vajalik kardioloogi konsultatsioon ja efektiivne ravi.
Väga sagedaste südame rütmihäirete korral on suur oht uute NVT episoodide tekkeks – supraventrikulaarsed tahhükardiad ja hoogude süvenemine. Eluohtlikud rütmihäired võivad samuti esile kutsuda kudede ja elundite vereringe puudulikkuse. See mõjutab negatiivselt nii rase naise seisundit kui ka loote arengut. Seetõttu on väga sagedaste tahhükardiate korral rasedus vastunäidustatud.
SVC sündroom - lühidalt
Wolff-Parkinson-White'i sündroom - täiendava raja olemasolu südames ( Kenti kimp), mis põhjustab rütmihäireid.
Täiendav veresoonte kimp tuvastatakse patsientidel alates sünnist, kuid esimesed sümptomid ilmnevad tavaliselt noorukieas.
Harvadel juhtudel on SVC sündroomi rütmihäired eluohtlikud.
SVC sündroomi ravi on kirurgiline - lisaraja hävitamine kirurgiliste meetoditega.
SVC sündroomi sümptomid
SVC tavalised sümptomid:
- kiire pulss
- südamelöögid
- pearinglus
- väsimus, kui kehaline aktiivsus
- minestamine
Sümptomid ilmnevad tavaliselt esmakordselt noorukieas, nagu juba mainitud. SVC sündroom on kaasasündinud. Täiendava tala ilmumise põhjus on geneetiline. Rütmihäirete episoodid kestavad mõnest sekundist mitme tunnini ja esinevad sagedamini füüsilise tegevuse ajal. Sümptomite ilmnemise põhjuseks võib olla teatud ravimite võtmine või liigne kofeiinisisaldus toidus ja mõnikord ka suitsetamine.
Raskematel juhtudel, eriti kui SVC sündroom on kombineeritud teiste südamehaigustega, võivad sümptomid hõlmata järgmist:
- raskustunne või valu rind
- hingeldus
- äkksurm
Mõnikord ei põhjusta täiendava raja olemasolu südames üldse sümptomeid ja see tuvastatakse alles EKG tegemisel.
SVC sündroom - rohkem üksikasju
Inimese süda koosneb neljast kambrist – paremast ja vasakust kodadest ning paremast ja vasakust vatsakesest. Südame kokkutõmbumise rütmi määrab südamestimulaator, see asub paremas aatriumis ja on nn. siinusõlm(seetõttu nimetatakse õiget rütmi siinusrütmiks).
Alates siinusõlm selle tekitatud elektriimpulss levib läbi kodade ja siseneb teise kodade ja vatsakeste vahel asuvasse sõlme (atrioventrikulaarne või atrioventrikulaarne või AV-sõlm). AV-sõlm aeglustab mõnevõrra impulsi juhtivust. See on vajalik selleks, et vatsakestel oleks aega kodadest verega täituda. Elektriimpulsi edasist teed me siinkohal ei uuri. SVC sündroomi korral on kodade ja vatsakeste vahel täiendav rada, mis möödub AV-sõlmest.
Milleni see võib viia? Elektriimpulss jõuab liiga kiiresti vatsakestesse – nn preexitation.
Pealegi võib elektriimpulss sattuda ahelasse ja hakata väga suurel kiirusel ringlema kodade ja vatsakeste vahel – tekib tahhükardia (kiire südamelöök). taassisenemine(taassisenemine). Selline tahhükardia on ohtlik eelkõige seetõttu, et liiga kiiresti kokku tõmbuvad vatsakesed ei jõua verega täituda ja süda töötab jõude, ei pumpa verd või pumpab seda liiga vähe (vähenenud südame väljund).
Südame väljundi puudumine või märkimisväärne vähenemine põhjustab katastroofilisi tagajärgi:
- halvimal juhul - äkksurma
- vererõhu languseni
- teadvusekaotus (kui aju ei saa piisavalt verd)
- südameisheemia (kui süda ei saa koronaararterite süsteemi kaudu piisavalt verd)
Võib tekkida ka teine probleem – elektriimpulsid hakkavad kaootiliselt läbi kodade liikuma, põhjustades nende kaootilisi kokkutõmbeid. Seda seisundit nimetatakse kodade virvendusarütmiaks (või kodade virvendusarütmiaks). Kodadest tulevad kaootilised impulsid võivad kiirendada ka vatsakeste kokkutõmbeid, mis jällegi viib südame väljundi vähenemiseni.
SVC uurimine
Lisaks patsiendi küsitlemisele ja uurimisele määravad arstid:
- Elektrokardiogramm. EKG (isegi sümptomite puudumisel) näitab spetsiaalset lainet täiendava juhtivuse rajast (deltalaine) ja elektrilise impulsi kiirenemist kodade ja vatsakeste vahel.
- EKG 24 tunni jooksul - nn. Holteri jälgimine. Patsient kannab 24 tundi kaasaskantavat EKG-seadet ja seejärel analüüsitakse salvestist. Holteri monitooring annab oma kestuse tõttu palju rohkem teavet südamerütmi kohta kui tavaline EKG.
- Elektrofüsioloogiline uuring. Selle uuringu käigus suunatakse spetsiaalsed elektroodidega kateetrid veresoonte kaudu südame erinevatesse osadesse, mis võimaldab täpselt tuvastada täiendava kimbu asukohta (et see seejärel hävitada). Põhimõtteliselt on elektrofüsioloogiline uuring teatud tüüpi EKG, kuid suurema arvu elektroodidega. Sageli kombineeritakse elektrofüsioloogilist testimist raviga - raadiosagedusliku kateetri ablatsiooniga (vt allpool).
SVC sündroomi ravi
Mittekirurgiline ravi
Tahhükardia tekkimisel võite proovida rütmi aeglustada järgmistel viisidel:
- vagaalsed testid. Vagaalsed testid või vagaalsed manöövrid on vagusnärvi (nervus vagus) stimuleerimine, mis aeglustab südamelöögid. Vagaaltestid hõlmavad pingutamist, unearteri siinuse massaaži (retseptorpunkt unearteril) jne.
- kui vagaaltestid ei aita, kasuta uimastiravi- manustatakse arütmiavastaseid ravimeid (erinevad olenevalt arütmia tüübist - amiodaroon, flekainiid, propafenoon, adenosiin jne) ja/või rütmi aeglustavaid ravimeid (beetablokaatorid nt esmolool) (tavaliselt intravenoosselt, loomulikult ainult Arst).
- Elektriline kardioversioon – kasutatakse tavaliselt siis, kui patsient on ebastabiilne või kui ravimteraapia on ebaefektiivne. Elektrilise kardioversiooni ajal, kasutades defibrillaatorit spetsiaalses sünkroniseeritud režiimis, antakse tuimastatud patsiendi südamele võimas elektriline impulss, mis "vaigistab" kõik ebanormaalsed südamestimulaatorid, nii et "juhised" naasevad siinussõlme.
Mõnele patsiendile määratakse pidevalt antiarütmikumid, et vältida arütmia episoode, peamiselt neil, kes ei ole radioablatsiooni kandidaadid.
SVC sündroomi kirurgiline ravi
Raadiosageduslik kateetri ablatsioon on SVC sündroomi ravis kõige sagedamini läbiviidav protseduur. Arst sisestab kateetri läbi veresoon südamesse kohas, kus ebanormaalne kiir läbib, ja hävitab selle kiire kõrgsagedusliku elektriimpulsi abil. Protseduur viiakse läbi kohaliku anesteesia all. Selle efektiivsus on peaaegu 100%. Sellega kaasnevad tüsistused on haruldased.
Wolff-Parkinson-White'i sündroomi kirurgilist ravi kasutatakse praegu harva, peamiselt juhuslikult, kui südameoperatsioon on vajalik muul põhjusel.
W.P.W.A tüüpi sündroom W.P.W. - vasaku vatsakese enneaegse erutuse väljendus
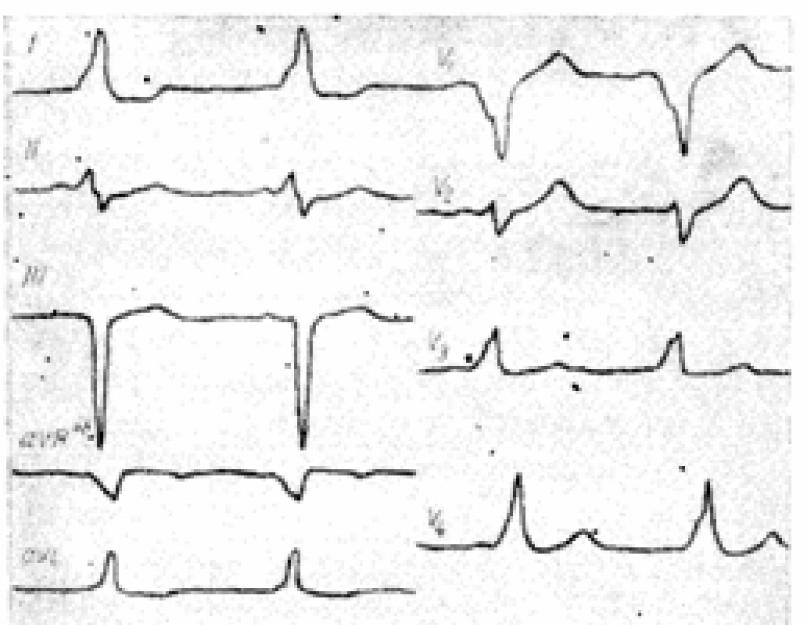
Südame potentsiaali uurimine arvukate otse epikardist tulevate juhtmetega võimaldas täpsemalt määrata täiendava juhtiva koe kimbu lokaliseerimise koht ja selle põhjal eristage WPW sündroomi nelja vormi: 1. Parema vatsakese eesmise basaalosa enneaegne erutus elektrokardiogrammiga, mis näitab B-tüüpi WPW sündroomi olemasolu (vatsakeste kompleks, juhtmetes valdavalt negatiivneV 1 ja V 2). 2. Posterobasaalse osa enneaegne erutus parema vatsakese elektrokardiogramm, mis sarnaneb WPW sündroomi B-tüüpi EKG-ga (vatsakeste kompleks on V1 puhul valdavalt negatiivne, kuid valdavalt positiivne V 2). 3. Vasaku vatsakese posterobasaalse osa enneaegne erutus elektrokardiogrammiga, mis näitab A-tüüpi WPW sündroomi olemasolu (vatsakeste kompleks on V1-s valdavalt positiivne ja perifeersetes juhtmetes - II, III aVF kehtestatakse patoloogilise lainega negatiivne deltalaine K ). 4. Külgmise vasaku vatsakese enneaegne erutus ebaiseloomuliku elektrokardiogrammiga, mis näitab veidi lühendatud P-intervalli R , väike delta laine, millel on rohkem väljendunud Q-laine Mina, aVL ja V 5, V 6 juhet, veidi laiendatud või laiendamata kompleks QRS , ei ole muutust ST-T.
sündroomW.P.W.võib olla konstantne, mööduv, vahelduv või ilmneda ainult üksikutes ventrikulaarsetes kompleksides.
A-tüüpi iseloomustab positiivne delta-laine ja positiivsed sarnased ventrikulaarsed kompleksid kõigis rindkere juhtmetes. EKG pliis V1 näitab valdavalt positiivset ventrikulaarset kompleksic R , RS , Rs , RSr , või Rsr"-konfiguratsiooniga ja juhtpositsioonil V 6 - Rs või R-vormi jaoks. Alumistes perifeersetes juhtmetes - II, III ja aVF , on sageli negatiivne delta laine koos patoloogilise lainega K . Südame elektriline telg ( aqrs)kaldus vasakule.
Diferentsiaaldiagnoos. WPW sündroomi tuleks eristada kimbu harude blokaadi, müokardiinfarkti ja ventrikulaarsete ekstrasüstoolide elektrokardiograafilistest mustritest.
|
Märgid |
Kimbu haruplokk |
WPW sündroom |
|
Intervall PQ(R) |
Tavaline |
Lühendatud |
|
PJ intervall |
Laiendatud |
Tavaline |
|
Langev jalg R |
Sakiline ja tasane |
Sujuv ja jahe |
B-tüüpi sündroom W.P.W. - parema vatsakese enneaegse erutuse väljendus

B-tüüpi iseloomustab negatiivne või kahefaasiline delta-laine ja valdavalt negatiivne vatsakeste kompleks pliis Vi ning positiivne delta-laine koos positiivse vatsakese kompleksiga vasakpoolsetes prekordiaalsetes juhtmetes. Juhtis V 1 rS, QS või qrS-i konfiguratsiooniga ja juhtpositsioonil V6 - kõrge R-laine I ja II juhtmetes on delta laine positiivne. Südame elektriline telg kaldub vasakule
WPW sündroomi juhtumeid on palju, mis on üleminekuvorm või A ja B tüüpide kombinatsioon, nn. segatüüpi või tüüp A-B sündroom W.P.W.

WPW sündroomi ajutine leevendamine pärast ajmaliini manustamist on oluline, kuna see võimaldab eristada seda müokardiinfarkti ajal esinevatest elektrokardiograafilistest muutustest (joonis 228).
Prognoos WPW sündroomiga on see väga hea tahhükardia ja südamehaiguste rünnakute puudumisel. Enamikul paroksüsmaalse tahhükardiaga WPW sündroomi juhtudel on ka prognoos soodne. Äkksurma võimalus väga kõrge vatsakeste sagedusega tahhükardiahoo ajal, kuigi see on väga haruldane, halvendab prognoosi. Kui WPW sündroom kombineeritakse südamehaigustega, suureneb tahhükardiahoo ajal surma võimalus.
Paroksüsmaalse tahhükardia rünnakute ravi WPW sündroomi korral
Supraventrikulaarset paroksüsmaalset tahhükardiat ravitakse beetablokaatorite, verapamiili, ajmaliini või amiodarooni intravenoosne infusioon. Samuti on tõhusad vaguse närvi mehaanilise stimulatsiooni meetodid, digitaalise ja kinidiini kasutamine. Kui nende kasutamine on ebaõnnestunud ja esinevad hemodünaamilised häired kasutada elektroimpulssravi väikestes kogustes või südame elektriline stimulatsioon sisestatud elektrood paremasse aatriumisse.

Kui vatsakeste löögisagedus ei ole eriti kõrge, kodade virvenduse rünnakud töödeldud digitaalisega ja seejärel kinidiin tavalise meetodi järgi. Kui vatsakeste löögisagedus on väga kõrge, võib sõltuvalt patsiendi seisundist proovida digitaalist, prokaiinamiidi või ajmaliini või elektriimpulssravi. Kõikidel sündroomi juhtudelW.P.W.kombinatsioonis südamehaigustega (reumaatilised haigused, hüpertensioon, südame isheemiatõbi, kardiomüopaatia) on elektroimpulssravi eelistatud vahend tahhükardiahoogude peatamiseks, eriti kui need põhjustavad hemodünaamilisi häireid.
Paroksüsmaalse tahhükardia ventrikulaarne vorm ravitakse lidokaiin või prokaiinamiid, ja kui mõju pole - viiakse läbi elektroimpulssravi.
|
Esimene järjekord tähendab |
Beetablokaatorid kinidiin digitaalis |
|
Teise järgu tähendab |
Prokaiinamiid difenüülhüdantoiin reserpiin kaaliumkloriid |
Sündroomi ennetav uimastiravi W.P.W.vajalik juhtudel, kui tahhükardiahood on sagedased, pikaajalised või põhjustavad patsientidel olulisi kaebusi.
Väga sobiv on beetablokaatori kombineerimine digitaalise või kinidiiniga või kinidiin digitaalisega.
IN viimased aastad, WPW sündroomi korral, mis ei allu ravimteraapiale, kasutage kirurgiline ravi, mis koosneb täiendava juhtiva koe kimbu lõikamisest. WPW sündroomi kirurgilise ravi kogemused on endiselt liiga väikesed, et teha lõplikke järeldusi selle tõhususe ja püsivate operatsioonijärgsete tulemuste kohta.
vatsakeste enneaegne ergastumine ATRIOVENTRIKULAARSÕLMME LÄBI IMPULSIDE NORMAALSE AJAL
Sellistel ebapiisavalt selgitatud juhtudel on elektrokardiogrammil näha delta laine ja laienenud kompleks QRS , nagu WPW sündroomi puhul, kuid erinevalt viimasest intervall P-Rtavaline või mõnikord piklik. Arvatakse, et vatsakeste aktiivsuse enneaegne ergastumine toimub Mahaimi kimbu kaudu, mis tekib atrioventrikulaarse sõlme all, ja seetõttu läbib erutusimpulss tavaliselt atrioventrikulaarset sõlme.
SÜNDROOM MADAL – GANONG – LEVINE
Seda täheldatakse peamiselt orgaanilise südamehaiguseta keskealistel naistel, kellel esineb P-intervalli lühenemine.R <0,12 секунды, нормальной формы и длительности комплекс QRS и склонность к пароксизмальным наджелудочковым тахикардиям. Предполагают, что речь идет об аномалии, при которой наджелудочковый импульс возбуждения обходит атриовентрикулярный узел, распространяясь по ненормально длинным дополнительным проводящим пучкам Джеймса, и поэтому отсутствует физиологическое замедление проводимости в атриовентрикулярном узле примерно на 0.07 сек. и интервал P-R lühendab. Vatsakeste erutus toimub tavapärasel viisil ja kompleksselt QRS – ST – Tei ole patoloogilisi muutusi

ELEKTROLÜÜDID JA RÜTMI HÄIRED
Elektrolüütide – kaaliumi, naatriumi, kaltsiumi ja magneesiumi – kontsentratsioonide ja vahekordade muutused rakuvälises ja rakusiseses vedelikus võivad põhjustada erinevaid juhtivuse ja südame rütmihäireid.
KAALIUM (K+)
Normaalne kaaliumi kontsentratsioon vereseerumis on 16-21 mg% (3,8-5,5 mEq/L).
HÜPERKALEEMIA
Hüperkaleemiat (K+ >5,5 mEq/l) täheldatakse järgmistel juhtudel:
Addisoni tõve kriis
Diabeetiline atsidoos
Neerupuudulikkus koos ureemiaga
Hemolüüs
Hüpovoleemiline šokk
Kaaliumisoolade üleannustamine ravi ajal
Elektrokardiograafilised märgid
Kerge hüperkaleemia korral (5,5-7,5 mEq/L) juhtivus ja rütm tavaliselt ei ole häiritud. Ainult T-laine muutub kõrgeks ja teravaks, sümmeetrilise kujuga kitsa põhjaga
Kaaliumi kontsentratsiooni edasine tõus (7-9 mEq/l) häirib intraatriaalset juhtivust – P-laine laieneb, muutub väga madalaks ja kahefaasiliseks. Mõnikord kaovad kodade lained sinoaurikulaarse blokaadi ilmnemise tõttu ja atrioventrikulaarse või idioventrikulaarse asenduskeskuse impulsside mõjul tõmbuvad vatsakesed kokku. Prong R muutub madalamaks ja hammas S-sügavamale ja laiemale
Kõrge hüperkaleemia korral (10 mEq/L või rohkem) intraventrikulaarne juhtivus on häiritud, keeruline QRSlaieneb ja deformeerub nagu kimbu haruploki puhul; Ilmub ventrikulaarne tahhükardia, ventrikulaarne fibrillatsioon, aeglane ventrikulaarne põgenemisrütm ja lõpuks ventrikulaarne asüstool. Ventrikulaarsele fibrillatsioonile eelneb sageli ventrikulaarne ekstrasüstool. Atrioventrikulaarne blokaad on väga haruldane

Hüperkaleemia neerupuudulikkusega patsiendil, kellele manustati intravenoosselt kaaliumkloriidi. Kui seerumi kaaliumisisaldus on 7,2 mEq/l, näitab elektrokardiogramm juhtmetes V2–6 väga kõrgeid, sümmeetrilisi, kitsapõhjalisi ja teravate otstega T-laineid. Kui kaaliumisisaldus vereseerumis on 9,4 mEq/l, siis ventrikulaarne kompleks laieneb ja on tugevalt deformeerunud, moodustades kimbu harublokaadi.
Suurenenud kaaliumiioonide kontsentratsioon rakuvälises vedelikus vähendab transmembraanset kaaliumigradienti ja selle tulemusena väheneb membraani potentsiaal puhkeolekus ja aeglustab juhtivus: rakumembraani kaaliumi läbilaskvus suureneb ja seeläbi kaaliumisisalduse tase. repolarisatsioon suureneb ja aktsioonipotentsiaali aeg lüheneb, diastoolse depolarisatsiooni aste siinusrakkudes väheneb sõlme- ja ektoopilised kolded.
Sest diagnostika hüperkaleemia, olulist rolli mängivad ka muud kliinilised ilmingud: üldine nõrkus, oksendamine, äkiline tõusva kvadripleegia, kõne- ja mõtlemishäired, millega kaasneb südame nõrkus, kollaps, oliguuria ja asoteemia. Surm saabub vatsakeste virvenduse või ventrikulaarse asüstoolia tõttu. Kirjeldatud kaaliumi toime müokardile on pöörduv protsess, kui on võimalik kiiresti vähendada selle kontsentratsiooni vereseerumis.
Ravi. Glükoosi ja insuliini manustamine toob kaasa kaaliumi kiire ülekandumise seerumist maksa ja lihastesse. Naatriumi manustamine suurendab kaaliumi eritumist organismist. Kaltsium on kaaliumi antagonist ja seetõttu manustatakse seda intravenoosselt või suukaudselt. Väga kõrge hüperkaleemia astmega on vaja läbi viia peritoneaaldialüüs või kasutada kunstneeru. Kasutatakse ka katioonvahetusvaikusid ja keha leelistamist.
HÜPOKALEEMIA
Hüpokaleemia (K+<3,9 мэкв/л) наблюдается при:
Kõhulahtisus ja oksendamine, ileostoomia, sapiteede fistul Turse kiire resorptsioon
Pikaajaline ravi diureetikumidega, eriti kombinatsioonis digitaalise preparaatidega Hemodialüüs
Insuliini ja glükoosi samaaegne kasutamine Hepatargia
Ravi ajal kortikosteroidide ja AKTH-ga Itsenko-Cushingi tõve korral Pärast gastrektoomiat ja haavandilist koliiti Perekondliku perioodilise halvatuse korral Suure vedeliku ja naatriumvesinikkarbonaadi infusiooniga
Elektrokardiograafilised sümptomid on mittespetsiifilised


Kõige tavalisem ja varajane märk on suurenenud laine amplituud U intervalli pikendamata K-T. Laine U peetakse patoloogiliselt kõrgeks, kui see on võrdne või suurem kui T-laine antud juhtmes või kui see ületab 0,1 mm või üle 0,5 mm juhtmes II ja üle 1 mm juhtmes V3, või U >T juhtmetes II ja V3 või T/U<1 во II или V3 отведении.
Segment ST liigub alla ja T-laine muutub madalaks või negatiivseks. ST muutused-T on mittespetsiifilised.
Teine iseloomulik märk, mis ilmneb raskema hüpokaleemia korral, on P-laine suurenemine ja teravnemine, Ma omandan kopsulaine P kujuga sarnase kuju
Hüpokaleemia esinemissagedus suureneb pidevalt salureetikumide ja kortikosteroidide laialdase kasutamise tõttu. Hüpokaleemia suurendab autonoomsete keskuste erutatavust ja põhjustab kõige sagedamini kodade ja vatsakeste ekstrasüstole, harvemini kodade tahhükardiat kombinatsioonis atrioventrikulaarse blokaadi ja sõlme tahhükardiaga või ilma nendeta. Mõnikord täheldatakse kompleksi kerget laienemistQRS ja intervalli pikkuse mõningane suurenemine PQ(R). BHarvadel juhtudel võib raske hüpokaleemia põhjustada ventrikulaarset tahhükardiat või vatsakeste virvendusarütmiat. Teise astme või kõrgema astme atrioventrikulaarne blokaad on väga haruldane.
Vagusnärvi ärritus hüpokaleemia ajal põhjustab rohkem väljendunud bradükardilist toimet ja pärsib oluliselt atrioventrikulaarset juhtivust. Hüpokaleemia suurendab müokardi tundlikkust südameglükosiidide toimele.
Digitaal ja strofantiin terapeutiliselt talutavas annuses või isegi väikeses annuses hüpokaleemia korral võivad põhjustada erinevat tüüpi emakaväliseid arütmiaid, sealhulgas ventrikulaarset virvendusarütmiat, mis on sageli surmav. On tõestatud, et "redigitaliseerumise" nähtus, st digitaalise tugeva toime ilmnemine või sellega mürgistuse ilmnemine pärast diureetikumravi koos tursete kiire resorptsiooniga, on põhjustatud hüpokaleemiast. Otsustav roll rütmihäireid mängib rakuvälise ja intratsellulaarse kaaliumitaseme suhe. Elektrokardiogrammi muutuste ja ioonide kontsentratsiooni vahel ei ole seerumi kaaliumisisaldus hüpokaleemia korral tihedas korrelatsioonis. Seerumi kaaliumisisaldus on vaid kaudne näitaja, mis ei anna kaaliumisisaldusest täpset ülevaadet Elektrokardiogramm ja erütrotsüütide kaaliumisisaldus võivad anda teadaolevat teavet rakusisese kaaliumisisalduse kohta.
Ravi. Hüpokaleemiast tingitud rütmihäired on pöörduvad ja kaovad tavaliselt pärast kaaliumkloriidi suukaudset manustamist 3 korda päevas 2-3 g või pärast 3,7 g kaaliumkloriidi aeglast intravenoosset infusiooni, mis on lahustatud 1 liitris 5% glükoosis. Intravenoosset kaaliumit tuleb manustada pideva elektrokardiograafilise jälgimise all, jälgides seerumi kaaliumisisaldust.
KALTSIUM (CA+)
Kaltsiumi normaalne kontsentratsioon vereseerumis on 9-11,5 mg °/o.
HÜPERKALTSEEMIA
Hüperkaltseemiat (Ca 2+ >11,5 mg%) täheldatakse suhteliselt harva:
Hüperparatüreoidism Tugev ravi kaltsiumisooladega
Kasvaja metastaasid luudes
Vitamiinimürgitus DSarkoidoos, hulgimüeloom
Elektrokardiograafilised märgid. Tavaliselt ilmnevad need kaltsiumi kontsentratsioonil seerumis umbes 15 mg%.

Bradükardia
Intervalli lühendamine K -T oluliselt lühendatud segmendi tõttuST
Kompleksi väike laiendusQRS
Intervalli kerge pikenemine PQ(R)
Arütmiaid täheldatakse suhteliselt harva - ventrikulaarsed ekstrasüstolid, ventrikulaarne tahhükardia ja mõnikord ka vatsakeste virvendus.
Võib ilmuda erineva raskusastmega atrioventrikulaarne blokaad ja kodade virvendusarütmia. Väga kõrge kaltsiumi kontsentratsiooni korral (üle 65 mg%) tekib siinustahhükardia ventrikulaarsete ekstrasüstoolide ja ventrikulaarse fibrillatsiooniga. Süda seiskub süstoolis. Kaltsiumisoolade intravenoosne manustamine põhjustab sageli müokardi erutatavuse äkilist suurenemist. Kirjeldatakse hüperkaltseemiast põhjustatud vatsakeste virvenduse tõttu operatsioonijärgset äkksurma juhtumeid. Rütmihäired on sagedane juhtum pärast kaltsiumi intravenoosset manustamist elustamise või südameoperatsiooni ajal. Sõrmenahk suurendab sageli hüperkaltseemia põhjustatud toimet ja vastupidi. Kaltsiumi kasutamine digitaalise preparaatidega küllastunud patsientidel on vastunäidustatud, kuna hüperkaltseemia suurendab südamelihase erutatavust ja tundlikkust digitaalise suhtes, mis võib põhjustada surmavaid arütmiaid.
Ravi. Parima efekti annab etüüldiaminotetraatsetaadi (MaEDTA) naatriumsool, mis alandab kiiresti ioniseeritud kaltsiumi taset vereseerumis.
HÜPOKALTSIEMIA
Hüpokaltseemia (ca<9 мг%) наблюдается при:
Hüpoparatüreoidism
Neerupuudulikkus koos ureemiaga
Hepatargia
Äge nekrotiseeriv pankreatiit
Raske steatorröa
Suure koguse tsitraadi vereülekanne
VitamiinipuudusD
Osteomalaatsia
Hingamisteede või mittegaasiline (metaboolne) atsidoos
Elektrokardiogramm

Pikendatud intervall K -T väga pikliku segmendi tõttuST
Hüpokaltseemia ei põhjusta tavaliselt juhtivuse häireid ega põhjusta tõsiseid emakaväliseid arütmiaid. Mõnikord täheldatakse ventrikulaarseid ekstrasüstole
Hüpokaltseemia vähendab südamelihase kontraktiilsust, süvendab südamepuudulikkust ja pärsib digitaalise ravimite toimet südamele.
NAATRIUM
Hüper- või hüponatreemiast tingitud rütmihäireid ei täheldata. Raske hüponatreemia võib põhjustada elektrokardiograafilisi muutusi, mis on sarnased hüperkaltseemia korral täheldatuga.
MAGNEESIUM
Normaalne seerumi magneesiumisisaldus on vahemikus 1,4 kuni 2,5 mekv/l. Hüpermagneseemia pikendab müokardi refraktaarset perioodi, pärsib erutuvust ja aeglustab juhtivust. See õigustab magneesiumsulfaadi kasutamist kodade ja vatsakeste ekstrasüstoolide ja paroksüsmaalse tahhükardia ravis, kuid selle terapeutiline toime on ebajärjekindel ja ebausaldusväärne. Kõrgema seerumi magneesiumikontsentratsiooni (27-28 mEq/L) korral intervallPQ(R ) pikeneb, ilmneb erineva raskusastmega atrioventrikulaarne blokaad, kompleks QRS laieneb ja tekib südameseiskus („ südame seiskumine"). Hüpermagneseemiaga kaasnevad elektrokardiograafilised muutused on sarnased hüperkaleemiaga kaasnevatele muutustele.
Hüpermagneseemia võib põhjustada supraventrikulaarseid ja ventrikulaarseid arütmiaid ning luua eeldused digitaalise ravimite mürgistuse kergemaks tekkeks.
SVC sündroom on südame struktuuride arengu kaasasündinud anomaalia, mille korral südames moodustub ekstra juhtiv kimp, mis transpordib siinussõlmest vatsakestesse elektriimpulsi, möödub atrioventrikulaarsest sõlmest, mis põhjustab vatsakeste enneaegset ergutamist. .
Oma olemuselt on see pahe, kuid see ei ilmne kohe. Sümptomid varases staadiumis on minimaalsed. Reeglina on sellise nähtuse tuvastamine elektrokardiograafia käigus tuvastatud õnnetus. Märgid on üsna iseloomulikud, nii et seisundit on peaaegu võimatu segi ajada.
Seda haigust nimetatakse ka Wolff-Parkinson-White'i sündroomiks, mis on nime saanud silmapaistvamate teadlaste järgi.
Seisundi ravil on igal etapil teatud väljavaated. Need on parimad avastamise ajal, kui orgaanilisi defekte veel pole.
Hälbe olemus on lisatee moodustumine südames.
See on asjade normaalne seis. Südame struktuuridel on võime kokku tõmbuda ja töötada autonoomselt tänu aktiivsete rakkude klastri olemasolule, mis genereerib elektriimpulsi.
See on nn siinusõlm või loomulik südamestimulaator. Ta töötab pidevalt. Signaalide juhtimise eest vastutavad niinimetatud His kimbud, neil on hargnenud struktuur ja need lõpevad vatsakeste tasemel.
SVC sündroomi (Wolf-Parkinson-White) taustal moodustub täiendav impulssliikumise rada mööda Kenti kimpu.
Siit ka südametegevuse suurenenud aktiivsus, mis väljendub nii tahhükardiana (täistsüklit läbivaid kokkutõmbeid aga alati ei esine) kui ka teist tüüpi arütmiatena (virvendusest ekstrasüstoolini). Kõik sõltub konkreetse inimese haiguse arengu omadustest.

Probleemi edenedes täheldatakse häireid kõigi elundite ja süsteemide normaalses töös. Kõigepealt kannatab süda, seejärel veresooned. Aju, neerud ja maks.
Mõned suhteliselt kerged vormid on asümptomaatilised. Teised annavad selgelt väljendunud kliinilise pildi ja on seotud patsiendi äkksurma suurenenud riskiga lühiajaliselt.
Klassifikatsioon
Tüüpilised tunnused on oma olemuselt peamiselt topograafilised. See tähendab, et nad määravad kindlaks, kust tuleb liigne juhtiv struktuur, millises suunas see ulatub ja kuidas see suhtleb ümbritsevate kudedega.
Kokku on selle alusel piiritletud umbes 10 sorti. See mitmekesisus määrab võimalike ravivõimaluste ja patoloogiliste ilmingute heterogeensuse, samuti prognoosi.
Patsiendi jaoks ei oma need klassifikatsioonid suurt tähtsust, kuna nende kliinilist tähendust on võimatu mõista ilma spetsiaalse kardioloogilise koolituseta ja selgitused võtaksid palju aega.
Suur roll on patoloogilise protsessi käigu kindlaksmääramisel.
Sel põhjusel nimetatakse seda:
- Ilmutav tüüp. Tekib spontaanselt. Episoodi võib vallandada liigne füüsiline aktiivsus, närvipinge, hetkeline või pikaajaline kofeiini, tubaka ja psühhoaktiivsete ainete tarbimine. Tüübi määrab raske tahhükardia, arütmilised komponendid on võimalikud, kuid need on suhteliselt haruldased. Ägenemiste sagedus on erinev: mitmest korrast aastas kuni kümnete juhtumiteni ühe kuu jooksul.
- Vahelduv (mööduv) tüüp. Selle määravad sarnased kliinilised tunnused, kuid need avalduvad väiksema jõuga. Lisaks esineb arütmia sagedamini ja on rohkem väljendunud, mistõttu on see vorm ohtlikum kui eelmine.
- Latentne tüüp. Ta on peidetud. Sümptomid puuduvad üldse, probleem tuvastatakse elektrokardiograafias. Kas antud juhul on SVC fenomenil ja sündroomil vahe? Kahtlemata. Haigus sellisel kujul, kuigi see ei anna ennast tunda, jätkab progresseerumist ja keha hävitamist. Protsess võib kesta aastaid. Patoloogia ilmneb alles sel hetkel, kui kompensatsioonimehhanismid enam toime ei tule.
Teine arusaadav viis protsessi tüpiseerimiseks põhineb anomaalse kiire lokaliseerimisel.
Sellest lähtuvalt on kahte tüüpi:
- A. Asub vasaku aatriumi ja vatsakese vahel. Tavaliselt liigub impulss viimasele siinusest läbi atrioventrikulaarse sõlme. A-tüübi puhul jõuab signaal anatoomilisse struktuuri varem, kuid siis stimulatsioon dubleeritakse normaalset rada pidi, mis viib liigse aktiivsuseni. Sellest ka hemodünaamika ja vereringe häire suures ringis.
- B. Lokaliseerimine - parema aatriumi ja vatsakese vahel. Mehhanism on identne, kuid kuna õige struktuur tõmbub kokku, kannatab esmalt kopsusüsteem.

Kliiniliselt on kõige raskem variant segatud, kui esineb mitu oksa. See on AB tüüp. Ravi viiakse läbi kiiresti.
Mis vahe on sündroomil ja SVC nähtusel?
Põhimõtteliselt on need sünonüümid. On ainult üks erinevus. Wpw fenomenist räägitakse siis, kui patsient ei kurda enda tervise üle.
Anomaalia avastatakse juhuslikult (juhuslikult) kolmandate isikute haiguste diagnoosimisel. Esineb 30-50% elanikkonnast depressioonis. Südame struktuurid ja keha üldiselt kohanduvad. See ei mõjuta kuidagi eeldatavat eluiga.
Seoses haigusega. WPW sündroom on kliiniliselt oluline tüüp. Kuid see esineb ka erineval viisil, mis annab hea võimaluse ravida ja prognoosida. Varajases staadiumis on kliinilise pildi intensiivsus minimaalne, progresseerumine aeglane, täieliku diagnoosimise ja ravi jaoks on aega.
Seega on WPW nähtus EKG kliiniline leid. Hälvetega patsiente tuleb hoolikalt jälgida. Sümptomite puudumisel vähemalt 2-4 kuud võib inimest pidada tinglikult terveks. Sündroom määrab plaanilise ravi vajaduse. Hädaolukorras on see kiireloomuline.
Põhjused
Patoloogilise protsessi arengu peamine tõestatud tegur on kaasasündinud anomaalia. Tavaliselt moodustub süda ja kogu verevarustussüsteem 3 rasedusnädalal. Teatud tegurid põhjustavad kõrvalekaldeid loote normaalses moodustumises ja provotseerivad kaasasündinud defekte.
On täiesti võimalik, et SVC sündroom ei jää lapse ajaloos ainsaks. Kuid selline punkt ei selgita põhjuseid, mis määravad defekti tekkimise võimaluse nii varajases staadiumis.
Huvitav:
Täiendav veresoonte kimp tekib eranditult kõigil, kuid esimese trimestri lõpuks taandub ja kõik normaliseerub.
Vahetud tegurid patogeense nähtuse arengus on:
- Geneetilised mutatsioonid. Need võivad olla spontaansed, st määratud ilma vanemate kromosomaalsete defektidega seoseta. See on suhteliselt haruldane kliiniline sort. Teine võimalus on teatud geenide pärimine esivanematelt. On domineeriv või retsessiivne tüüp - see ei mängi suurt rolli. Lihtsalt sel juhul on patoloogia väljakujunemise tõenäosus väiksem, teisalt on kõik sedalaadi teadaolevad haigused palju raskemad. Sageli ei tuvastata mitte ainult südamerikkeid, vaid ka üldistatud probleeme.
- Stress raseduse ajal. Omavad suurt kliinilist tähtsust. Lapseootel ema peaks raseduse ajal vältima psühho-emotsionaalset ülekoormust. See ei taga patoloogiate puudumist, kuid riskid on viidud miinimumini. Stressi ajal eraldub verre suures koguses kortikosteroide ja katehhoolamiine. Selline reaktsioon on loomulik mehhanism negatiivsetele keskkonnateguritele, mis tagavad ellujäämise. Ühendid, nagu kortisool, norepinefriin ja teised, suurendavad lihaste toonust, vererõhku ja neil on lapse arengule toksiline toime.
- Liigne füüsiline aktiivsus. Sünnitusel olev naine ei peaks istuma ühe koha peal, vaid kõiges, mida ta vajab, teadma, millal lõpetada. Ebatavalisel tegevusel on sama mõju kui stressil, kui mitte rohkem. Selle tulemusena on võimalik raseduse spontaanne katkemine.
- Tubakatoodete, alkoholi, eriti narkootikumide tarbimine tiinuse ajal. Hoolematud “vanemad” mõtlevad vähe oma järglaste tervisele või lubavad end sõltuvustest ja nõrkustest keeldumise raskuse ja võõrutussündroomi hirmu tõttu. See on põhimõtteliselt vale praktika, millel on lootele kahjulik mõju. Kas laps sünnib tervena või mitte – sel juhul ei oska öelda ka parim arst.
- Halva kvaliteediga toit ja vesi. Raske on täpselt kindlaks teha, millist rolli see tegur mängib. Negatiivne mõju lootele aga kiirtoidust eraldatud kantserogeensetel ainetel, nn “kahjulikul” toidul, nagu praetud toidud, suitsutatud toidud, konservid ja kahtlased pooltooted. Samamoodi mõjutab monotoonset toitumist vitamiinide ja mineraalainete puudus. Menüü tuleb kohandada sündimata lapse huvidele vastavaks. Selles aitab toitumisspetsialist.
- Negatiivsed keskkonnategurid, sealhulgas liigne ioniseeriv kiirgus elukohapiirkonnas. Keha saab suurenenud taustkiirgusega kohaneda, kuid hiljem mõjutab see hetk tõenäoliselt lapse tervist. Negatiivseteks nähtusteks on õhusaaste, metallisoolade liig joogivees, päikese aktiivsus ja ultraviolettkiirguse tase.
- Somaatiliste haiguste ajalugu. Eriti hormonaalne profiil. Need mitte ainult ei süvenda raseduse kulgu, muutes selle mõnikord väljakannatamatuks, vaid mõjutavad ka loodet. Ravi viiakse ideaalis läbi raseduse planeerimise eelses staadiumis. Suurt kliinilist rolli mängivad hüpertüreoidism, spetsiifiliste kilpnäärme ainete vaegus, neerupealiste hormoonide vaegus või liig ning naistehaigused (munasarjade düsfunktsioon ebastabiilse taustaga).
- Pärilik tegur. Kui perekonnas oli vähemalt üks inimene, kes kannatas SVC sündroomi all, suureneb selle järglastele edasikandumise tõenäosus peaaegu kolmekordseks. Samal ajal saavad arstid kindlaks teha, kas see on lapsel olemas. Kohe peale sündi. Tingimuslikkus on absoluutne, see tähendab, et pärimisega pole tulevikus parandusvõimalust. Ravi on juba vajalik, ennetamine ei aita. Õnneks on selline defekt suhteliselt kerge ja selle väljakujunemise sagedus ei ole kõrge.
Neid põhjuseid tuleb käsitleda tervikuna. Veelgi enam, günekoloog peaks neile tähelepanu pöörama isegi raseduse planeerimise etapis või raseduse varases staadiumis. Vajadusel antakse saatekiri eriarsti vastuvõtule.
Sümptomid
Märgid on heterogeensed (erineb juhtumite lõikes). Kui me räägime varjatud vormist, siis neid pole seal üldse. Vahelduvad või esmased sordid määratakse sümptomite ebaühtlase täielikkuse ja intensiivsuse kliinilise pildi järgi.
Näidisloend näeb välja selline:
- Kõige iseloomulikum hetk täiendava impulsi tee olemasolul on arütmia. Võimalusi on palju. Ventrikulaarsed, kodade tüübid (esimesed on palju ohtlikumad), tahhükardia, südametegevuse aeglustumine, rühm või üksik ekstrasüstool, virvendus. Õigeid intervalle kontraktsioonide vahel hoitakse harva. See on suhteliselt hiline märk kõrvalekaldest. Selle arendamiseks kulub rohkem kui üks aasta. Tõendid kaugelearenenud sündroomi kasuks. Algfaasis piirdub kõik tahhükardiaga.
- Tundmatu päritoluga valu rinnus. Võib olla seotud episoodidega või esindada nende kärbitud versiooni. Iseloomulikud põletus- ja surveaistingud. Kipitust ei esine. Võimalik on kaasuvate haiguste areng.
- Hingeldus. Intensiivse kehalise aktiivsuse taustal või täieliku puhkeolekus. See sõltub patoloogilise protsessi staadiumist.
- Nõrkus, uimasus, töövõime langus. Eriti töö füüsilise iseloomuga.
- Nasolabiaalse kolmnurga tsüanoos. Perioraalse piirkonna sinine värvus.
- Kahvatu nahk, higistamine, kuumatunne, kuumahood.
- Minestamine ja minestus. Tavalise iseloomuga.
- Vaimse aktiivsuse ja mälu häired.
Paljud esitatud tunnused ei ole otseselt seotud SVC sündroomiga, need on põhjustatud paralleelselt esinevatest sekundaarsetest või tertsiaarsetest seisunditest.
Pole raske kindlaks teha, kus haigus ise lõpeb ja selle tüsistused algavad. WPW-d iseloomustavad erineva raskusastmega rütmihäired. Ülejäänud märgid on tema jaoks puhtalt ebatüüpilised.
Kuidas rünnak peatada?
Tahhükardia on kirjeldatud seisundile kõige tüüpilisem. Mööda Kenti kimpu naaseb impulss vatsakestest kodadesse ja AV-sõlm saadab selle kodadest tagasi vatsakestesse. Seega liigub signaal ringi ja pulss kahekordistub või kolmekordistub.

Sõltumata patoloogilise impulsi asukohast tuleb võtta stabiliseerimismeetmeid.
Kuid tasub meeles pidada: te ei saa proovida iseseisvalt taastuda. See on aja raiskamine.
Ravi sõltub rütmihäire tüübist. Kui te võtate ravimeid oma äranägemise järgi, võite surra südameseiskumise, südameataki või muude tüsistuste tõttu.
Algoritm on järgmine:
- Kutsu kiirabi. Isegi kui episood toimus esimest korda.
- Rahune maha, võta end kokku.
- Avage aken, et tuua tuppa värsket õhku.
- Eemaldage rõhuvad esemed ja ehted.
- Võtke ettenähtud ravimeid. Kui neid pole, sobib tahhükardiahoo peatamiseks Anapriliin (1 tablett) koos diltiaseemi või verapamiiliga (sama kogus). Need aitavad rütmi normaliseerida, mitte ainult seda aeglustada.
- Võite juua tablettidena emarohi, palderjani, fenobarbitaalipõhiseid ravimeid (Corvalol, Valocordin).
- Heida pikali, hinga ühtlaselt ja sügavalt. Võite proovida kasutada vagaaltehnikaid (vajutades silmamunadele vähese jõuga, iga 5-10 sekundi järel, hinge kinni hoidmine sissehingamisel koos pingutamisega jne).

Brigaadi saabumisel rääkige oma tunnetest. Kui pakutakse haiglat, minge läbivaatusele.
Diagnostika
See viiakse läbi kardioloogi järelevalve all. Haiglas või ambulatoorses keskkonnas. Olenemata liigist on aega aidata. Seetõttu võetakse kiireloomulisi meetmeid harva ja ainult tüsistuste korral.
Eksami skeem:
- Patsiendi suuline küsitlemine. Tavaliselt ei anna see palju, eriti varajases staadiumis.
- Anamneesi kogumine. Tuvastatakse tegurid: perekonna ajalugu, somaatilised patoloogiad, võetud ravimid, harjumused ja muud.
- Südame löögisageduse mõõtmine.
- Südame heli kuulamine.
- Elektrokardiograafia. See on ette nähtud peamiselt pärast rutiinset tegevust. Määrab funktsionaalse kahjustuse tüübi. Nõuetekohase kvalifikatsiooniga saab arst koguda palju kasulikku teavet. Võimalik kombineerida EFI-ga.
- Ehhokardiograafia. Primaarse või sekundaarse tüüpi orgaaniliste häirete tuvastamine.
- MRI. Südame üksikasjalike piltide saamiseks. Seda tehakse vastavalt näidustustele suhteliselt harva. Kui kahtlustatakse muid südame struktuuride defekte.
Koronograafia, vereanalüüsid, koormustestid arsti äranägemisel.
Märgid EKG-s
Iseloomuomadused:
- QRS kompleksi laiendamine (üle 0,12 sek). Deformatsioonid, mis meenutavad kimbu haruplokiga seotud deformatsioone.
- P-Q intervalli kitsendamine.
Delta laine muutub sõltuvalt protsessi tüübist:

SVC sündroomi tunnused EKG-l on spetsiifilised, isegi algaja kardioloog suudab need lahti mõtestada.
Ravi meetodid
Konservatiivne ravi on suunatud ainult sümptomite leevendamisele, hilisemates staadiumides ei saa ka sellega toime, kuna antiarütmikumide suurtes annustes on vastupidine toime.
Peamine viis normaalse südamefunktsiooni taastamiseks on raadiosageduslik ablatsioon. Tehnika põhiolemus on juhtivuse fookuse pehmendamine. Täpsus on oluline. See on minimaalselt invasiivne meetod ja võimaldab teil probleemiga toime tulla peaaegu kohe.

Preoperatiivsel perioodil on näidustatud antiarütmiliste ravimite (Amiodaroon, Hindin), vererõhku langetavate ravimite kasutamine (näidustuste korral, püsiva hüpertensiooni korral jätkatakse selliste ravimite kasutamist ka pärast radiokirurgiat).
Statsionaarne periood kestab mitmest päevast nädalani. Patsienti jälgitakse aja jooksul, rütmi stabiliseerumine väljaspool orgaanilisi häireid toimub 1-2 päeva pärast.
Kui esineb sekundaarseid või tertsiaarseid defekte (mis on juba põhjustatud südame liigsest aktiivsusest), on näidustatud eluaegne säilitusravi nende ravimitega. Seetõttu on soovitatav ravi alustada varem.
Prognoos ja võimalikud tagajärjed
Võimalike tüsistuste hulka kuuluvad:
- Südamepuudulikkus.
- Südameatakk.
- Kardiogeenne šokk.
- Insult.
- Elundi lihaskihi suurenemine.
- Vaskulaarne dementsus.
Paljudel juhtudel on elukvaliteedi märkimisväärne langus.
Enamikus tuvastatud olukordades on prognoos soodne. ERW fenomeni taustal on tulemus peaaegu garanteeritud. Teised vormid toimivad erineval viisil.
Järeldused tuleb teha protsessi dünaamika põhjal. Mida keerulisem on tüüp, seda rohkem sümptomeid, mida kauem haigusseisund kestab, seda väiksem on täieliku taastumise tõenäosus.
Suremus ilma ravita on suhteliselt kõrge. Ühest või teisest erakorralisest protsessist sureb kuni 25% kõigist patsientidest.
Head tegurid:
- Positiivne reaktsioon ravile.
- Puuduvad kaasnevad patoloogiad ega halvad harjumused.
- Soodne perekonna ajalugu.
- Normaalne kehakaal.
- Minimaalsed sümptomid.
WPW-sündroom on kaasasündinud kõrvalekalle südame juhtivuse kimpude arengus, kui moodustub liig. Sellest tuleneb südame struktuuride suurenenud aktiivsus, väljendunud arütmiad ja muud potentsiaalselt surmaga lõppevad nähtused.
Taastumine toimub spetsialiseerunud spetsialistide järelevalve all (nii rutiinravi kui ka kirurgia valdkonnas). Ainus efektiivne ravimeetod on raadiosageduslik ablatsioon. Kuid selliseid radikaalseid meetmeid pole alati vaja. Kokkupuuteviisi määrab arst.
09.11.2011, 13:54
Tere.
Palun andke mulle minu juhtumi kohta nõu.
Mees, 29 aastat vana, pikkus 183, kaal 84 kg, vererõhu norm 115/75 (pulss 75-85), maksimum mõõdetud 140/90 (pulss umbes 100) hiljutisel kardioloogi vastuvõtul, oli ilmselt väga närviline.
Mul diagnoositi lapsepõlves MV prolaps.
Olen olnud mures arütmiahoogude pärast umbes 10-aastaselt, sel ajal möödusid need iseenesest või horisontaalasendis (hoo kestus mitu minutit),
Alates umbes 20. eluaastast muutusid hood veidi sagedamaks, möödusid vagaaltestidega või horisontaalasendi võtmisel (atakkide kestus oli mitu minutit),
Viimasel paaril aastal on rünnakuid esinenud ligikaudu kord kuus, need on möödunud vagaaltestidega või horisontaalasendis (hoo kestus on mitu minutit, kui proovite neid kohe peatada).
Viimased kaks episoodi kestsid umbes pool tundi (ei saanud kohe pikali heita ja/või vagaalteste teha; lõpuks peatasid need ka vagaaltestid).
Aeg-ajalt tunnen katseid alustada arütmiat (ilmselt nn ekstrasütoolid).
Tunded arütmia ajal: südame rütmiline kokkutõmbumine tavalisest suurema sagedusega ja kontraktsiooni "sügavus" puudub; keskkonna tajumise kerge ebareaalsus; võimalik õhupuuduse tunne; hirm teadvuse kaotamise ees (seda kõike on sõnadega raske seletada). Eelmistes arütmiaepisoodides ta teadvust ei kaotanud.
Pärast mõningaid arütmiahoogusid (mitte kõiki) võib mõnikord mitu päeva tekkida tunne, et ma ei saa sügavalt hingata.
Ma pole suitsetanud üle 5 aasta, alkoholi joon kuni viimase ajani harva (aga tabavalt, ausalt öeldes), pole viimased paar kuud alkoholi tarvitanud, sest... tundis seost pohmelli sündroomi ja arütmiahoo väljakujunemise võimaluse vahel.
Kuni 2011. aastani WPW-d ei salvestatud.
2011. aasta jaanuaris registreeriti EKG-s WPW. Tegin Magnerot kuuri (saan aru, et need on lollid pillid, aga pigem üldse mitte ravim, aga arütmia episoode tundub olevat vähem).
2011. aasta veebruaris uuriti põhjalikumalt: ultraheli ja kilpnäärmehormoonid, EKG, Holter, EchoCG - MV prolaps on hemodünaamiliselt ebaoluline, kõik muu on normi piires, WPW pole kokkuvõttes kirjeldatud.
Võtsin 2011. aasta septembris-oktoobris läbi Panangini kuuri ja tundsin end subjektiivselt paremini.
2011. aasta oktoobris otsustasin mind uuesti läbi vaadata.
Tulemused:
EKG - WPW sündroom
EchoCG - MV prolaps on hemodünaamiliselt ebaoluline.
Holter - keskmine pulss 86, minimaalne 45 (uni), maksimum 164 (trepist ronimine), WPW sündroom (koormuse all - trepist ronimine - pulsisagedusel 140 WPW muutus mööduvaks, pulsisagedusel 150 juhtivus normaalseid radu).
TEE - esialgne EKG (siinusrütm, manifesteeriv RPV). RR – 512 ms, HR – 117, PQ – 112 ms, QRS – 136 ms, QT – 328 ms, VVFSU – 720 ms, kVVFSU – 208 ms. T. Wekenbach DPZhS ja AV-sõlm - 220 imp/min, ERP AV-sõlm - 270ms.
Sisse... (ma ei saa kokkuvõttes sõna välja lugeda) 270 - 330 (Ma ei saa ühikute tähistust välja, see näeb välja nagu ms) indutseeritakse ortodroomne tahhükardia (hoogude ajal tunneb end samamoodi) pulsisagedusega 208, VA - 100ms.
Järeldus: ilmneb WPW, paroksüsmaalne ortodroomne tahhükardia, soovitatav RFA.
Küsimused on järgmised:
1. Lugesin Internetist palju kirjandust ja sain teada, et vatsakeste virvenduse (ja seega ka VS-i riski) risk on suur, kui DPVA Weckenbachi punkt on üle 250...270 impulssi/min ja ERP. DPVA-st alla 250...270 ms.
Järelduste järgi otsustades on seltsimees Wekenbachi DPHS 220 imp/min, kuid DPHS-i ERP-d ei mõõdeta (või on see ainult umbes 270–330, siis mis ERP on minu DPHS)? Tsiteerisin kõik järeldusest saadud arvud.
2. Kui kiiresti on teie arvates vaja RFA teha (tuleneb esimesest küsimusest)? Ta võib alustada tablettidega, isegi kui Panangin ja Magnerot on olukorda subjektiivselt parandanud.
Vajadusel saan postitada fotod uuringutest.
Ette tänades.
09.11.2011, 20:26
1. Kui on EKG WPW tunnustega, siis postitage see. EKG abil saate määrata kiire ligikaudse lokaliseerimise, kuna see võib olla erinev;
2. Arütmiavastaseid ravimeid saab kasutada juhtivuse blokeerimiseks piki kimpu, kuid tavaliselt seda ei tehta;
3. See, mida te võtate, ei aita WPW puhul;
4. Tõepoolest, kui ERP on DPHS< 250 мс, то возрастает риск проведения по пучку мерцательной аритмии и фибрилляции желудочков;
5. Minu soovitus on tulla silmast-silma konsultatsioonile igasse keskusesse, kus RFA-d tehakse.
10.11.2011, 08:20
Aitäh.
Kas minu esitatud andmete põhjal on võimalik ERP-d määrata?
10.11.2011, 14:16
1. Ma ei saanud teie esimesest küsimusest aru. Tõestatud ortodroomse tahhükardia korral ei ole ERP ja DPP ja AV väärtus oluline.
ERP-d saab määrata AINULT programmeeritud stimulatsiooniga ja mitte mingil muul viisil (ei teksti ega muude numbrite järgi). Obsessiivne ERP tähenduse otsimine, kui vajalik ravi on täiesti selge, on neuroosi ilming.
2. Mida kiiremini, seda parem. Pärast edukat RFA-d kaob lahutatud VF-i risk.
3. Panangini ja Magnerot ei kasutata WPW jaoks, sest see on mõttetu.
10.11.2011, 15:52
Aitäh, Aleksander Ivanovitš, vastuste eest.
Vastavalt minu leitud materjalidele (teaduslikud publikatsioonid) saab VF-i tekke riski hinnata Wenckebachi punkti ja DPJ ERP väärtuste järgi.
Muidugi mitte 100% garantii, kuid siiski.
Neuroosi osas on sul ilmselt õigus - mind jahmatas info, et WPW-l võivad olla nii tõsised tagajärjed, ja olen olnud passiivne peaaegu 20 aastat. Ma tahan veidi rõõmustada.
Operatsiooni olen vaimselt otsustanud, aga selle organiseerimine võtab aega (raha, arsti leidmine jne).
Ma tahan tegelikku olukorda mõista, sellepärast küsisin DPJS-i ERP kohta, kas see on seotud numbritega 270 ms - 300 ms või mitte?
10.11.2011, 16:21
Ja ma tahan ka küsida:
sotalex? või midagi muud?
ja millistes annustes.
ette tänades
10.11.2011, 16:24
Ärge jääge rippuma ei ERP-st ega seltsimees Wenckebachist. Need on väga spetsiifilised detailid, mida paljud tõlgendavad erinevalt. ERP leiutati DPP kaudseks kinnitamiseks, kui tahhükardiat ei saanud esile kutsuda. Teie diagnoos on selge.
Kõigil, kellel on WPW sündroom, on kodade virvendusarütmia tekkimisel WPW sündroomi korral VF risk. Selle riski astmelisus sõltuvalt ERP-st on minu arvates kurjast.
Pealegi saab seda (ERP) mõjutada ainult RFA.
Enne RFA-d on oluline vältida ravimeid, mis blokeerivad normaalset AV juhtivust, muutmata ebanormaalset (vastavalt DPP-le): beetablokaatorid ja verapamiil.
10.11.2011, 16:26
270–300 ms on nn tahhükardia aken - sellised ekstrastiimulite ühendamise (ja elus - ekstrasüstoolide) intervallid, mis vallandavad tahhükardia paroksüsmi.
AV-ühenduse ERP - 270 ms. See tähendab, et kiire ERP on suurem kui 270 ms. Järelikult on äkksurma oht väike.
Soovitatav on ikkagi teha RFA: kui teete RFA-d, siis krambihooge ei teki.
Tore oleks EKG-d näha.
10.11.2011, 17:17
Ja ma tahan ka küsida:
arütmiahoo ajal, kui vagaaltestid ei ole efektiivsed, milliseid ravimeid saab kasutada (mitte pidevalt, vaid spetsiaalselt leevendamiseks).
sotalex? või midagi muud?
ja millistes annustes.
ette tänades
Sotalool EI ole lubatud.
Optimaalselt IV ATP.
Alternatiivina prokaiinamiid (novokaiinamiid).
Või elektriline kardioversioon.
10.11.2011, 19:57
Tänud.
Homme panen ekg üles.
10.11.2011, 21:43
See toiming viiakse läbi kvoodi järgi, kuna see sisaldub kõrgtehnoloogilise ravi (kõrgtehnoloogilise ravi) mõistes. Pärast konsultatsiooni antakse teile saatekiri kvoodi saamiseks ehk riik maksab teie ravi kinni ja raha pole vaja otsida. Mis puudutab arsti, siis võin teile nõu anda, kui soovite. Tule minu juurde – nime saanud südame-veresoonkonnakirurgia teaduskeskus. A.N. Bakulev RAMS.
11.11.2011, 08:36
Tore oleks EKG-d näha.
ma kinnitan
See toiming viiakse läbi kvoodi järgi, kuna see sisaldub kõrgtehnoloogilise ravi (kõrgtehnoloogilise ravi) mõistes. Pärast konsultatsiooni antakse teile saatekiri kvoodi saamiseks ehk riik maksab teie ravi kinni ja raha pole vaja otsida. Mis puudutab arsti, siis võin teile nõu anda, kui soovite. Tule minu juurde – nime saanud südame-veresoonkonnakirurgia teaduskeskus. A.N. Bakulev RAMS.
Täname teid kutse eest. Kas saaksime seda küsimust ükshaaval arutada?
Mulle tundub, et kõige parem on seda teha telefoni teel.
kas sa saaksid mulle öelda oma koordinaadid?
E-posti aadress on foorumi reeglite kohaselt avalikust juurdepääsust eemaldatud. Moderaator.